Clear Sky Science · ar
ساعات الشيخوخة تميّز أنواع الخلايا العصبية المعرضة أو المقاومة للتحلّل العصبي وتحدّد تدخلات وقائية عصبية
لماذا تتقدم بعض خلايا الدماغ في العمر أسرع من غيرها
لماذا تذبل بعض خلايا الدماغ في وقت مبكر من الحياة بينما تظل أخرى قوية لعقود؟ يكمن هذا السؤال في صميم العديد من اضطرابات الشيخوخة، من الزهايمر إلى داء باركنسون. في هذه الدراسة، استعمل الباحثون دودة صغيرة مستديرة، Caenorhabditis elegans، التي خُرّط نظامها العصبي بأكمله خلية بخلاياها، ليفتحوا السؤال عما إذا كانت أنواع الخلايا العصبية المختلفة لها «أعمار بيولوجية» خاصة بها وما إذا كانت تلك الأعمار تتنبأ بالخلايا التي ستتحلّل. عملهم لا يقتصر على تحديد أنواع الخلايا المعرضة وعمليّة جزيئية تسرّع تدهورها، بل يكشف أيضاً جزيئات صغيرة يمكنها إبطاء أو تعجيل شيخوخة الخلايا العصبية — مقدمًا دلائل قد تمتد إلى الدماغ البشري.
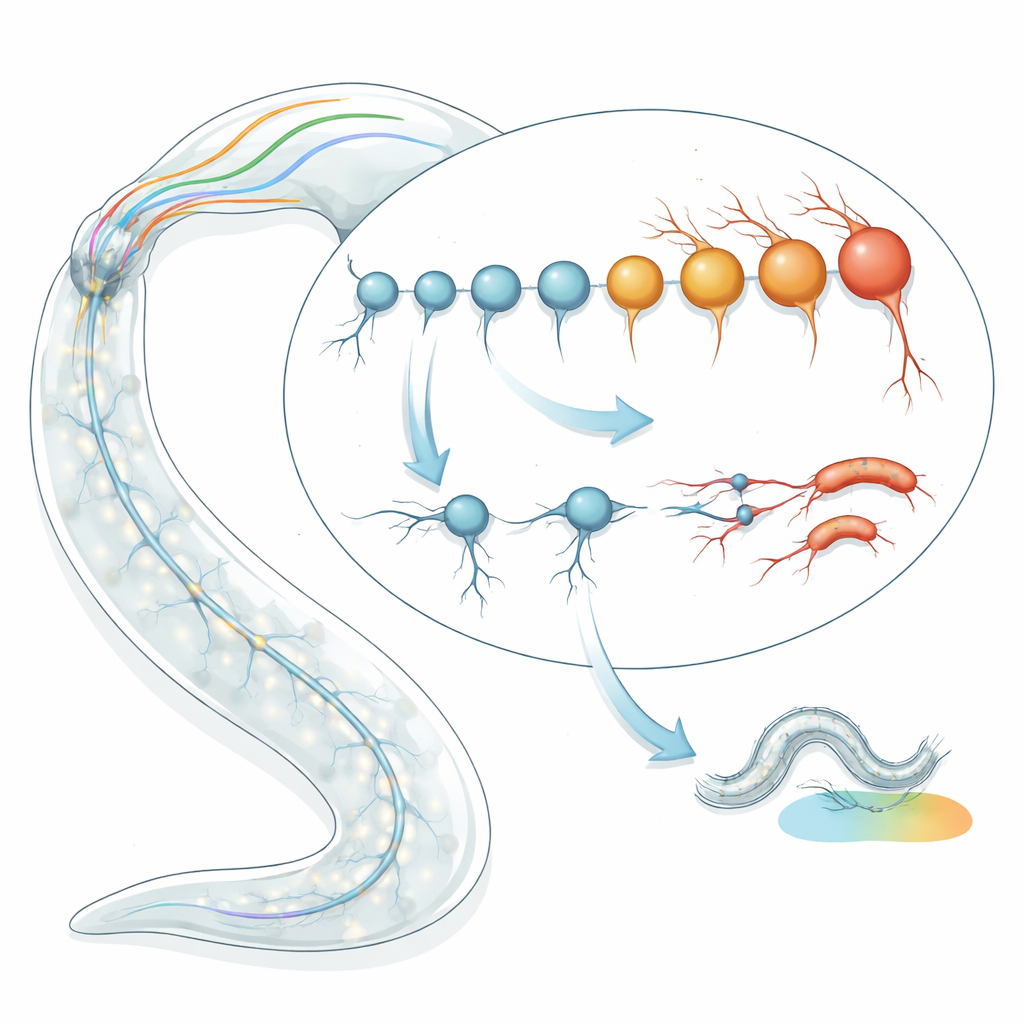
تأريخ عمر الخلايا العصبية الفردية
بدأ الفريق بتطبيق «ساعات» الشيخوخة المستندة إلى النسخ الجيني على أنواع الخلايا العصبية الفردية في C. elegans. بدلاً من النظر إلى عمر الدودة بالأيام، فحصوا أنماط نشاط الجينات لتقدير العمر البيولوجي لكل نوع خلية. باستخدام نموذجي ساعة مستقلين — أحدهما قائم على بصمات جينية مميّزة للشيخوخة والآخر يلتقط كيفية تراكم التغيرات العشوائية مع الزمن — حلّلوا بيانات تسلسل الرنا لأكثر من 128 نوع خلية عصبية محدّدة جيدًا في يرقات متأخرة وديدان بالغة شابة. وبشكل مفاجئ، وجدوا تباينًا يقارب ضعفين إلى أربعة أضعاف في العمر البيولوجي المتوقَّع بين خلايا عصبية كلّها تشترك في نفس العمر الزمني. بدا بعض الخلايا العصبية «أصغر سنًا» بكثير مما هو متوقع، في حين بدا البعض الآخر «مسنًا» قبل الأوان، وكانت هذه التقديرات متسقة عبر مجموعات بيانات وأساليب تسلسل متعددة.
من العمر الجزيئي إلى الضرر المرئي وفقدان السلوك
لاختبار ما إذا كانت هذه التنبؤات بالعمر ذات أهمية في ديدان حقيقية، تتبّع الباحثون حالة خلايا عصبية مختارة مع مرور الوقت باستخدام علامات فلورية. أظهرت الخلايا المتوقَّع أن تكون شابة بيولوجيًّا (مثل I2 وOLL وPHC) أضرارًا بنيوية طفيفة فقط في نسبة قليلة من الحيوانات مع تقدّم الديدان في العمر. على النقيض الحاد، أظهرت الخلايا المتوقعة أن تكون مسنّة (بما في ذلك ASI وASJ وASK) علامات تدهور بالفعل في ما يقرب من نصف اليرقات المتأخرة، وارتفعت النسبة إلى نحو 90% خلال أسبوع من البلوغ. بدا الضرر على شكل تورّمات ونموّات صغيرة على طول الألياف العصبية وزاد إلى حدّ كبير بشكل عشوائي على طول كل محوِّل عصبي، وهو ما يتوافق مع عملية شيخوخة عشوائية بدلاً من برنامج تنموي ثابت. كما ترجم التدهور البنيوي المبكر إلى عجز سلوكي فعلي: في الدوائر التي يتحكّم فيها نوع خلية عصبية واحد بمهمة محدّدة، طابق تدهور تلك الخلية بدقة فشلًا في تجنب المُمْرِض أو في التعلم المبني على الملح.
لماذا تكون الخلايا الحسية المكشوفة في خطر خاص
كشف رسم تقديرات العمر البيولوجي على خريطة الاتصال العصبي الكاملة للدودة نمطًا لافتًا. تجمع أقدم الخلايا العصبية بين خلايا حسية مهدبة في الرأس، خصوصًا خلايا الأمفيد whose cilia are directly exposed to the environment. هذه الخلايا تكتشف المواد الكيميائية والروائح وغيرها من الإشارات ومزدانة بغنى بالنيوروببتيدات والمستقبلات. عبر أنواع الخلايا العصبية، ارتبط عدد أكبر من النيوروببتيدات والمستقبلات المعبر عنها بعمر بيولوجي أقدم، بينما لم يرتبط عدد المشابك بوضوح. كانت الخلايا المهدبة التي تبرز نهاياتها الحسية إلى العالم الخارجي هي الأكثر تقدّمًا في العمر، ممّا يوحي بأن كلًّا من التعرض البيئي وحِمل الإشارة الثقيل قد يجعلانها عرضة للتدهور المبكر. هذا يلقى صدى في علم الأعصاب البشري، حيث تُعدُّ الخلايا العصبية المهدبة المكشوفة في الجهاز الشمي من أوائل الخلايا التي تتحلل في مرض الزهايمر.
تخليق البروتين كمحرّك — وكمفصل — للشيخوخة
لكشف الآليات الكامنة وراء هذه الفروقات العمرية، جمع الفريق الخلايا العصبية بحسب العمر البيولوجي وفحص اتجاهات التعبير الجيني. وجدوا أن العمليات المتعلقة بتكوين الرايبوسومات، وتخليق البروتين، ووظيفة النواة الفرعية (النوكليولوس) كانت مُثرية في الخلايا الشائخة، إلى جانب تغيّرات في جينات الإشارة عند المشابك والنيوروببتيدات. أشار ذلك إلى أن تخليق البروتين الكثيف قد يكون عبئًا يسرّع تآكل الخلايا العصبية. اختبر الباحثون بعد ذلك جرعة متواضعة من السيكلوهكسيميد، مركب يبطئ الترجمة جزئيًا. في الخلايا التي تتقدم سريعًا في العمر، أدّت هذه المثبطة الرقيقة إلى تقليل الضرر البنيوي بشكل ملحوظ والحفاظ على الأداء في مهمة تعلّم قائمة على الملح، مع تأثيرات وقائية استمرت حتى بعد وقف العلاج. بالمقابل، كانت الخلايا الأبطأ عمرًا أقل تأثرًا. تربط هذه النتائج حِمل الترجمة العالي بالعرضة النوعية للخلايا العصبية وتظهر أن خفض تخليق البروتين يمكن أن يستعيد السلامة البنيوية والوظيفية في الخلايا المعرضة للخطر.
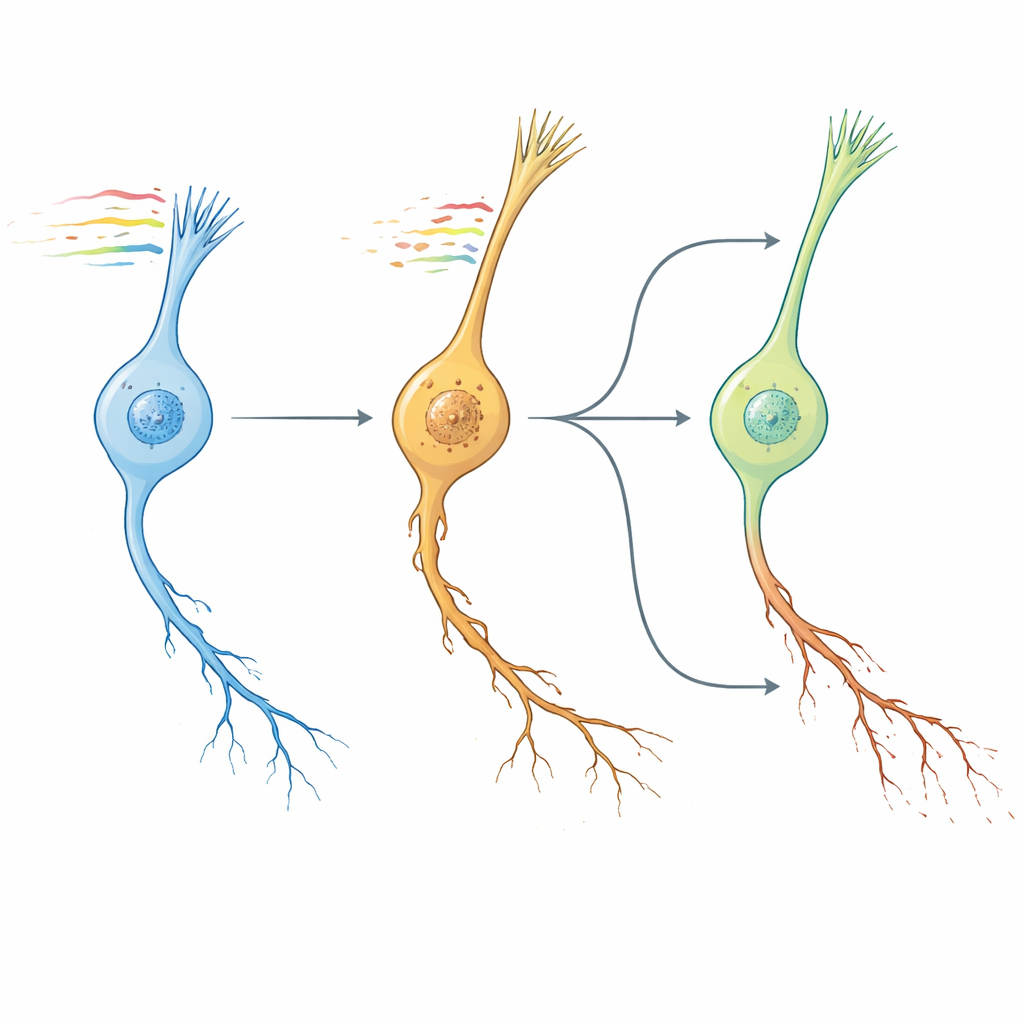
ساعات الدودة، أدمغة البشر، ومرشّحات أدوية
بعد ذلك، تساءل المؤلفون عما إذا كان نمط شيخوخة الخلايا العصبية في الدودة يشبه شيخوخة الدماغ في الثدييات. بمقارنة تغيّرات على مستوى المسارات عبر الجينات المحفوظة، وجدوا أن بصمة «عمر الخلية العصبية» النسيجية في C. elegans تجمعت بإحكام مع مسارات الشيخوخة من مناطق دماغية متعددة في الفأر والإنسان، بينما أظهرت تدخلات معروفة بأنها محمية من الشيخوخة — مثل عوامل الدم الشاب والتمارين والمركبات الغذائية — أنماطًا معاكسة. مستغلين هذا الحفظ، توجّهوا إلى مورد خلايا بشرية واسع للبحث الكمبيوترى عن جزيئات صغيرة تكون تأثيراتها مضادة أو مقلدة لبصمة NeuronAge. وُسمت المركبات التي عكست NeuronAge كمحتمَلات حامية عصبيًا؛ بينما وُصفت تلك التي دعمتها كمحتملة سامة عصبيًا. اختبارات تجريبية في الديدان صادقت على عدة تنبؤات. قلّلت مادة نباتية من الاستقلاب تُدعى حمض السرينجيك والدواء فانكسرين من التحلّل في الخلايا سريعة الشيخوخة دون أن تضر الخلايا الشابة، بينما زيّدت عوامل مثل Bay K8644 وWAY-100635 من تلف المحاور العصبية وأضعفت السلوك. حتى الريسفيراترول، الذي يُروّج له غالبًا كمادة حامية، ظهر هنا كعامل معزّز للشيخوخة وزاد من الباثولوجيا العصبية.
ماذا يعني هذا لصحة الدماغ
باختصار، تُظهر هذه الدراسة أنه حتى داخل جهاز عصبي واحد، تسير أنواع خلايا عصبية مختلفة عبر مسارات الشيخوخة بسرعات متباينة، وأن هذه الساعات الداخلية تتنبأ بالخلايا التي ستتحلل وتفقد وظيفتها أولًا. تبدو الخلايا الحسية المواجهة للعالم الخارجي والمكثّفة في إنتاج البروتين هشة بشكل خاص. من خلال ربط الشيخوخة النوعية للخلايا العصبية بمسارات التعبير الجيني المحفوظة، تقدّم الدراسة وسيلة لترجمة الرؤى من دودة بسيطة إلى دماغ الإنسان. والأهم من ذلك، تُظهر أن بصمات الشيخوخة النسيجية يمكن استخدامها كمرشّح قوي لتحديد جزيئات تُبطئ أو تُسرّع التحلّل العصبي. وبينما لا يزال الكثير مطلوبًا قبل أن تُؤخذ هذه المرشّحات بعين الاعتبار للعلاج البشري، يشير النهج إلى مستقبل يمكننا فيه ليس فقط قياس العمر البيولوجي لأنواع الخلايا العصبية الفردية، بل أيضًا تصميم تدخلات مدروسة لإبقائها أصغر سنًا لفترة أطول.
الاستشهاد: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
الكلمات المفتاحية: شيخوخة عصبية, التحلّل العصبي, تخليق البروتين, Caenorhabditis elegans, حماية عصبية