Clear Sky Science · de
Alterungsuhren unterscheiden Neuronentypen, die gegenüber Neurodegeneration anfällig oder widerstandsfähig sind, und identifizieren neuroprotektive Interventionen
Warum einige Gehirnzellen schneller altern als andere
Warum gehen einige Gehirnzellen frühzeitig zugrunde, während andere über Jahrzehnte hinweg robust bleiben? Diese Frage steht im Zentrum vieler altersbedingter Erkrankungen, von Alzheimer bis Parkinson. In dieser Studie nutzten Forschende den winzigen Fadenwurm Caenorhabditis elegans, dessen komplettes Nervensystem zellengenau kartiert ist, um zu untersuchen, ob verschiedene Neuronentypen eigene „biologische Alter“ aufweisen und ob diese Alter vorhersagen, welche Zellen degenerieren. Die Arbeit identifiziert nicht nur besonders anfällige Neuronentypen und einen molekularen Prozess, der ihren Verfall beschleunigt, sondern liefert auch kleine Moleküle, die das neuronale Altern verlangsamen oder beschleunigen können — Hinweise, die auf das menschliche Gehirn übertragbar sein könnten.
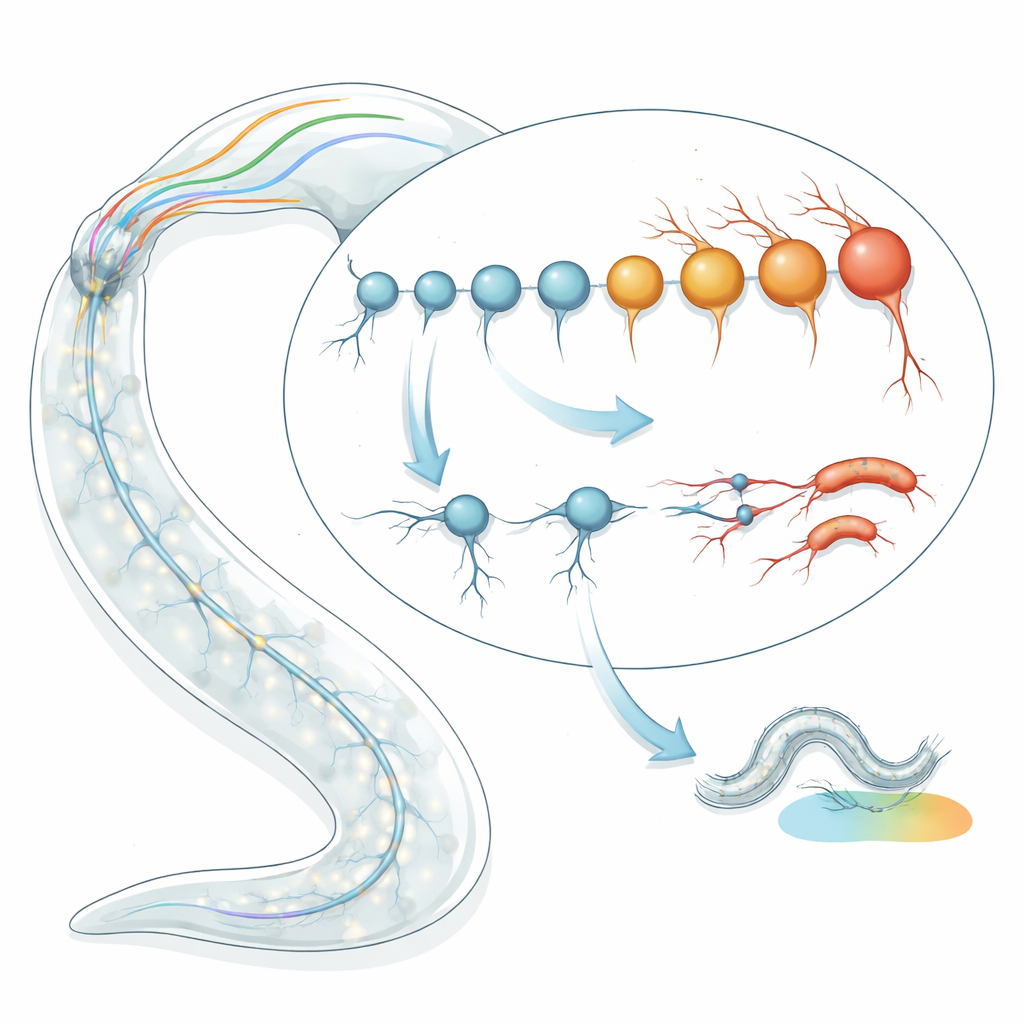
Das Alter einzelner Nervenzellen bestimmen
Das Team begann damit, transkriptomische „Alterungsuhren“ auf einzelne Neuronentypen in C. elegans anzuwenden. Anstatt das Alter des Wurms in Tagen zu betrachten, analysierten sie Muster der Genaktivität, um das biologische Alter jedes Zelltyps zu schätzen. Mit zwei unabhängigen Uhrmodellen — einem, das auf charakteristischen Altersgenen beruht, und einem anderen, das erfasst, wie sich zufällige Veränderungen im Laufe der Zeit anhäufen — werteten sie RNA-Sequenzdaten für 128 gut definierte Neuronentypen in späten Larven- und jungen Adultstadien aus. Überraschenderweise fanden sie eine fast zwei- bis vierfache Streuung im vorhergesagten biologischen Alter unter Neuronen desselben chronologischen Alters. Einige Neuronen erschienen deutlich „jünger“ als erwartet, andere wirkten vorzeitig „alt“, und diese Schätzungen waren über mehrere Datensätze und Sequenziermethoden hinweg konsistent.
Vom molekularen Alter zu sichtbaren Schäden und Funktionsverlust
Um zu prüfen, ob diese Altersvorhersagen in realen Würmern relevant sind, verfolgten die Forschenden den physischen Zustand ausgewählter Neuronen über die Zeit mit fluoreszenten Markern. Neuronen, die biologisch jung vorhergesagt wurden (wie I2, OLL und PHC), zeigten im Alter nur in einer Minderheit der Tiere leichte strukturelle Schäden. Im krassen Gegensatz dazu wiesen Neuronen, die als alt vorhergesagt wurden (darunter ASI, ASJ und ASK), bereits in fast der Hälfte der späten Larven Anzeichen von Verschleiß auf, und dieser Anteil stieg bis zur ersten Erwachsenenwoche auf etwa 90 % an. Die Schäden traten als winzige Schwellungen und Auswüchse entlang der Nervenfasern auf und verteilten sich ungefähr zufällig entlang der einzelnen Neurite, was zu einem stochastischen Alterungsprozess eher als zu einem festen Entwicklungsprogramm passt. Der frühe strukturelle Verfall zeigte sich auch in echten Verhaltensdefiziten: In Schaltkreisen, in denen ein einzelner Neuronentyp eine spezifische Aufgabe steuert, stimmte die Degeneration dieses Neurons eng mit Ausfällen bei der Vermeidung von Krankheitserregern oder beim Lernen an Salzkonzentrationen überein.
Warum exponierte sensorische Neuronen ein besonderes Risiko tragen
Die Zuordnung der biologischen Altersabschätzungen zum vollständigen Konnektom des Wurm-Nervensystems zeigte ein auffälliges Muster. Die ältesten Neuronen konzentrierten sich unter den gekräuselten (zilierten) sensorischen Zellen im Kopf, insbesondere bei den Amphid-Neuronen, deren Zilien direkt der Umwelt ausgesetzt sind. Diese Zellen detektieren Chemikalien, Gerüche und andere Reize und sind reich an Neuropeptiden und Rezeptoren. Über die Neuronentypen hinweg korrelierte eine höhere Anzahl exprimierter Neuropeptide und Rezeptoren mit einem höheren biologischen Alter, während die bloße Anzahl der Synapsen nicht mit dem Alter zusammenhing. Ziliare Neuronen, deren sensorische Enden in die Außenwelt ragen, waren am stärksten gealtert, was darauf hindeutet, dass sowohl Umwelteinflüsse als auch hohe Signalbelastung sie für einen frühen Verfall prädisponieren. Dies spiegelt Befunde aus der Humanneurologie wider, wo exponierte, ziliare Neuronen im Riechsystem zu den ersten gehören, die bei Alzheimer- Erkrankungen degenerieren.
Proteinsynthese als Treiber — und Ansatzpunkt — des Alterns
Um Mechanismen hinter diesen Altersunterschieden aufzudecken, gruppierten die Forschenden Neuronen nach biologischem Alter und untersuchten Trends in der Genexpression. Sie stellten fest, dass Prozesse im Zusammenhang mit Ribosomenbiogenese, Proteinsynthese und nucleolarer Funktion in älteren Neuronen angereichert waren, zusammen mit Veränderungen in Synapsen- und Neuropeptidsignalisierungsgenen. Dies deutet darauf hin, dass hohe Proteinsynthese eine mögliche Belastung darstellt, die den neuronalen Verschleiß beschleunigt. Die Forschenden testeten daraufhin eine geringe Dosis Cycloheximid, eine Verbindung, die die Translation teilweise verlangsamt. Bei schnell alternden Neuronen reduzierte diese milde Hemmung strukturelle Schäden deutlich und erhielt die Leistung in einer Salzl ernpfaufgabe, wobei der Schutz auch nach Absetzen der Behandlung anhielt. Langsam alternde Neuronen blieben hingegen weitgehend unbeeinflusst. Diese Ergebnisse verknüpfen hohe translatorische Belastung mit neuronenspezifischer Verwundbarkeit und zeigen, dass das Herunterregeln der Proteinsynthese strukturelle und funktionelle Integrität gefährdeter Zellen wiederherstellen kann.
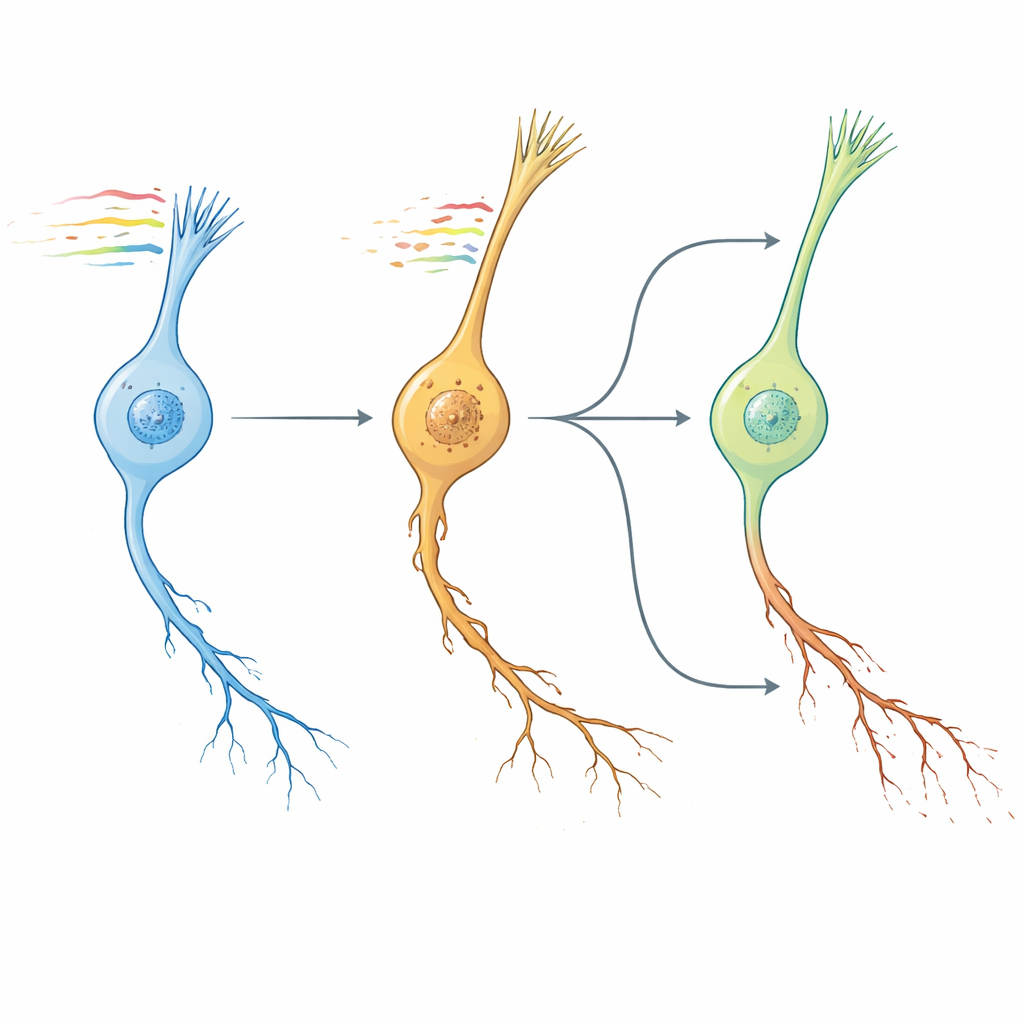
Wurmuhren, menschliche Gehirne und Wirkstoffkandidaten
Als Nächstes fragten die Autorinnen und Autoren, ob das Altersmuster der Wurmneuronen dem Gehirnalterungsprozess bei Säugetieren ähnelt. Durch den Vergleich von Wegveränderungen auf Ebene konservierter Gene fanden sie, dass die transkriptomische „NeuronAge“-Signatur in C. elegans eng mit Alterungstrajektorien aus mehreren Maus- und menschlichen Hirnregionen gruppierte, während bekannte geroprotektive Interventionen — wie Faktoren aus jungem Blut, Bewegung und diätetische Verbindungen — entgegengesetzte Muster zeigten. Diese Konservierung nutzend, griffen sie auf eine große humanzelllinienbasierte Ressource zurück, um in silico nach kleinen Molekülen zu suchen, deren Wirkung NeuronAge entgegenwirkt oder imitiert. Verbindungen, deren Profile NeuronAge entgegenwirkten, wurden als potenzielle Neuroprotektiva markiert; jene, die es verstärkten, als potenzielle Neurotoxine. Experimentelle Tests in Würmern bestätigten mehrere Vorhersagen. Der pflanzliche Metabolit Syringinsäure und das Medikament Vanoxerin verringerten die Degeneration in schnell alternden Neuronen, ohne junge Zellen zu schädigen, während Substanzen wie Bay K8644 und WAY-100635 neuritische Schäden verschärften und Verhalten beeinträchtigten. Selbst Resveratrol, oft als protektiv gepriesen, zeigte in diesem System pro-aging-Eigenschaften und erhöhte neuronale Pathologie.
Was das für die Hirngesundheit bedeutet
Im Kern zeigt diese Arbeit, dass innerhalb eines einzelnen Nervensystems verschiedene Neuronentypen mit unterschiedlichen Geschwindigkeiten altern und dass diese internen Uhren vorhersagen, welche Zellen zuerst degenerieren und ihre Funktion verlieren. Sensorische Neuronen, die der Außenwelt ausgesetzt sind und hohe Proteinsynthese betreiben, erscheinen besonders fragil. Indem das neuronenspezifische Altern mit konservierten Expressionspfaden verknüpft wird, bietet die Studie einen Weg, Erkenntnisse aus einem einfachen Wurm auf das menschliche Gehirn zu übertragen. Ebenso wichtig ist, dass transkriptomische Alterungssignaturen als leistungsfähiger Filter dienen können, um Moleküle zu identifizieren, die Neurodegeneration verlangsamen oder beschleunigen. Zwar ist noch viel zu tun, bevor diese Kandidaten für die Anwendung beim Menschen in Betracht gezogen werden können, doch der Ansatz weist in eine Zukunft, in der wir nicht nur das biologische Alter einzelner Neuronentypen messen, sondern auch gezielt Interventionen entwickeln können, um sie länger jünger zu halten.
Zitation: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Schlüsselwörter: neuronalem Altern, Neurodegeneration, Proteinsynthese, Caenorhabditis elegans, Neuroprotektion