Clear Sky Science · fr
Les horloges du vieillissement distinguent les types de neurones vulnérables ou résilients à la neurodégénérescence et identifient des interventions neuroprotectrices
Pourquoi certaines cellules cérébrales vieillissent plus vite que d’autres
Pourquoi certaines cellules cérébrales se détériorent-elles tôt dans la vie tandis que d’autres restent robustes pendant des décennies ? Cette question est au cœur de nombreux troubles liés à l’âge, de la maladie d’Alzheimer à la maladie de Parkinson. Dans cette étude, les chercheurs ont utilisé un petit nématode, Caenorhabditis elegans, dont le système nerveux complet est cartographié cellule par cellule, pour se demander si différents types neuronaux possèdent des « âges biologiques » propres et si ces âges prédisent quelles cellules dégénéreront. Leur travail identifie non seulement les types neuronaux vulnérables et un processus moléculaire accélérant leur déclin, mais révèle aussi de petites molécules capables de ralentir ou d’accélérer le vieillissement neuronal — des indices potentiellement transposables au cerveau humain.
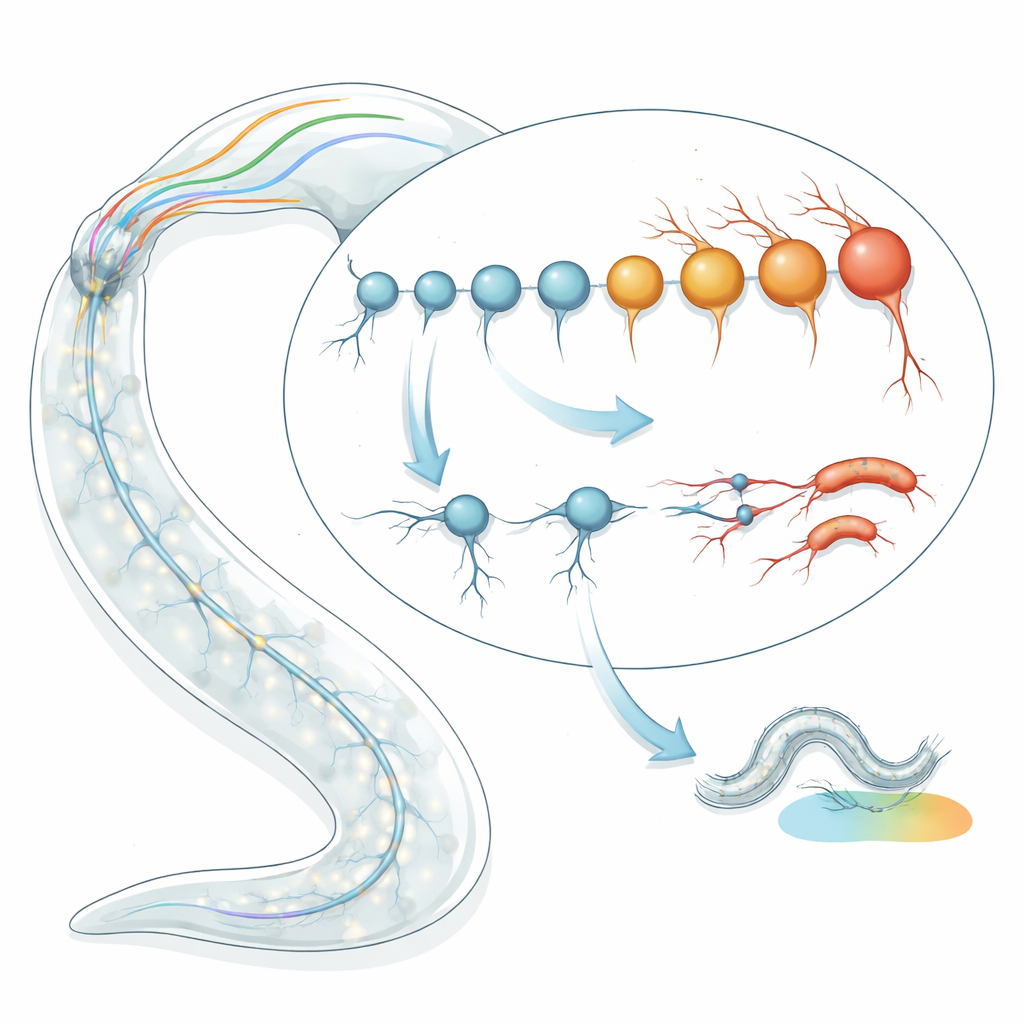
Chronométrer l’âge de cellules nerveuses individuelles
L’équipe a commencé par appliquer des « horloges » transcriptomiques du vieillissement à des types neuronaux individuels chez C. elegans. Plutôt que de considérer l’âge du ver en jours, ils ont examiné des profils d’activité génique pour estimer l’âge biologique de chaque type cellulaire. En utilisant deux modèles d’horloge indépendants — l’un fondé sur des signatures géniques caractéristiques du vieillissement et l’autre capturant l’accumulation de changements aléatoires au fil du temps — ils ont analysé des données de séquençage ARN pour 128 types neuronaux bien définis chez des larves tardives et de jeunes adultes. De manière surprenante, ils ont observé un écart d’environ deux à quatre fois dans l’âge biologique prédit parmi des neurones ayant le même âge chronologique. Certains neurones semblaient beaucoup plus « jeunes » que prévu, tandis que d’autres paraissaient prématurément « vieux », et ces estimations étaient cohérentes entre plusieurs jeux de données et méthodes de séquençage.
De l’âge moléculaire aux dommages visibles et à la perte de comportements
Pour vérifier si ces prédictions d’âge avaient un impact dans des vers vivants, les chercheurs ont suivi au fil du temps l’état physique de neurones choisis à l’aide de marqueurs fluorescents. Les neurones prédits comme biologiquement jeunes (par exemple I2, OLL et PHC) montraient seulement des dégâts structurels légers chez une minorité d’animaux avec l’âge. En contraste marqué, les neurones prédits comme vieux (dont ASI, ASJ et ASK) présentaient déjà des signes de détérioration chez près de la moitié des larves tardives, atteignant environ 90 % à une semaine d’âge adulte. Les dommages se manifestaient par de petites enflures et des excroissances le long des fibres nerveuses et apparaissaient de manière essentiellement aléatoire le long de chaque neurite, compatible avec un processus de vieillissement stochastique plutôt qu’un programme développemental fixe. Le déclin structurel précoce se traduisait aussi par des déficits comportementaux réels : dans des circuits où un seul type de neurone contrôle une tâche spécifique, la dégénérescence de ce neurone correspondait étroitement à des échecs dans l’évitement des pathogènes ou l’apprentissage lié au sel.
Pourquoi les neurones sensoriels exposés sont particulièrement à risque
Cartographier les estimations d’âge biologique sur le connectome complet du ver a révélé un schéma frappant. Les neurones les plus âgés se regroupaient parmi les cellules sensorielles ciliées dans la tête, en particulier les neurones amphidiaux dont les cils sont directement exposés à l’environnement. Ces cellules détectent des produits chimiques, des odeurs et d’autres signaux et sont riches en neuropeptides et en récepteurs. À travers les types neuronaux, un nombre plus élevé de neuropeptides et de récepteurs exprimés corrélait avec un âge biologique plus avancé, alors que le simple nombre de synapses ne le faisait pas. Les neurones ciliés dont les terminaisons sensorielles émergent vers l’extérieur étaient les plus âgés, ce qui suggère que l’exposition environnementale et une charge de signalisation élevée peuvent les prédisposer à un déclin précoce. Cela fait écho à la neurologie humaine, où des neurones ciliés exposés dans le système olfactif sont parmi les premiers à dégénérer dans la maladie d’Alzheimer.
La production de protéines comme moteur — et levier — du vieillissement
Pour découvrir les mécanismes sous-jacents à ces différences d’âge, l’équipe a regroupé les neurones par âge biologique et examiné les tendances d’expression génique. Ils ont trouvé que des processus liés à la biogenèse des ribosomes, la synthèse protéique et la fonction nucléolaire étaient enrichis dans les neurones plus âgés, ainsi que des changements dans les gènes de signalisation synaptique et des neuropeptides. Cela pointe vers une forte production protéique comme charge possible qui accélère l’usure neuronale. Les chercheurs ont ensuite testé une faible dose de cycloheximide, un composé qui ralentit partiellement la traduction. Dans les neurones vieillissant rapidement, cette inhibition modeste a significativement réduit les dégâts structurels et préservé les performances dans une tâche d’apprentissage au sel, avec des effets protecteurs persistants même après l’arrêt du traitement. Les neurones vieillissant plus lentement, en revanche, étaient largement non affectés. Ces résultats relient une charge translationnelle élevée à la vulnérabilité neuronale spécifique et montrent que réduire la synthèse protéique peut restaurer l’intégrité structurelle et fonctionnelle des cellules à risque.
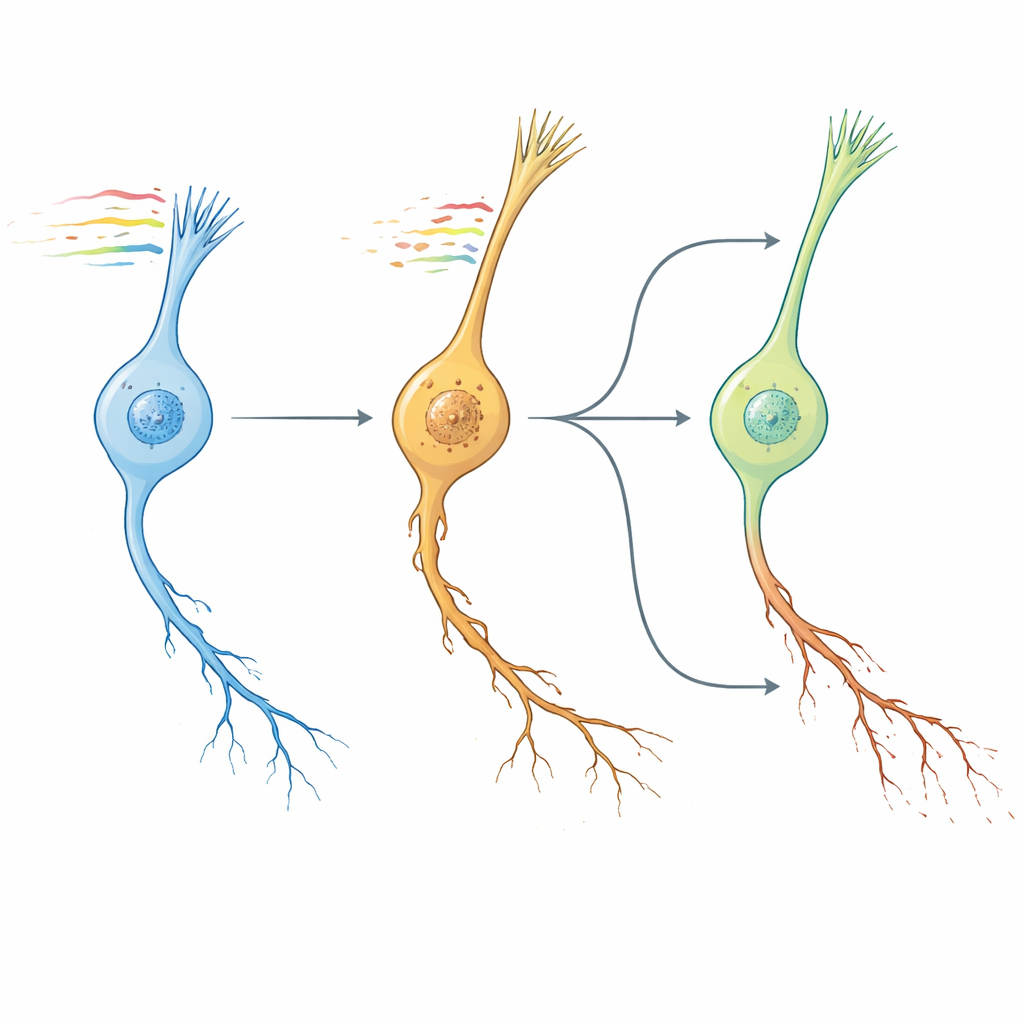
Des horloges du ver aux cerveaux humains, et des pistes médicamenteuses
Les auteurs se sont ensuite demandé si leur schéma de vieillissement neuronal chez le ver ressemblait au vieillissement cérébral chez les mammifères. En comparant les changements au niveau des voies entre gènes conservés, ils ont trouvé que la signature transcriptomique « NeuronAge » chez C. elegans se rapprochait fortement des trajectoires de vieillissement observées dans plusieurs régions cérébrales de souris et d’humains, tandis que des interventions connues pour être géroprotectrices — comme des facteurs présents dans le sang jeune, l’exercice et certains composés alimentaires — montraient des profils opposés. Tirant parti de cette conservation, ils se sont tournés vers une vaste ressource de lignées cellulaires humaines pour rechercher in silico de petites molécules dont les effets contrarieraient ou imiteraient NeuronAge. Les composés dont les profils s’opposaient à NeuronAge ont été signalés comme potentiels neuroprotecteurs ; ceux qui le renforçaient comme potentiels neurotoxiques. Des tests expérimentaux chez le ver ont validé plusieurs prédictions. Le métabolite d’origine végétale acide syringique et le médicament vanoxerine ont tous deux réduit la dégénérescence dans les neurones vieillissant rapidement sans nuire aux neurones jeunes, tandis que des agents comme Bay K8644 et WAY-100635 ont aggravé les dommages aux neurites et altéré le comportement. Même le resvératrol, souvent présenté comme protecteur, est apparu pro-vieillissement dans ce système et a augmenté la pathologie neuronale.
Ce que cela signifie pour la santé cérébrale
Essentiellement, ce travail montre que, même au sein d’un seul système nerveux, différents types neuronaux traversent le vieillissement à des rythmes différents, et que ces horloges internes prédisent quelles cellules dégénéreront et perdront leur fonction en premier. Les neurones sensoriels exposés et soumis à une forte production protéique semblent particulièrement fragiles. En reliant le vieillissement spécifique aux neurones à des voies d’expression génique conservées, l’étude offre une voie de traduction des informations d’un ver simple vers le cerveau humain. Tout aussi important, elle démontre que les signatures transcriptomiques du vieillissement peuvent servir de filtre puissant pour identifier des molécules qui ralentissent ou accélèrent la neurodégénérescence. Bien qu’il reste beaucoup à faire avant que ces candidats puissent être envisagés pour une thérapie humaine, l’approche ouvre la perspective d’un futur où nous pourrons non seulement mesurer l’âge biologique de types neuronaux individuels, mais aussi concevoir rationnellement des interventions pour les maintenir plus jeunes plus longtemps.
Citation: Gallrein, C., Meyer, D.H., Woitzat, Y. et al. Aging clocks delineate neuron types vulnerable or resilient to neurodegeneration and identify neuroprotective interventions. Nat Aging 6, 849–868 (2026). https://doi.org/10.1038/s43587-026-01067-5
Mots-clés: vieillissement neuronal, neurodégénérescence, synthèse protéique, Caenorhabditis elegans, neuroprotection