Clear Sky Science · zh
TH5487在对MCC950耐药的FCAS患者中特异性靶向NLRP3
为何平息失控炎症至关重要
从罕见发热综合征到与年龄相关的疾病,许多慢性病都由一种无法关闭的免疫报警系统驱动。本研究探索了能够抑制人体最强大的炎症开关之一——NLRP3——的新药候选物,同时不完全抑制免疫防御。通过重新考察最初用于DNA修复的现有分子,作者发现了一种抑制有害炎症的新途径,甚至可将其重新导向更具保护性的抗病毒式反应。
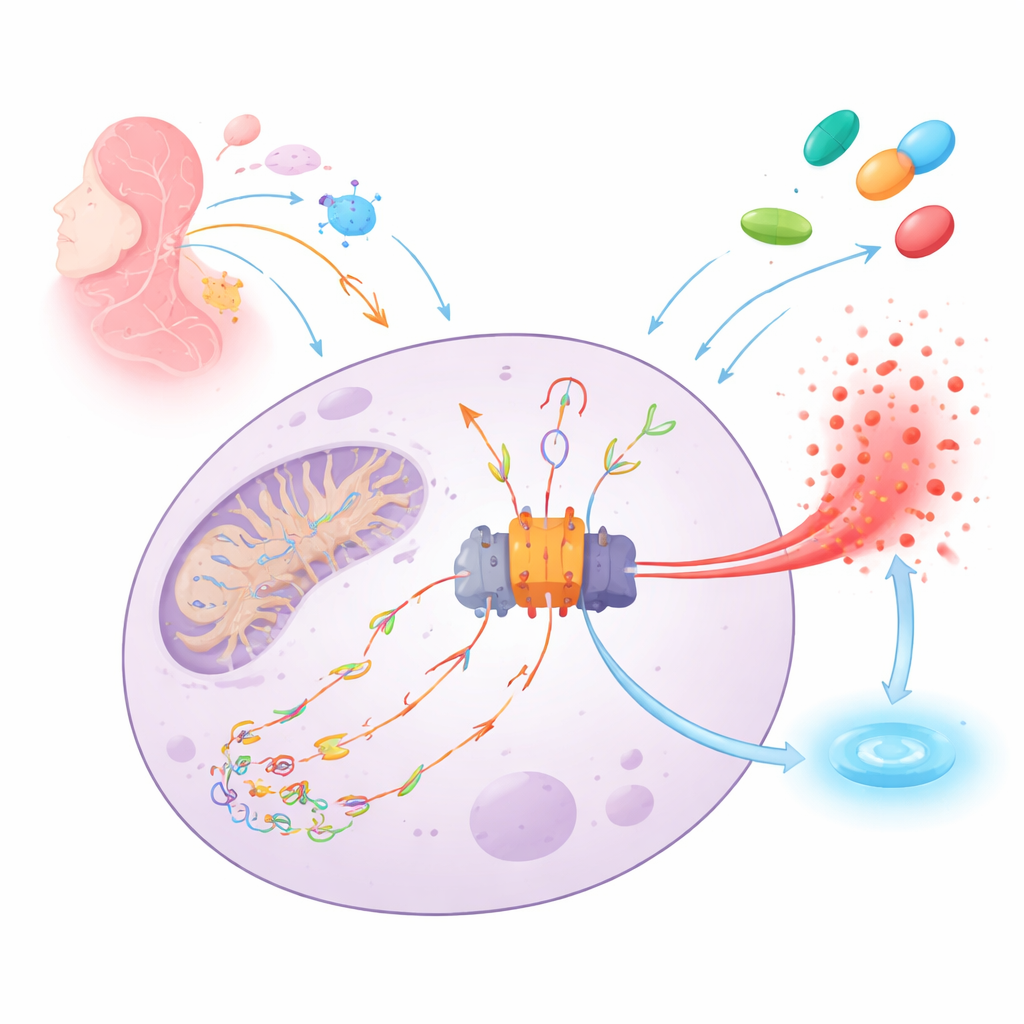
体内的火警与导火索
NLRP3在免疫细胞内像分子烟雾探测器一样工作。当它感知到危险——从感染到组织损伤——就会组装成一个大型蛋白机器(炎症小体),触发强效报警信号IL‑1β的释放,并可导致细胞破裂以警示邻近细胞。促发该警报的关键导火索之一是被活性氧切割并氧化的线粒体DNA。这些受损的DNA片段可以从线粒体泄出、在细胞内游离、与NLRP3结合,进而促进炎症小体组装和炎性细胞死亡。
旧的DNA修复药物,新的抗炎作用
作者考察了最初针对一种称为hOGG1的DNA修复酶(负责去除DNA中的氧化碱基)设计的小分子。出人意料的是,这些药物——TH5487、SU0268以及一种名为TH10785的激活剂——也能与NLRP3相互作用。在人外周血免疫细胞和模型细胞系中,低微摩尔浓度的TH5487和SU0268显著降低了IL‑1β的释放及成熟该细胞因子的酶caspase‑1的活化。详尽的蛋白质捕获和成像实验表明,这些药物阻止NLRP3组装完整的炎症小体复合体:它们阻断了关键伙伴(ASC、NEK7和pro‑caspase‑1)的招募,并减少了标志活性炎症小体的亮色“斑点”形成。
切断受损DNA与炎症小体之间的联系
鉴于线粒体损伤是NLRP3活性的重要驱动因素,研究团队测试了这些药物是否能抑制由线粒体应激触发的炎症小体活化。一种破坏细胞能量工厂并提高活性氧的化合物通常会将氧化的线粒体DNA导向NLRP3,并显著提高IL‑1β水平。TH5487和SU0268不仅在这些条件下减少了IL‑1β的释放,还降低了在与线粒体相关的NLRP3数量。冷冻电子显微镜证实,NLRP3可以形成一个大型环状复合体,物理结合线粒体DNA,计算机建模则提示该蛋白的pyrin结构域通过带正电的表面斑块识别氧化的单链DNA。这些药物干扰了该DNA感知步骤,从而切断了受损DNA与失控炎症之间的关键联系。
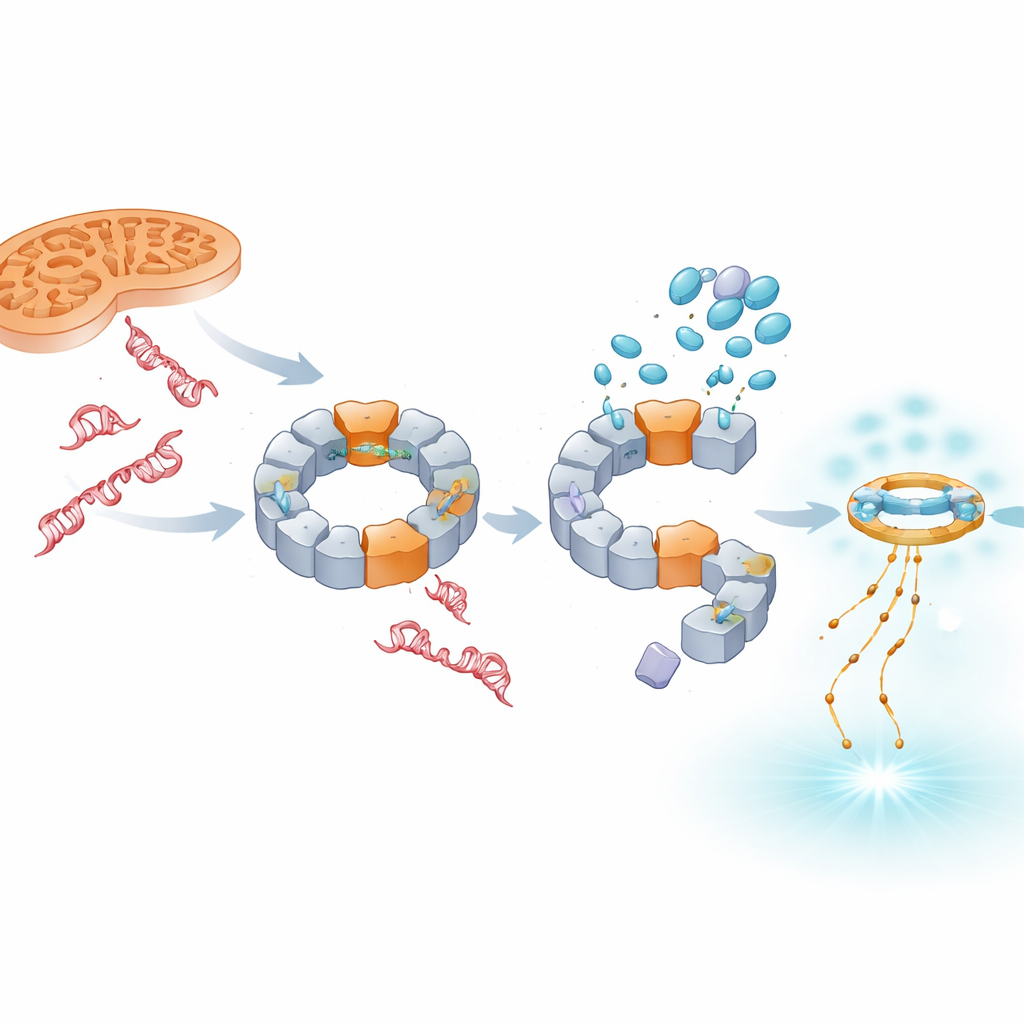
将信号转向抗病毒式防御
抑制NLRP3并不会让受损的DNA消失;相反,更多的DNA,尤其是来自细胞核的DNA,会在细胞液中积累。研究表明,这些过量DNA会被另一套传感系统cGAS–STING捕获,该系统通常响应病毒基因组。当存在TH5487、SU0268或TH10785时,激活的STING和抗病毒信使IFN‑β在模型细胞和原代人血细胞中水平上升。重要的是,这种增强即便在基因上敲除NLRP3的情况下仍然发生,表明cGAS–STING作为一个独立的后备报警系统发挥作用。因此,这些化合物在压制IL‑1β驱动的炎症的同时,使免疫反应倾向于可能在慢性病中更具保护性的干扰素信号。
对难治遗传性炎症的希望
一项特别引人注目的测试涉及家族性冷诱发自身炎症综合征(FCAS),这是一种罕见疾病,NLRP3的突变使其过度活跃并对一种领先的试验性抑制剂MCC950产生耐药。在携带这些突变的小鼠和人患者的免疫细胞中,MCC950无法抑制IL‑1β的释放。然而,TH5487和SU0268在不损害细胞存活性的剂量下显著降低了这种过度产生。这表明靶向NLRP3的氧化DNA感知表面,而非其更传统的酶促核心,可能绕过耐药性,为目前缺乏靶向疗法的患者提供新的治疗选择。
这些发现对未来治疗的意义
对非专业读者而言,核心信息是研究者发现了细胞内一台强大炎症机器的新“关断”方式。通过重新利用DNA修复药物阻断NLRP3感知受损的线粒体和核DNA的方式,他们能够抑制慢性炎症的主要来源,同时让另一条通路接管并产生抗病毒的干扰素信号。如果这一策略在进一步研究中被证明安全,它不仅可能为像FCAS这样的罕见遗传性发热综合征开辟靶向治疗途径,也可能适用于广泛的“炎性老化”状况,其中持续的、低度炎症推动疾病进展。
引用: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
关键词: NLRP3炎症小体, 氧化线粒体DNA, TH5487, cGAS-STING通路, 自身炎症性疾病