Clear Sky Science · he
TH5487 פועל במיוחד על NLRP3 בחולי FCAS העמידים ל‑MCC950
למה חשוב להשקיט דלקת שברחה משליטה
מחלות כרוניות רבות, ממחוסר חום נדיר ועד הפרעות הקשורות להזדקנות, מונעות על‑ידי מערכת אזעקה חיסונית שמסרבת להיכבות. המחקר בוחן מועמדי תרופות חדשים שיכולים להרגיע אחד המתגים העוצמתיים של הדלקת בגוף, הנקרא NLRP3, מבלי לכבות את מערכות ההגנה שלנו לחלוטין. על ידי חשיבה מחדש על מולקולות קיימות שתוכננו במקור כלפי תיקון DNA, המחברים חושפים דרך חדשה לרסן דלקת מזיקה ואפילו לנתב אותה לתגובה אנטי‑ויראלית מגן יותר.
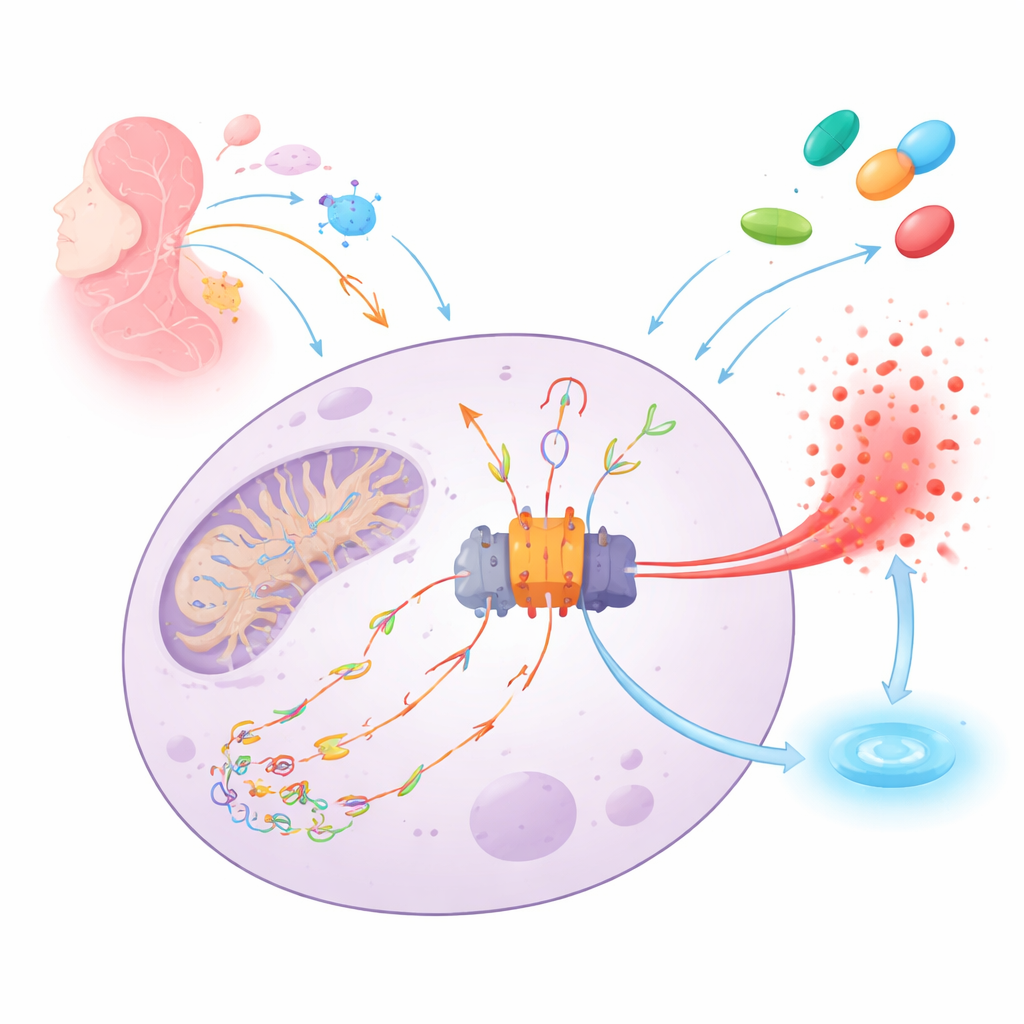
מערכת האזעקה של הגוף והנציצות שמפעילה אותה
NLRP3 פועל כמו גלאי עשן מולקולרי בתוך תאי מערכת החיסון. כאשר הוא מזהה סכנה — החל מזיהומים ועד לנזק רקמתי — הוא מרכיב מכונת חלבון גדולה (האינפלמזום) שמפעילה שחרור של אות האזעקה החזק IL‑1β ועלולה לקרוע את התא כדי להתריע לשכנים. ניצוץ מרכזי לאזעקה זו הוא DNA מיטוכונדריאלי שניזוק, נותק וחומצן על‑ידי מולקולות חמצון ריאקטיביות. שברי DNA פגומים אלה יכולים לדלוף מהמיטוכונדריה, לשוטט בתא, להיקשר ל‑NLRP3 ולהניע את הרכבת האינפלמזום ומוות דלקתי תאי.
תרופות ישנות לתיקון DNA — תפקידים אנטי‑דלקתיים חדשים
החוקרים בחנו מולקולות קטנות שתוכננו בתחילה לכוון אנזים לתיקון DNA בשם hOGG1, המסיר בסיסים מחומצנים מתוך ה‑DNA. באופן מפתיע, תרופות אלה — TH5487, SU0268 ומפעיל בשם TH10785 — גם מתקשרות עם NLRP3. בתאי דם חיסוניים אנושיים ובשורות תאים מודליות, מינונים נמוכים במיקרומול של TH5487 ו‑SU0268 הקטינו באופן חד את שחרור ה‑IL‑1β ואת הפעלתו של קספאז‑1, האנזים שמבשיל את הציטוקין הזה. ניסויים מפורטים של משיכות חלבון (pull‑down) והדמיה הראו שהתרופות מונעות מ‑NLRP3 להרכיב את קומפלקס האינפלמזום המלא: הן חוסמות גיוס של שותפים מרכזיים (ASC, NEK7 ו‑pro‑caspase‑1) ומפחיתות את היווצרות ה"נקודות" הבהירות שמסמנות אינפלמזום פעיל.
גיזום הקשר בין DNA פגום לאינפלמזום
מכיוון שנזק מיטוכונדריאלי הוא דוחף מרכזי לפעילות NLRP3, הצוות בדק האם התרופות יכולות לחסום הפעלת אינפלמזום שמתרחשת בעקבות מתח מיטוכונדריאלי. תרכובת שמפרקת את תחנות האנרגיה של התא ומגבירה רדיקלים חופשיים בדרך כלל שולחת DNA מיטוכונדריאלי מחומצן לכיוון NLRP3 ומגבירה מאוד את רמות ה‑IL‑1β. TH5487 ו‑SU0268 לא רק קיצצו שחרור IL‑1β במצבים אלה, אלא גם הפחיתו את כמות ה‑NLRP3 שנמצאה על המיטוכונדריה. מיקרוסקופיה קריואלקטרונית אישרה כי NLRP3 יכול ליצור קומפלקס טבעתי גדול שמקשר פיזית ל‑DNA מיטוכונדריאלי, ודגמי מחשב הציעו כי דומיין הפירין של החלבון מזהה DNA חד‑גדילי מחומצן דרך משטח שטחי טעון חיובי. התרופות מתערבות בשלב חישה זה של ה‑DNA, וחותכות קישור חשוב בין DNA פגום לדלקת שברחה משליטה.
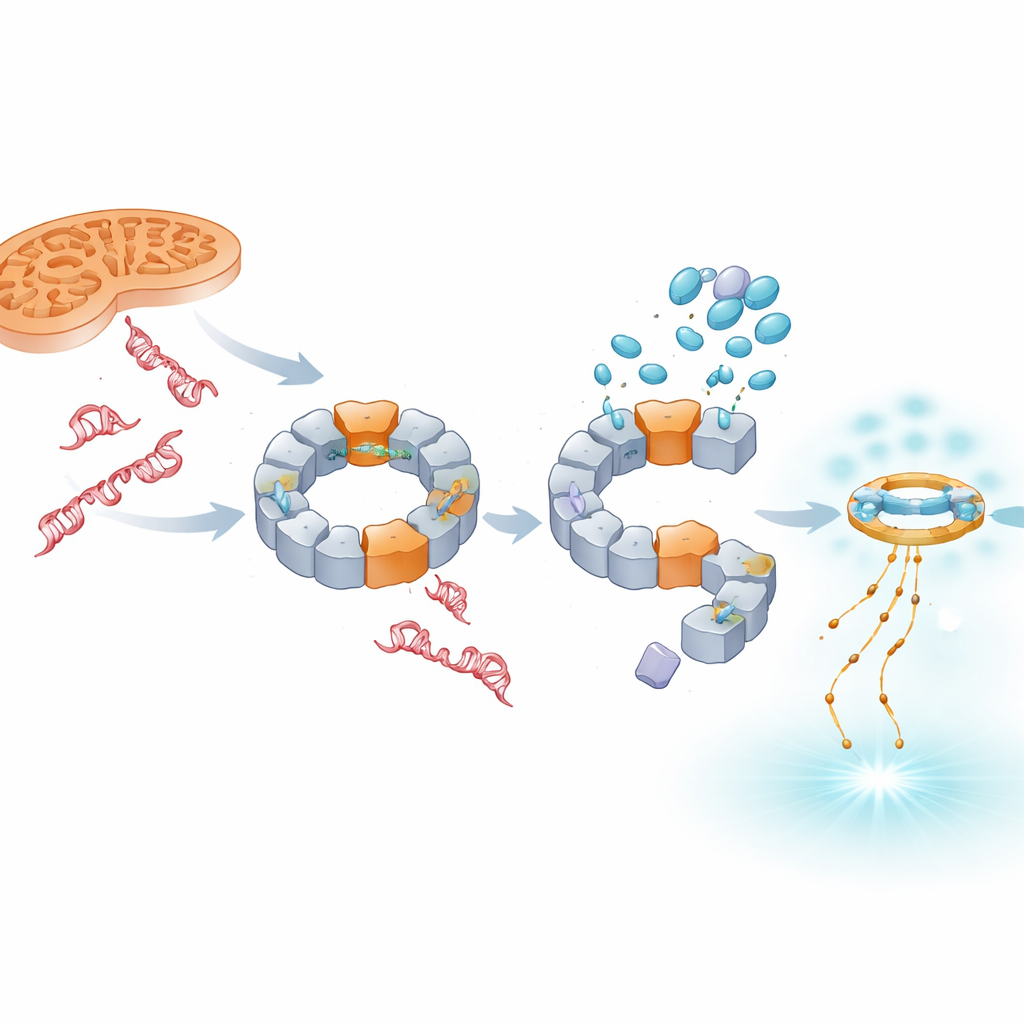
הזזת האות לעבר הגנות בסגנון אנטי‑ויראלי
חסימת NLRP3 אינה גורמת להיעלמות ה‑DNA הפגום; במקום זאת, יותר ממנו, ובמיוחד מהגרעין, מצטבר בציטוזול של התא. המחקר מראה ש‑DNA עודף זה נקלט על‑יד מערכת חישה אחרת, cGAS–STING, שמגיבה בדרך כלל לגנומי וירוסים. כאשר TH5487, SU0268 או TH10785 נוכחים, רמות ה‑STING המופעל ו‑IFN‑β האנטי‑ויראלי עולות גם בתאי מודל וגם בתאי דם ראשוניים של בני אדם. חשוב לציין שהעלייה הזו מתרחשת גם כאשר NLRP3 מוסר גנטית, מה שמצביע על כך ש‑cGAS–STING פועל כאזעקת גיבוי עצמאית. לפיכך, תרכובות אלה משקיטות את הדלקת המונעת על‑ידי IL‑1β תוך הטיית תגובת החיסון לעבר איתות מבוסס אינטרפרון שעשוי להיות מגן יותר במחלות כרוניות.
תקווה לדלקות תורשתיות קשות לטיפול
ניסוי מעניין במיוחד עסק בתסמונת אוטו‑דלקתית משפחתית הקרה (FCAS), הפרעה נדירה שבה מוטציות ב‑NLRP3 הופכות אותו לפעיל יתר ועמיד מול מעכב ניסיוני מוביל, MCC950. בתאי חיסון של עכברים ושל מטופלים אנושיים הנושאים את המוטציות הללו, MCC950 נכשל בעיכוב שחרור ה‑IL‑1β. לעומת זאת, TH5487 ו‑SU0268 הקטינו משמעותית את ההפרזה הזו במינונים ששמרו על חיוניות התאים. זה מצביע על כך שאימוץ אסטרטגיה שמכוונת למשטח החישה של DNA מחומצן ב‑NLRP3, במקום לגרעין האנזימתי היותר מסורתי שלו, עשוי לעקוף עמידות ולהציע אופציות טיפוליות חדשות לחולים שמחלותיהם כיום מוגבלות בטיפולים ממוקדים.
מה המשמעות של ממצאים אלה לטיפולים עתידיים
ללא רקע מקצועי, המסר המרכזי הוא שהחוקרים מצאו "מכבה" חדש למכונת דלקת עוצמתית בתוך תאים שלנו. על‑ידי שימוש מחדש בתרופות לתיקון DNA כדי לחסום את אופן חישת ה‑NLRP3 ל‑DNA מיטוכונדריאלי וגרעיני פגום, הם יכולים להמעיט מקור משמעותי של דלקת כרונית ובאותו הזמן לאפשר לציר אחר להיכנס ולייצר אותות אינטרפרון אנטי‑ויראליים. אם אסטרטגיה זו תימצא בטוחה במחקרים הבאים, היא עשויה לפתוח טיפולים ממוקדים לא רק לסינדרומי חום תורשתיים נדירים כמו FCAS, אלא גם למצבים רחבים יותר של "דלקת‑הזדקנות" שבהם דלקת ממושכת וברמה נמוכה מזינה מחלות.
ציטוט: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
מילות מפתח: אינפלמזום NLRP3, DNA מיטוכונדריאלי מחומצן, TH5487, ציר cGAS‑STING, מחלות אוטו‑דלקתיות