Clear Sky Science · nl
TH5487 richt zich specifiek op NLRP3 bij FCAS-patiënten die resistent zijn tegen MCC950
Waarom het dempen van uit de hand lopende ontsteking belangrijk is
Veel chronische aandoeningen, van zeldzame koortssyndromen tot leeftijdsgebonden ziekten, worden aangedreven door een immuunsignaleringssysteem dat weigert uit te schakelen. Deze studie onderzoekt nieuwe kandidaat-geneesmiddelen die één van de krachtigste ontstekingsschakelaars van het lichaam, NLRP3, kunnen kalmeren zonder onze verdediging volledig uit te schakelen. Door bestaande moleculen, oorspronkelijk ontwikkeld voor DNA-reparatie, opnieuw te bekijken, ontdekken de auteurs een nieuwe manier om schadelijke ontsteking te beteugelen en deze zelfs om te buigen naar een meer beschermende antivirale respons.
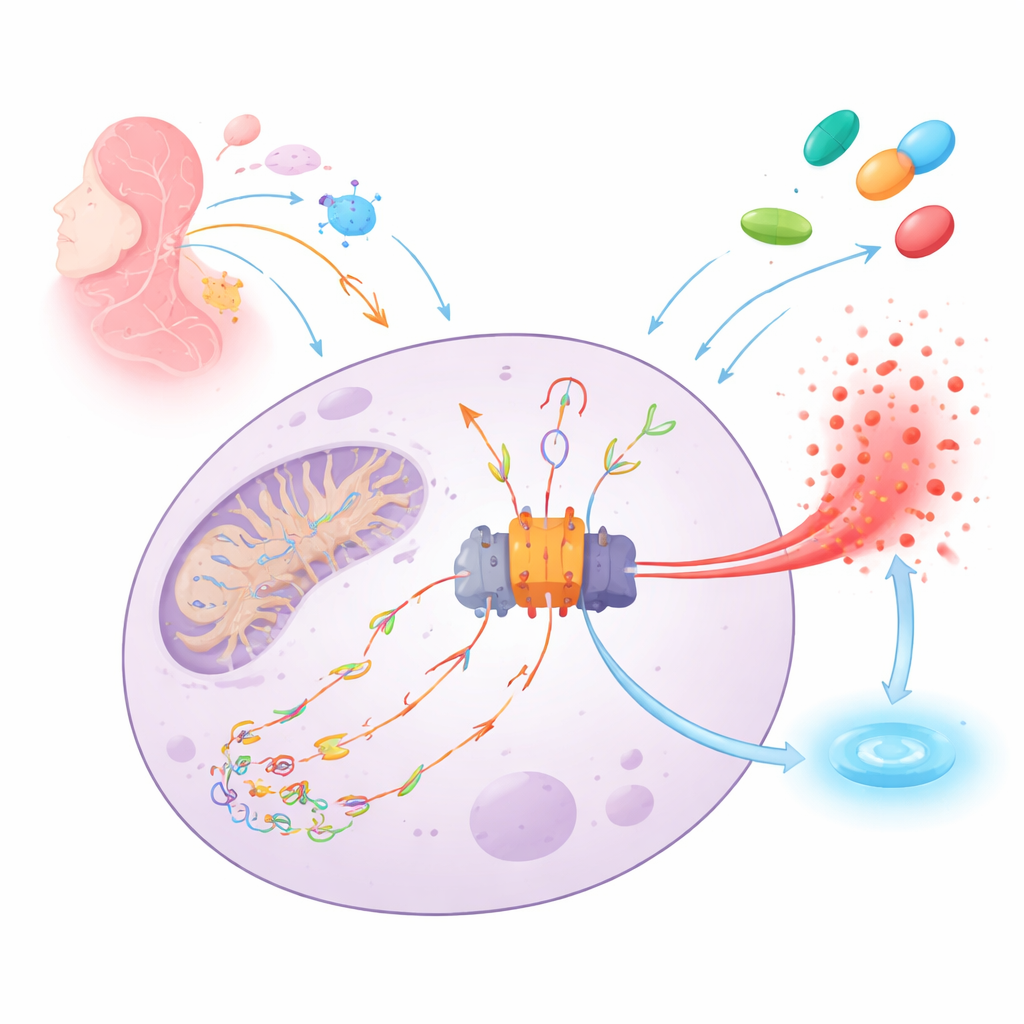
Het brandalarm van het lichaam en de vonk
NLRP3 werkt als een moleculaire rookmelder binnen immuuncellen. Wanneer het gevaar detecteert—variërend van infecties tot weefselschade—bouwt het een groot eiwitcomplex (het inflammasoom) op dat de afgifte van het sterke alarmsignaal IL‑1β activeert en de cel kan laten barsten om de buren te waarschuwen. Een belangrijke vonk voor dit alarm is beschadigd mitochondriaal DNA dat is geknipt en geoxideerd door reactieve zuurstofsoorten. Deze beschadigde DNA-fragmenten kunnen uit mitochondriën lekken, door de cel zweven, binden aan NLRP3 en de assemblage van het inflammasoom en inflammatoire celdood aandrijven.
Oude DNA-reparatiegeneesmiddelen, nieuwe ontstekingsremmende rollen
De auteurs onderzochten kleine moleculen die oorspronkelijk zijn ontworpen om een DNA-reparatie-enzym, hOGG1, aan te pakken, dat geoxideerde basen uit DNA verwijdert. Verrassend genoeg interageren deze middelen—TH5487, SU0268 en een activator genaamd TH10785—ook met NLRP3. In menselijke bloedimmuuncellen en modelcellijnen verminderden lage micromolaire doses TH5487 en SU0268 sterk de afgifte van IL‑1β en de activatie van caspase‑1, het enzym dat deze cytokine rijpt. Gedetailleerde eiwit pull‑down- en beeldvormingsexperimenten toonden aan dat de middelen voorkomen dat NLRP3 zijn volledige inflammasoomcomplex assembleert: ze blokkeren de rekrutering van sleutelpartners (ASC, NEK7 en pro‑caspase‑1) en verminderen de vorming van de heldere “specks” die een actief inflammasoom markeren.
De schakel tussen beschadigd DNA en het inflammasoom doorsnijden
Aangezien mitochondriale schade een belangrijke aanjager is van NLRP3-activiteit, testte het team of de middelen inflammasoomactivatie veroorzaakt door mitochondriale stress konden blokkeren. Een verbinding die de energiecentrales van de cel verstoort en reactieve zuurstofsoorten verhoogt, stuurt normaal gesproken geoxideerd mitochondriaal DNA naar NLRP3 en verhoogt sterk de IL‑1β-niveaus. TH5487 en SU0268 verlaagden niet alleen de IL‑1β-afgifte onder deze omstandigheden, maar verminderden ook de hoeveelheid NLRP3 die bij mitochondriën werd gevonden. Cryo-elektronenmicroscopie bevestigde dat NLRP3 een groot ringachtig complex kan vormen dat fysiek bindt aan mitochondriaal DNA, en computermodellering suggereerde dat het pyrinedomein van het eiwit geoxideerd enkelstrengs DNA herkent via een positief geladen oppervlaktepatch. De middelen treden in op deze DNA‑detectiestap en verbreken zo een cruciale verbinding tussen beschadigd DNA en uit de hand lopende ontsteking.
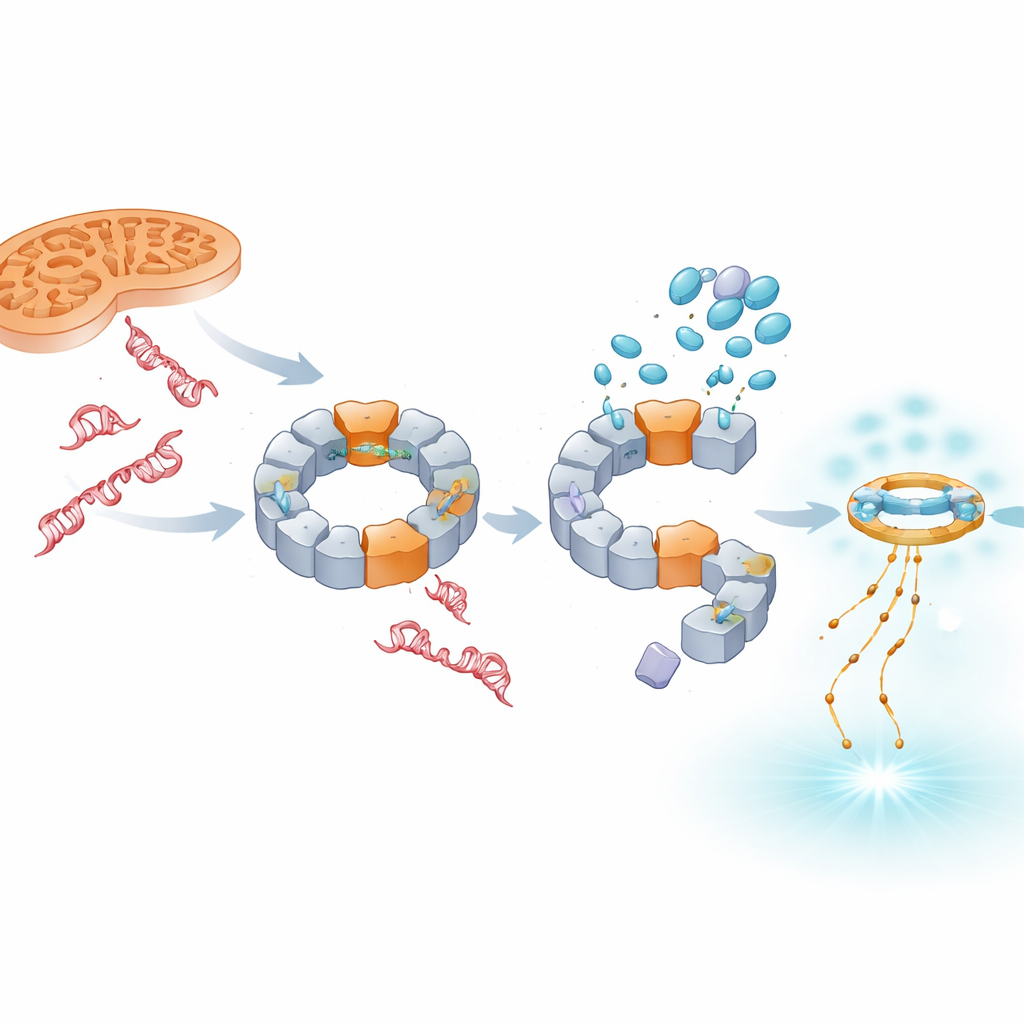
Het signaal verschuiven naar antivirale verdedigingsmechanismen
Het blokkeren van NLRP3 laat beschadigd DNA niet verdwijnen; in plaats daarvan hoopt meer ervan, met name uit de kern, zich op in het cellulaire cytosol. De studie toont aan dat dit overtollige DNA wordt opgepikt door een ander sensorsysteem, cGAS–STING, dat gewoonlijk reageert op viraal genoommateriaal. Wanneer TH5487, SU0268 of TH10785 aanwezig zijn, stijgen de niveaus van geactiveerde STING en de antivirale boodschapper IFN‑β in zowel modelcellen als primaire menselijke bloedcellen. Belangrijk is dat deze toename ook optreedt wanneer NLRP3 genetisch is verwijderd, wat aangeeft dat cGAS–STING als een onafhankelijke back-upalarmfunctie werkt. Zo dempen deze verbindingen IL‑1β‑gedreven ontsteking terwijl ze de immuunrespons kantelen naar interferon‑gebaseerde signalering die in chronische ziekte mogelijk beschermender is.
Belofte voor moeilijk te behandelen erfelijke ontstekingen
Een bijzonder opvallende test betrof Familial Cold Autoinflammatory Syndrome (FCAS), een zeldzame aandoening waarbij mutaties in NLRP3 het hyperactief maken en resistent tegen een toonaangevende experimentele remmer, MCC950. In immuuncellen van muizen en menselijke patiënten met deze mutaties faalde MCC950 in het verminderen van IL‑1β-afgifte. TH5487 en SU0268 verminderden deze overproductie daarentegen aanzienlijk bij concentraties die de celviabiliteit spaarden. Dit suggereert dat het richten op het geoxideerde DNA‑herkenningsoppervlak van NLRP3, in plaats van op de meer traditionele enzymatische kern, resistentie kan omzeilen en nieuwe behandelingsopties kan bieden voor patiënten van wie de ziekte momenteel weinig gerichte therapieën kent.
Wat deze bevindingen betekenen voor toekomstige therapieën
Voor niet‑specialisten is de kernboodschap dat de onderzoekers een nieuwe “uit‑schakelaar” hebben gevonden voor een krachtig ontstekingsmechanisme binnen onze cellen. Door DNA-reparatiemiddelen te herbestemmen om te blokkeren hoe NLRP3 beschadigd mitochondriaal en nucleair DNA waarneemt, kunnen ze een belangrijke bron van chronische ontsteking dempen terwijl een ander pad het overneemt en antivirale interferonsignalen produceert. Als deze strategie in verdere studies veilig blijkt, zou ze gerichte behandelingen kunnen openen, niet alleen voor zeldzame erfelijke koortssyndromen zoals FCAS, maar ook voor bredere aandoeningen van “inflammaging” waarbij aanhoudende, laaggradige ontsteking ziekte aanwakkert.
Bronvermelding: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
Trefwoorden: NLRP3-inflammasoom, geoxideerd mitochondriaal DNA, TH5487, cGAS-STING-pad, autoinflammatoire ziekte