Clear Sky Science · es
TH5487 se dirige específicamente a NLRP3 en pacientes con FCAS resistentes a MCC950
Por qué importa calmar la inflamación descontrolada
Muchas enfermedades crónicas, desde fiebres raras hasta trastornos relacionados con la edad, están impulsadas por un sistema de alarma inmunitario que se niega a apagarse. Este estudio explora nuevos candidatos farmacológicos que pueden silenciar uno de los interruptores inflamatorios más potentes del cuerpo, llamado NLRP3, sin desactivar por completo nuestras defensas. Al replantear moléculas existentes originalmente dirigidas a la reparación del ADN, los autores descubren una nueva forma de contener la inflamación perjudicial e incluso reconducirla hacia una respuesta más protectora de tipo antiviral.
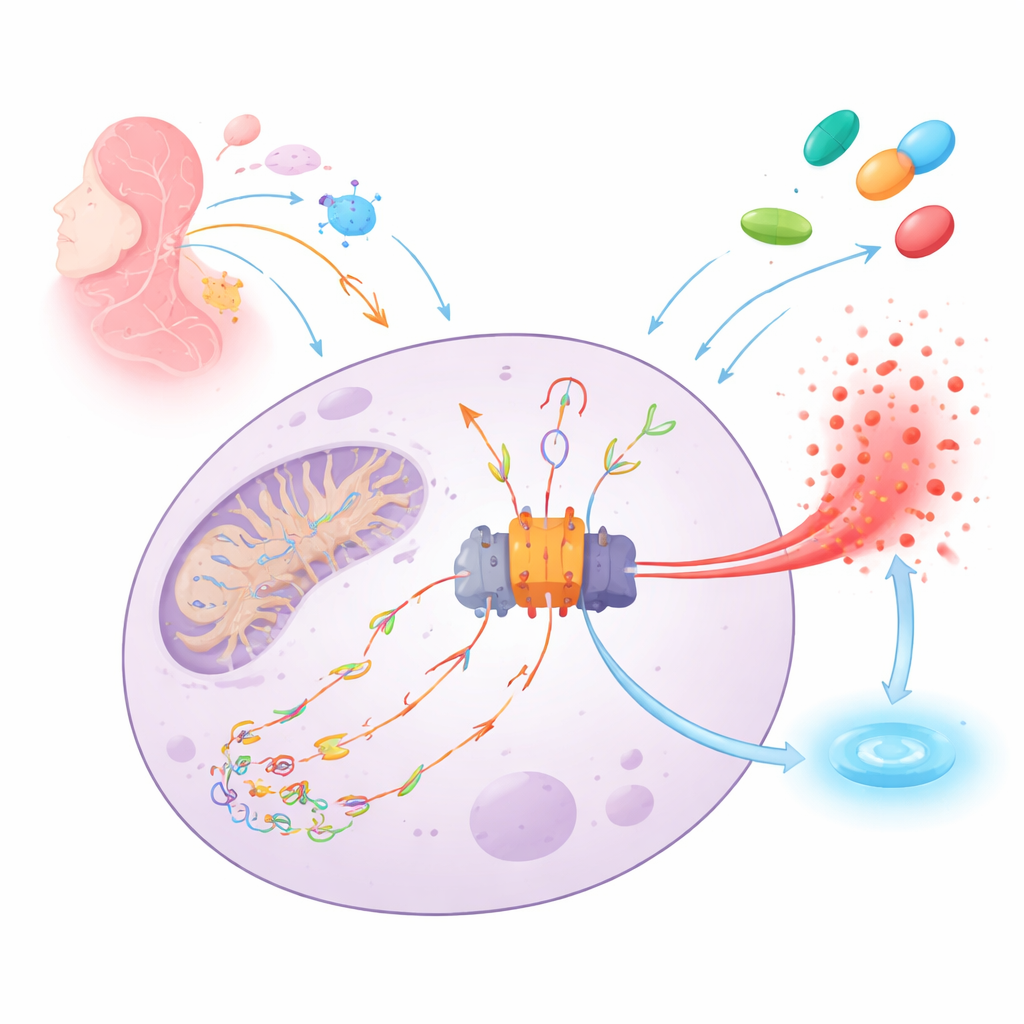
La alarma de incendios del cuerpo y su chispa
NLRP3 actúa como un detector de humo molecular dentro de las células inmunitarias. Cuando detecta peligro —que va desde infecciones hasta daño tisular— se ensambla en una gran máquina proteica (el inflammasoma) que desencadena la liberación de la potente señal de alarma IL‑1β y puede hacer que la célula se rompa para avisar a sus vecinas. Una chispa clave para esta alarma es el ADN mitocondrial dañado que ha sido mellado y oxidado por especies reactivas de oxígeno. Estos fragmentos de ADN dañados pueden filtrarse desde las mitocondrias, desplazarse por la célula, unirse a NLRP3 e inducir el ensamblaje del inflammasoma y la muerte inflamatoria celular.
Antiguos fármacos de reparación del ADN, nuevos papeles antiinflamatorios
Los autores examinaron pequeñas moléculas diseñadas inicialmente para dirigirse a una enzima de reparación del ADN llamada hOGG1, que elimina bases oxidada del ADN. Sorprendentemente, estos fármacos —TH5487, SU0268 y un activador llamado TH10785— también interactúan con NLRP3. En células inmunitarias de sangre humana y en líneas celulares modelo, dosis bajas en micromolar de TH5487 y SU0268 redujeron de forma pronunciada la liberación de IL‑1β y la activación de la caspasa‑1, la enzima que madura esta citocina. Experimentos detallados de captura proteica e imagen mostraron que los fármacos impiden que NLRP3 ensamble su complejo inflammasoma completo: bloquean el reclutamiento de socios clave (ASC, NEK7 y pro‑caspasa‑1) y reducen la formación de los brillantes “puntos” que marcan un inflammasoma activo.
Romper el vínculo entre el ADN dañado y el inflammasoma
Puesto que el daño mitocondrial es un impulsor importante de la actividad de NLRP3, el equipo probó si los fármacos podían bloquear la activación del inflammasoma desencadenada por estrés mitocondrial. Un compuesto que perturba las fábricas de energía celular y aumenta las especies reactivas de oxígeno normalmente dirige ADN mitocondrial oxidado hacia NLRP3 y eleva fuertemente los niveles de IL‑1β. TH5487 y SU0268 no solo redujeron la liberación de IL‑1β en estas condiciones, sino que también disminuyeron la cantidad de NLRP3 encontrada en las mitocondrias. La criomicroscopía electrónica confirmó que NLRP3 puede formar un amplio complejo en forma de anillo que se une físicamente al ADN mitocondrial, y el modelado por ordenador sugirió que el dominio pirina de la proteína reconoce ADN monocatenario oxidado mediante un parche superficial cargado positivamente. Los fármacos interfieren con este paso de detección del ADN, cortando un vínculo crucial entre el ADN dañado y la inflamación descontrolada.
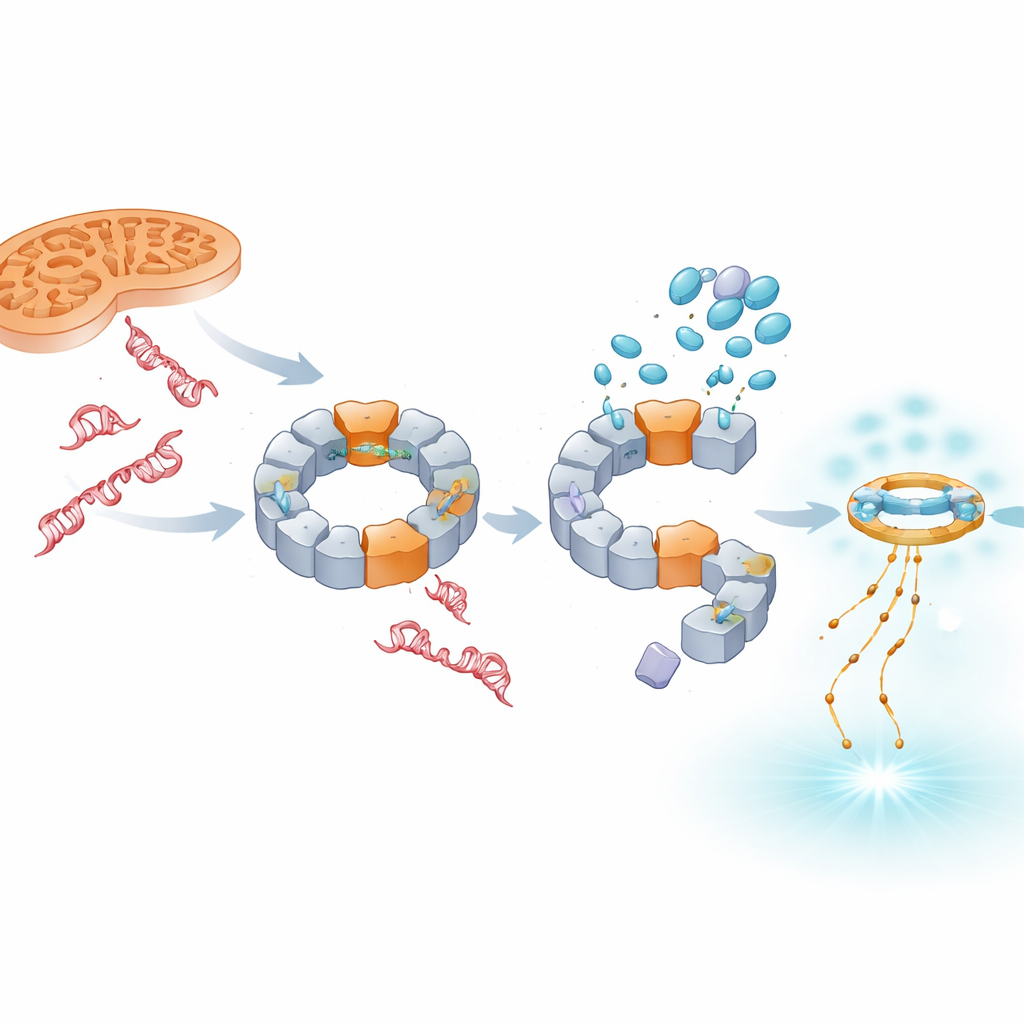
Desplazar la señal hacia defensas de tipo antiviral
Bloquear NLRP3 no hace desaparecer el ADN dañado; en su lugar, más ADN, especialmente procedente del núcleo, se acumula en el fluido celular. El estudio muestra que este exceso de ADN es detectado por otro sistema sensor, cGAS–STING, que responde típicamente a genomas virales. Cuando están presentes TH5487, SU0268 o TH10785, los niveles de STING activado y del mensajero antiviral IFN‑β aumentan tanto en células modelo como en células sanguíneas humanas primarias. Es importante que este aumento se produce incluso cuando NLRP3 se elimina genéticamente, lo que indica que cGAS–STING actúa como una alarma de respaldo independiente. Así, estos compuestos silencian la inflamación mediada por IL‑1β mientras inclinan la respuesta inmunitaria hacia la señalización por interferón, que puede ser más protectora en enfermedades crónicas.
Promesa para inflamaciones heredadas difíciles de tratar
Una prueba particularmente llamativa implicó el Síndrome Autoinflamatorio Familiar por Frío (FCAS), un trastorno raro en el que mutaciones en NLRP3 lo vuelven hiperactivo y resistente a un inhibidor experimental líder, MCC950. En células inmunitarias de ratones y pacientes humanos portadores de estas mutaciones, MCC950 no logró frenar la liberación de IL‑1β. TH5487 y SU0268, sin embargo, redujeron significativamente esta sobreproducción a dosis que respetaron la viabilidad celular. Esto sugiere que dirigirse a la superficie de NLRP3 que detecta ADN oxidado, en lugar de su núcleo enzimático más tradicional, puede sortear la resistencia y ofrecer nuevas opciones terapéuticas para pacientes cuya enfermedad actualmente dispone de terapias dirigidas limitadas.
Qué significan estos hallazgos para futuras terapias
Para un no especialista, el mensaje central es que los investigadores han encontrado un nuevo “interruptor de apagado” para una potente máquina inflamatoria dentro de nuestras células. Al reutilizar fármacos de reparación del ADN para bloquear cómo NLRP3 detecta ADN mitocondrial y nuclear dañado, pueden atenuar una fuente importante de inflamación crónica al tiempo que permiten que otra vía asuma el control y produzca señales interferón antivirales. Si esta estrategia resulta segura en estudios posteriores, podría abrir tratamientos dirigidos no solo para síndromes febriles hereditarios raros como FCAS, sino también para condiciones más amplias de “inflammaging” en las que la inflamación persistente y de bajo grado alimenta la enfermedad.
Cita: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
Palabras clave: inflammasoma NLRP3, ADN mitocondrial oxidado, TH5487, vía cGAS-STING, enfermedad autoinflamatoria