Clear Sky Science · tr
TH5487, MCC950’ye dirençli FCAS hastalarında özel olarak NLRP3’ü hedefliyor
Kontrolsüz inflamasyonun yatıştırılması neden önemli
Nadir ateş hastalıklarından yaşa bağlı bozukluklara kadar birçok kronik hastalık, kapanmayan bir bağışıklık alarm sisteminden kaynaklanır. Bu çalışma, vücudun en güçlü iltihap anahtarlarından biri olan NLRP3’ü savunmalarımızı tamamen kapatmadan sakinleştirebilecek yeni ilaç adaylarını araştırıyor. DNA onarımını hedefleyen mevcut molekülleri yeniden değerlendirerek, yazarlar zararlı inflamasyonu dizginlemenin ve hatta onu daha koruyucu antiviral tarzı bir yanıt haline yönlendirmenin yeni bir yolunu ortaya koyuyor.
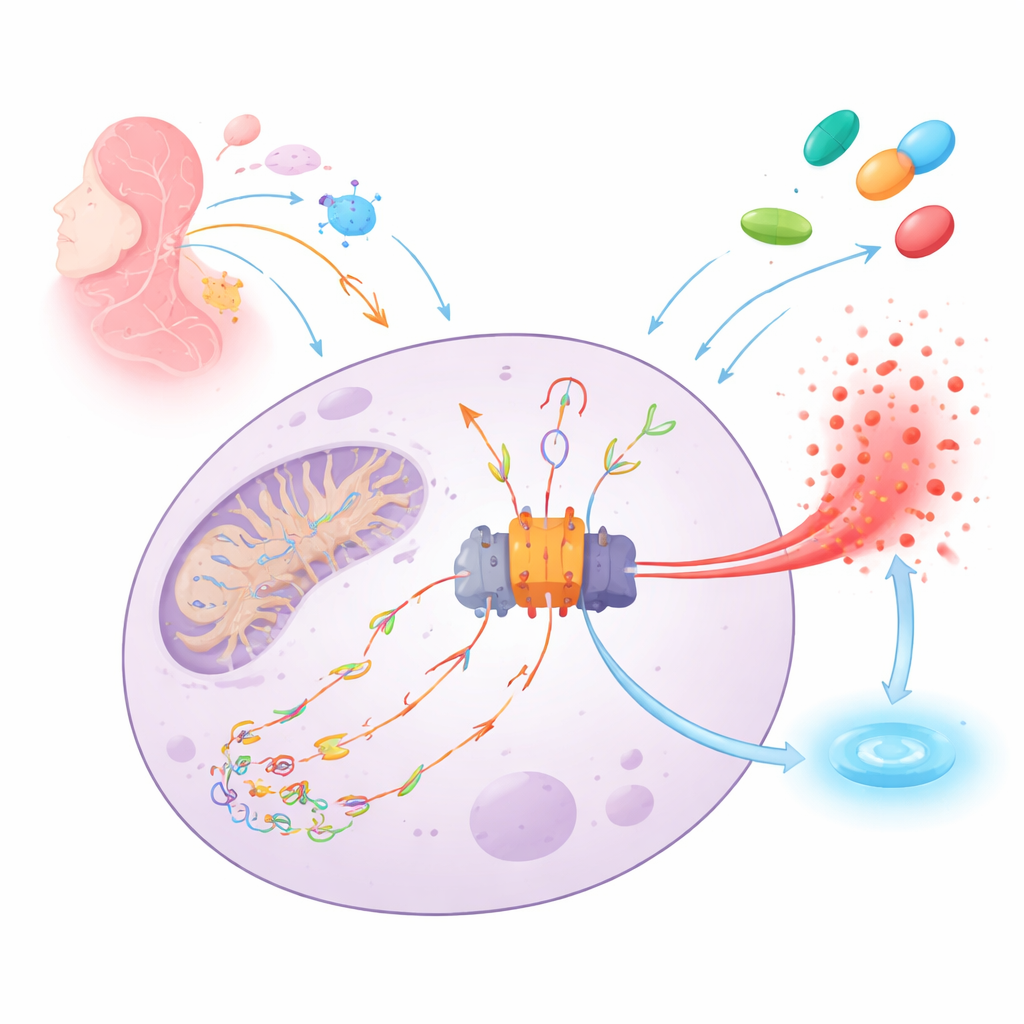
Vücudun yangın alarmı ve kıvılcımı
NLRP3, bağışıklık hücreleri içinde moleküler bir duman dedektörü gibi davranır. Enfeksiyonlardan doku hasarına kadar tehlike algıladığında, güçlü alarm sinyali IL‑1β’nin salınımını tetikleyen ve komşularını uyarmak için hücrenin parçalanmasına yol açabilen büyük bir protein makinası (inflammasom) kurar. Bu alarm için önemli bir kıvılcım, reaktif oksijen türleri tarafından kesilmiş ve oksitlenmiş mitokondriyal DNA’dır. Hasarlı DNA parçacıkları mitokondrilerden sızabilir, hücre içinde dolaşabilir, NLRP3’e bağlanabilir ve inflammasom montajını ve inflamatuvar hücre ölümünü tetikleyebilir.
Eski DNA onarım ilaçları, yeni anti‑inflamatuar roller
Yazarlar, oksitlenmiş bazları DNA’dan çıkaran bir DNA onarım enzimi olan hOGG1’i hedeflemek üzere tasarlanmış küçük molekülleri incelediler. İlginç bir şekilde bu ilaçlar — TH5487, SU0268 ve bir aktivatör olan TH10785 — aynı zamanda NLRP3 ile etkileşiyor. İnsan kanı kaynaklı bağışıklık hücrelerinde ve model hücre hatlarında, düşük mikromol düzeylerindeki TH5487 ve SU0268 IL‑1β salınımını ve bu sitokini olgunlaştıran enzim olan kaspaz‑1 aktivasyonunu keskin biçimde azalttı. Ayrıntılı protein çekme ve görüntüleme deneyleri, ilaçların NLRP3’ün tam inflammasom kompleksini kurmasını engellediğini gösterdi: ana ortakların (ASC, NEK7 ve pro‑kaspaz‑1) toplanmasını bloke ediyor ve aktif inflammasomu işaretleyen parlak “speck”lerin oluşumunu azaltıyordu.
Hasarlı DNA ile inflammasom arasındaki bağı kesmek
Mitokondri hasarı NLRP3 aktivitesinin ana tetikleyicilerinden biri olduğu için ekip, ilaçların mitokondriyal stresle tetiklenen inflammasom aktivasyonunu bloke edip edemeyeceğini test etti. Hücrenin enerji fabrikalarını bozup reaktif oksijen türlerini artıran bir bileşik normalde oksitlenmiş mitokondriyal DNA’yı NLRP3’e yönlendirir ve IL‑1β seviyelerini güçlü şekilde yükseltir. TH5487 ve SU0268 bu koşullar altında yalnızca IL‑1β salınımını azaltmakla kalmadı, aynı zamanda mitokondrilerde bulunan NLRP3 miktarını da düşürdü. Kriyomikro‑elektron mikroskobu, NLRP3’ün mitokondriyal DNA ile fiziksel olarak bağlanabilen büyük halka benzeri bir kompleks oluşturabileceğini doğruladı ve bilgisayar modellemeleri proteinin pirin (pyrin) bölgesinin pozitif yüklü bir yüzey yamacıyla oksitlenmiş tek zincirli DNA’yı tanıyabileceğini öne sürdü. İlaçlar bu DNA algılama basamağına müdahale ederek hasarlı DNA ile kontrolden çıkmış inflamasyon arasındaki hayati bağı koparıyor.
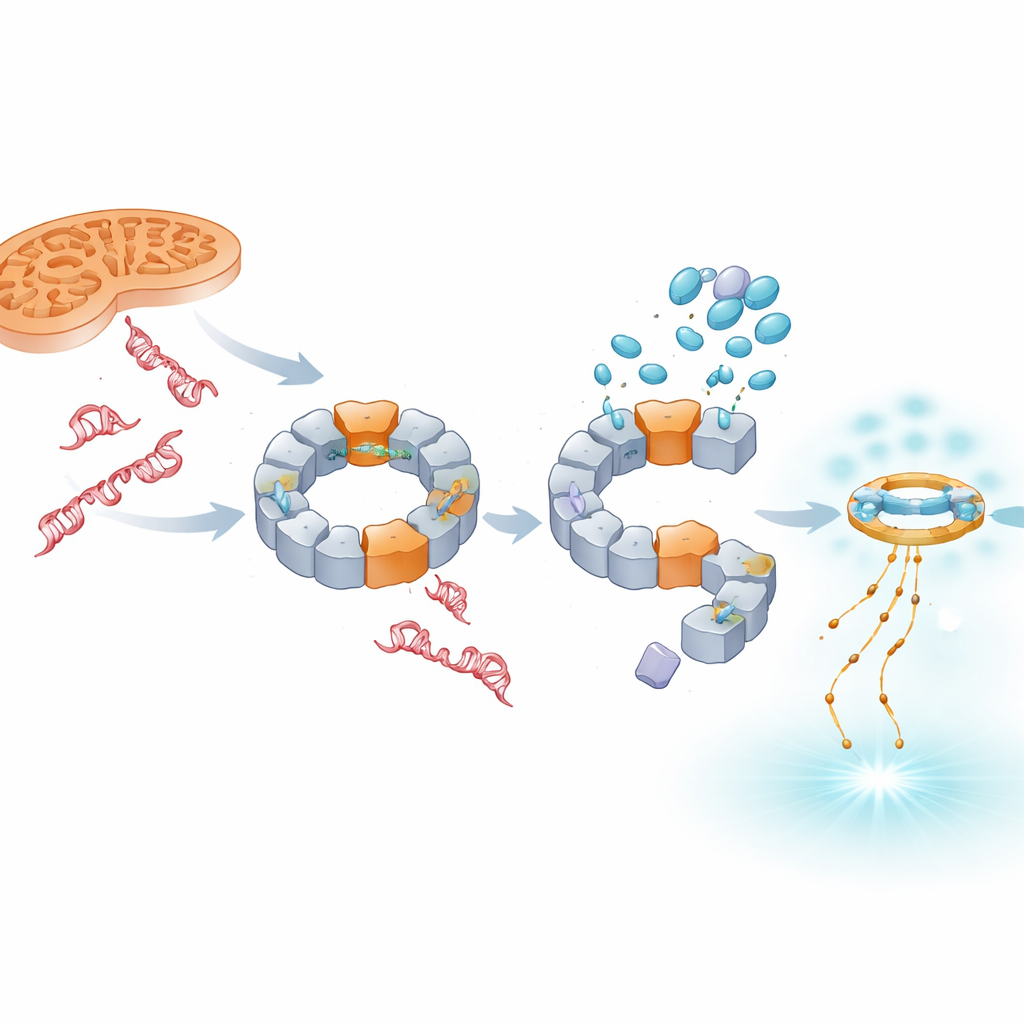
Sinyali antiviral tarzı savunmalara kaydırmak
NLRP3’ü bloke etmek hasarlı DNA’yı yok etmez; bunun yerine özellikle çekirdekten gelen daha fazla DNA hücre sıvısında birikir. Çalışma, bu fazla DNA’nın tipik olarak viral genomlara yanıt veren başka bir algılayıcı sistem olan cGAS–STING tarafından algılandığını gösteriyor. TH5487, SU0268 veya TH10785 bulunduğunda aktive STING ve antiviral haberci IFN‑β düzeyleri hem model hücrelerde hem de primer insan kan hücrelerinde artıyor. Önemli olarak, bu artış NLRP3 genetik olarak yok edildiğinde bile ortaya çıkıyor; bu da cGAS–STING’in bağımsız bir yedek alarm olarak işlev gördüğünü gösteriyor. Böylece bu bileşikler IL‑1β kaynaklı inflamasyonu yatıştırırken bağışıklık yanıtını kronik hastalıkta daha koruyucu olabilecek interferon‑temelli sinyallemeye doğru kaydırıyor.
Tedavi edilmesi zor kalıtsal inflamasyon için umut
Özellikle çarpıcı bir test, NLRP3’teki mutasyonların onu aşırı aktif hale getirdiği ve önde gelen deneysel bir inhibitör olan MCC950’ye dirençli olduğu Familial Cold Autoinflammatory Syndrome (FCAS) idi. Bu mutasyonları taşıyan fare ve insan hastalardan alınan immün hücrelerde MCC950 IL‑1β salınımını kontrol altına alamadı. Ancak TH5487 ve SU0268, hücre canlılığını koruyan dozlarda bu aşırı üretimi anlamlı şekilde azalttı. Bu durum, NLRP3’ün daha geleneksel enzimatik çekirdeği yerine oksitlenmiş DNA’yı algılayan yüzeyini hedeflemenin direnci aşabileceğini ve hastalığın şu an sınırlı hedefe yönelik tedavisi olan hastalar için yeni tedavi seçenekleri sunabileceğini düşündürüyor.
Bu bulgular gelecekteki terapiler için ne anlama geliyor
Uzman olmayan bir okur için temel mesaj, araştırmacıların hücrelerimizdeki güçlü bir inflamatuar makine için yeni bir “kapatma düğmesi” bulmuş olmalarıdır. DNA onarım ilaçlarını yeniden amaçlayarak NLRP3’ün mitokondriyal ve nükleer hasarlı DNA’yı nasıl algıladığını bloke edebiliyorlar; böylece kronik inflamasyonun önemli bir kaynağını azaltırken başka bir yolun devreye girip antiviral interferon sinyalleri üretmesine izin veriyorlar. Bu strateji daha ileri çalışmalarda güvenli bulunursa, yalnızca FCAS gibi nadir kalıtsal ateş sendromları için değil, aynı zamanda sürekli düşük dereceli inflamasyonun hastalığı körüklediği daha geniş “inflammazing” durumlar için de hedefe yönelik tedavilerin yolunu açabilir.
Atıf: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
Anahtar kelimeler: NLRP3 inflammasomu, okside mitokondriyal DNA, TH5487, cGAS‑STING yolu, otoenflamatuar hastalık