Clear Sky Science · pt
TH5487 mira especificamente o NLRP3 em pacientes com FCAS resistentes ao MCC950
Por que acalmar a inflamação descontrolada importa
Muitas doenças crônicas, desde febres raras até transtornos relacionados à idade, são impulsionadas por um sistema de alarme imunológico que se recusa a desligar. Este estudo explora novos candidatos a fármacos que podem silenciar um dos interruptores inflamatórios mais potentes do corpo, chamado NLRP3, sem desligar totalmente nossas defesas. Ao repensar moléculas existentes originalmente direcionadas à reparação do DNA, os autores descobrem uma maneira inédita de controlar a inflamação prejudicial e até redirecioná‑la para uma resposta mais protetora no estilo antiviral.
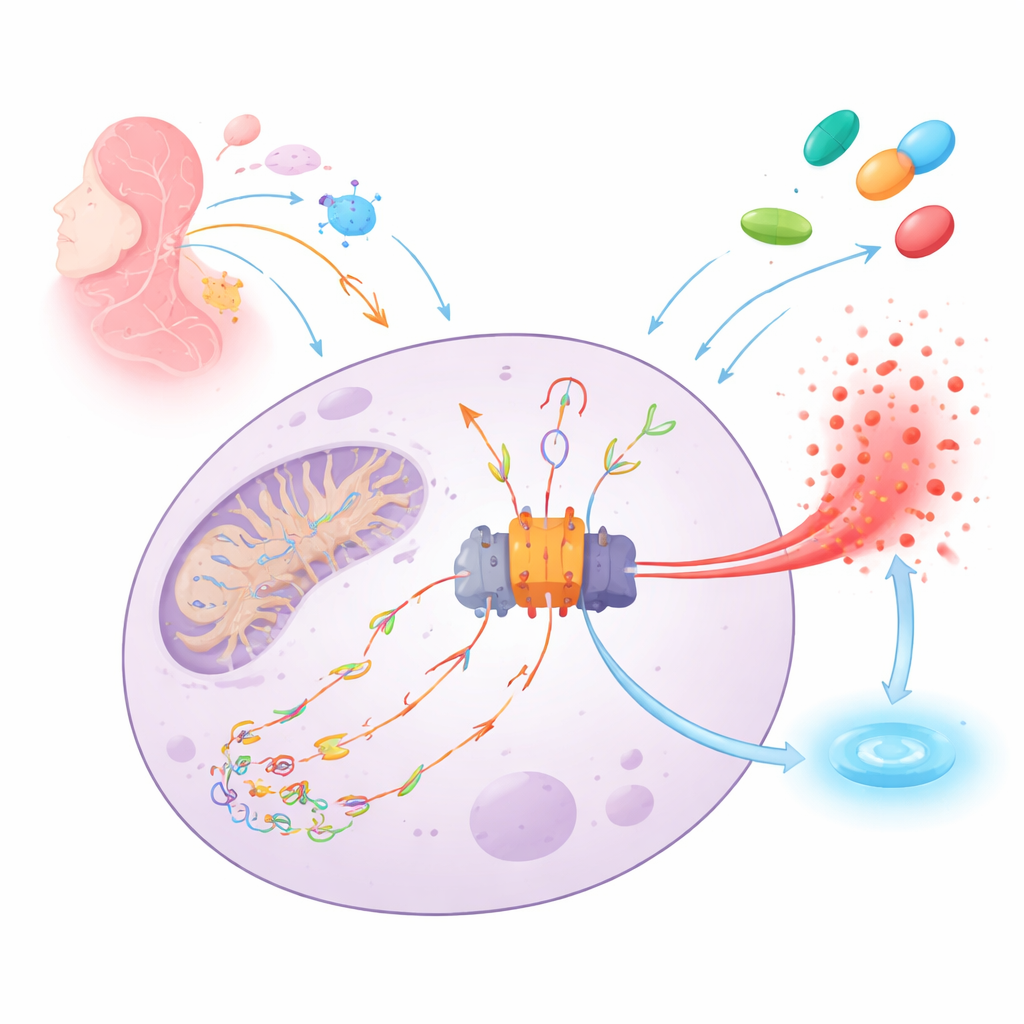
O alarme de incêndio do corpo e sua faísca
O NLRP3 funciona como um detector molecular de fumaça dentro das células imunes. Quando percebe perigo — desde infecções até danos teciduais — ele monta uma grande máquina proteica (o inflamassoma) que desencadeia a liberação do potente sinal de alarme IL‑1β e pode romper a célula para avisar as vizinhas. Uma faísca importante para esse alarme é o DNA mitocondrial danificado, que foi cortado e oxidado por espécies reativas de oxigênio. Esses fragmentos de DNA danificados podem vazar das mitocôndrias, flutuar pela célula, ligar‑se ao NLRP3 e impulsionar a montagem do inflamassoma e a morte celular inflamatória.
Antigos fármacos de reparo do DNA, novos papéis antiinflamatórios
Os autores examinaram pequenas moléculas originalmente concebidas para atingir uma enzima de reparo de DNA chamada hOGG1, que remove bases oxidada do DNA. Surpreendentemente, esses fármacos — TH5487, SU0268 e um ativador chamado TH10785 — também interagem com o NLRP3. Em células imunes do sangue humano e em linhas celulares modelo, doses micromolares baixas de TH5487 e SU0268 reduziram drasticamente a liberação de IL‑1β e a ativação da caspase‑1, a enzima que maturiza essa citocina. Experimentos detalhados de pull‑down proteico e imagens mostraram que os fármacos impedem o NLRP3 de montar seu complexo inflamassoma completo: eles bloqueiam o recrutamento de parceiros-chave (ASC, NEK7 e pro‑caspase‑1) e reduzem a formação dos brilhantes “specks” que marcam um inflamassoma ativo.
Cortando a ligação entre DNA danificado e o inflamassoma
Como o dano mitocondrial é um motor importante da atividade do NLRP3, a equipe testou se os fármacos podiam bloquear a ativação do inflamassoma desencadeada pelo estresse mitocondrial. Um composto que perturba as usinas de energia da célula e aumenta as espécies reativas normalmente direciona DNA mitocondrial oxidado ao NLRP3 e eleva fortemente os níveis de IL‑1β. TH5487 e SU0268 não apenas reduziram a liberação de IL‑1β nessas condições, como também diminuíram a quantidade de NLRP3 encontrada nas mitocôndrias. Microscopia crioeletrônica confirmou que o NLRP3 pode formar um grande complexo em forma de anel que se liga fisicamente ao DNA mitocondrial, e modelagem computacional sugeriu que o domínio pirina da proteína reconhece DNA de fita simples oxidado por meio de uma superfície carregada positivamente. Os fármacos interferem nesse passo de detecção do DNA, rompendo um elo crucial entre DNA danificado e inflamação descontrolada.
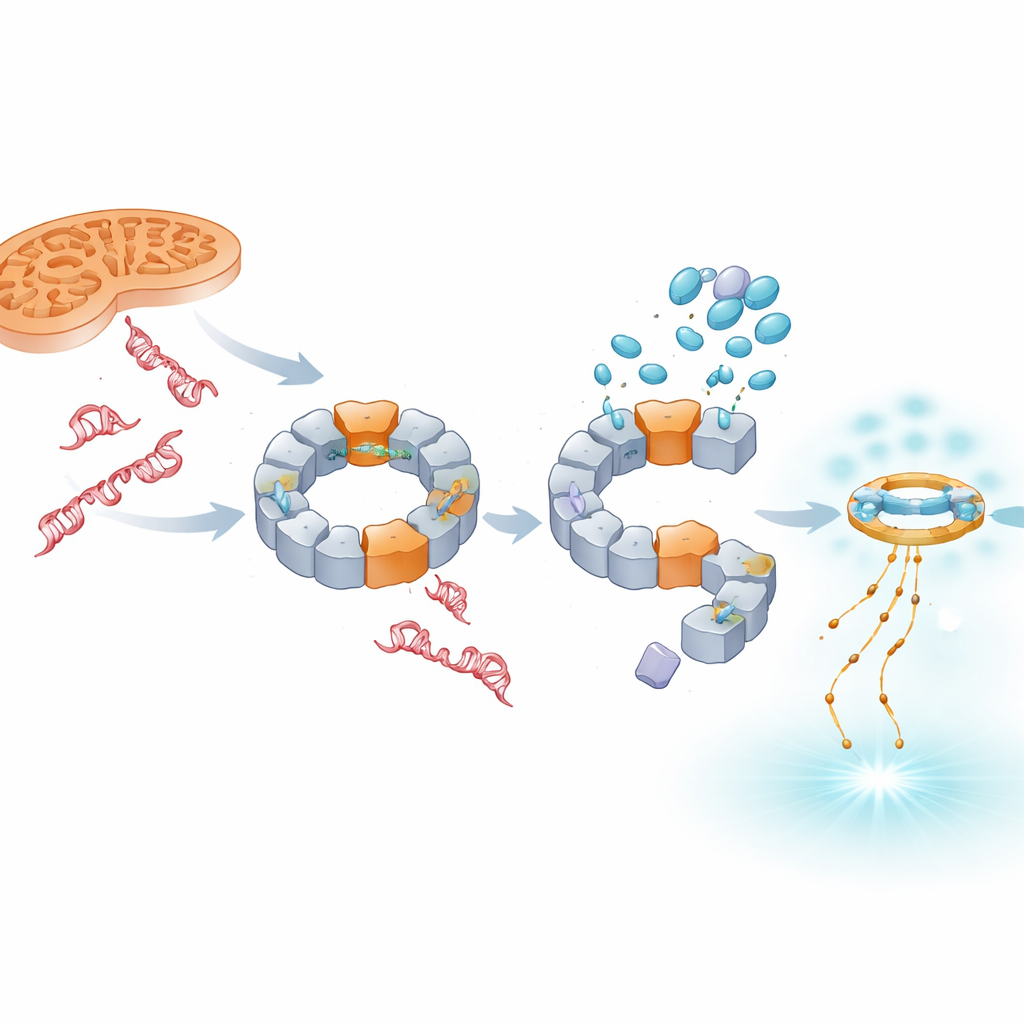
Redirecionando o sinal para defesas no estilo antiviral
Bloquear o NLRP3 não faz o DNA danificado desaparecer; em vez disso, mais desse DNA, especialmente proveniente do núcleo, se acumula no fluido celular. O estudo mostra que esse excesso de DNA é captado por outro sistema sensor, cGAS–STING, que normalmente responde a genomas virais. Quando TH5487, SU0268 ou TH10785 estão presentes, os níveis de STING ativado e do mensageiro antiviral IFN‑β aumentam tanto em células modelo quanto em células sanguíneas humanas primárias. Importante, esse aumento ocorre mesmo quando o NLRP3 é removido geneticamente, indicando que o cGAS–STING atua como um alarme reserva independente. Assim, esses compostos silenciam a inflamação dirigida por IL‑1β enquanto inclin am a resposta imune para a sinalização por interferons, que pode ser mais protetora em doenças crônicas.
Promessa para inflamações hereditárias de difícil tratamento
Um teste particularmente marcante envolveu a Síndrome Autoinflamatória Familiar ao Frio (FCAS), um distúrbio raro em que mutações no NLRP3 o tornam hiperativo e resistente a um importante inibidor experimental, MCC950. Em células imunes de camundongos e pacientes humanos portadores dessas mutações, o MCC950 não conseguiu conter a liberação de IL‑1β. TH5487 e SU0268, entretanto, reduziram significativamente essa superprodução em doses que preservaram a viabilidade celular. Isso sugere que direcionar a superfície de detecção de DNA oxidado do NLRP3, em vez de seu núcleo enzimático mais tradicional, pode contornar a resistência e oferecer novas opções de tratamento para pacientes cuja doença atualmente tem terapias direcionadas limitadas.
O que essas descobertas significam para terapias futuras
Para um não especialista, a mensagem central é que os pesquisadores encontraram um novo “interruptor” para uma potente máquina inflamatória dentro de nossas células. Ao reutilizar fármacos de reparo do DNA para bloquear como o NLRP3 detecta DNA mitocondrial e nuclear danificado, eles conseguem atenuar uma fonte importante de inflamação crônica enquanto permitem que outra via assuma e produza sinais antivirais por interferons. Se essa estratégia se mostrar segura em estudos adicionais, ela pode abrir tratamentos direcionados não apenas para síndromes febris hereditárias raras como a FCAS, mas também para condições mais amplas de “inflammaging”, nas quais inflamação persistente e de baixo grau alimenta doenças.
Citação: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
Palavras-chave: inflamassoma NLRP3, DNA mitocondrial oxidado, TH5487, via cGAS-STING, doença autoinflamatória