Clear Sky Science · ru
TH5487 избирательно ингибирует NLRP3 у пациентов с FCAS, резистентных к MCC950
Почему важно усмирять неконтролируемое воспаление
Многие хронические заболевания — от редких лихорадочных синдромов до возрастных расстройств — вызваны системой иммунного оповещения, которая отказывается выключаться. В этом исследовании рассматриваются новые кандидатные препараты, способные подавить один из самых мощных воспалительных переключателей в организме, называемый NLRP3, не отключая при этом всю нашу защиту. Переосмыслив существующие молекулы, изначально направленные на репарацию ДНК, авторы обнаружили новый способ сдерживать вредное воспаление и даже перенаправлять его в более защитный антивирусный ответ.
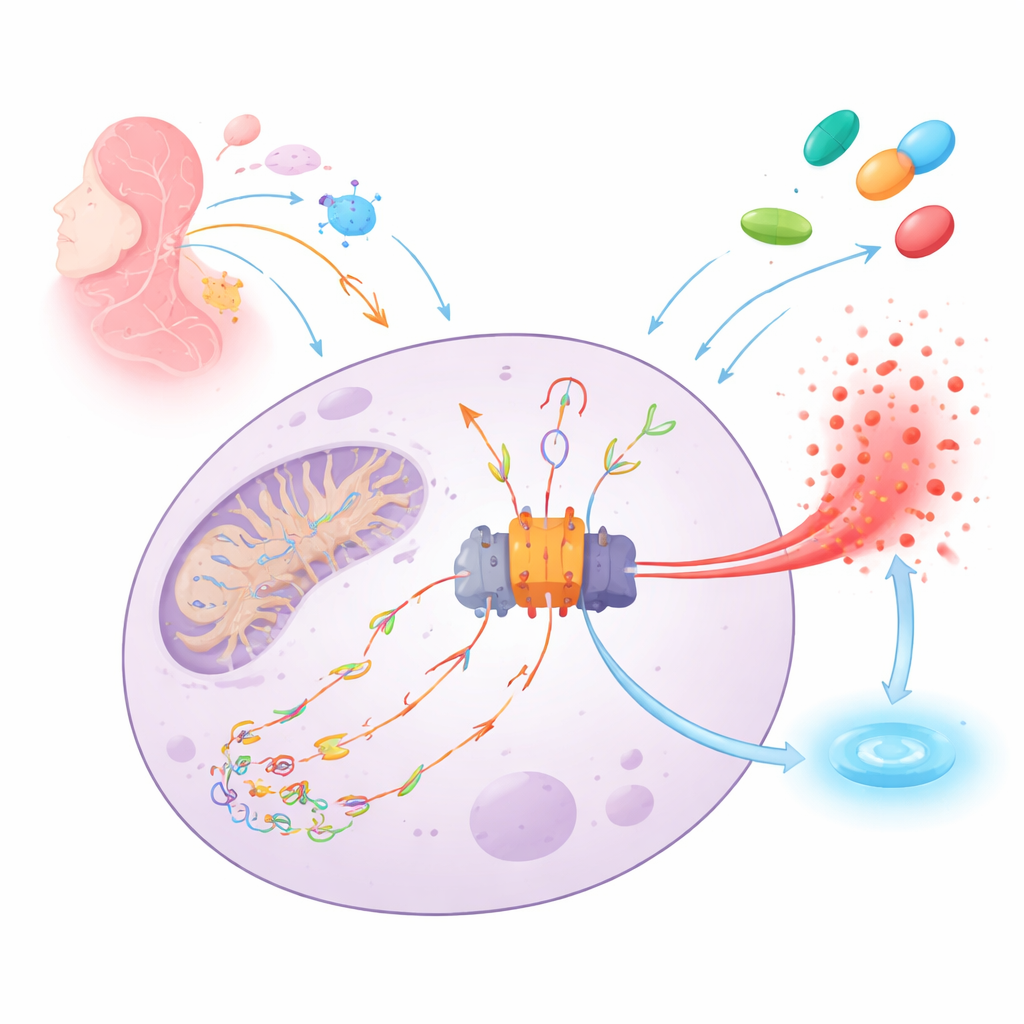
Сигнал тревоги в организме и его искра
NLRP3 действует как молекулярный дымовой детектор внутри иммунных клеток. Когда он улавливает опасность — от инфекций до повреждения тканей — он собирает большой белковый механизм (инфламмасому), который вызывает выделение мощного сигнала тревоги IL‑1β и может разрушить клетку, чтобы предупредить соседей. Важной искрой для этого сигнала является повреждённая митохондриальная ДНК, надрезанная и окислённая реактивными видами кислорода. Эти фрагменты повреждённой ДНК могут просачиваться из митохондрий, перемещаться по клетке, связываться с NLRP3 и стимулировать сборку инфламмасомы и воспалительную гибель клетки.
Старые препараты для ремонта ДНК — новые противовоспалительные роли
Авторы изучали малые молекулы, изначально разработанные для ингибирования фермента репарации ДНК hOGG1, удаляющего окисленные основания из ДНК. Удивительно, но эти препараты — TH5487, SU0268 и активатор TH10785 — также взаимодействуют с NLRP3. В иммунных клетках крови человека и модельных клеточных линиях низкие микромолярные дозы TH5487 и SU0268 значительно снижали выделение IL‑1β и активацию каспазы‑1, фермента, созревающего этот цитокин. Детальные эксперименты по аннотированию белков и визуализации показали, что препараты препятствуют полноценной сборке инфламмасомы NLRP3: они блокируют привлечение ключевых партнёров (ASC, NEK7 и про‑каспазы‑1) и уменьшают образование ярких «спеков», служащих маркером активной инфламмасомы.
Перерезание связи между повреждённой ДНК и инфламмасомой
Поскольку повреждение митохондрий является важным фактором активации NLRP3, исследователи проверили, способны ли препараты блокировать активацию инфламмасомы, вызванную митохондриальным стрессом. Соединение, нарушающее работу энергетических «фабрик» клетки и повышающее образование реактивных видов кислорода, обычно направляет окисленную митохондриальную ДНК к NLRP3 и сильно повышает уровни IL‑1β. TH5487 и SU0268 не только сокращали выделение IL‑1β в таких условиях, но и уменьшали количество NLRP3, обнаруживаемого у митохондрий. Криоэлектронная микроскопия подтвердила, что NLRP3 может формировать большой кольцеобразный комплекс, который физически связывает митохондриальную ДНК, а компьютерное моделирование предположило, что пириновый домен белка распознаёт окисленную одноцепочечную ДНК через положительно заряженную поверхностную область. Эти препараты вмешиваются в этап распознавания ДНК, разрывая ключевую связь между повреждённой ДНК и неконтролируемым воспалением.
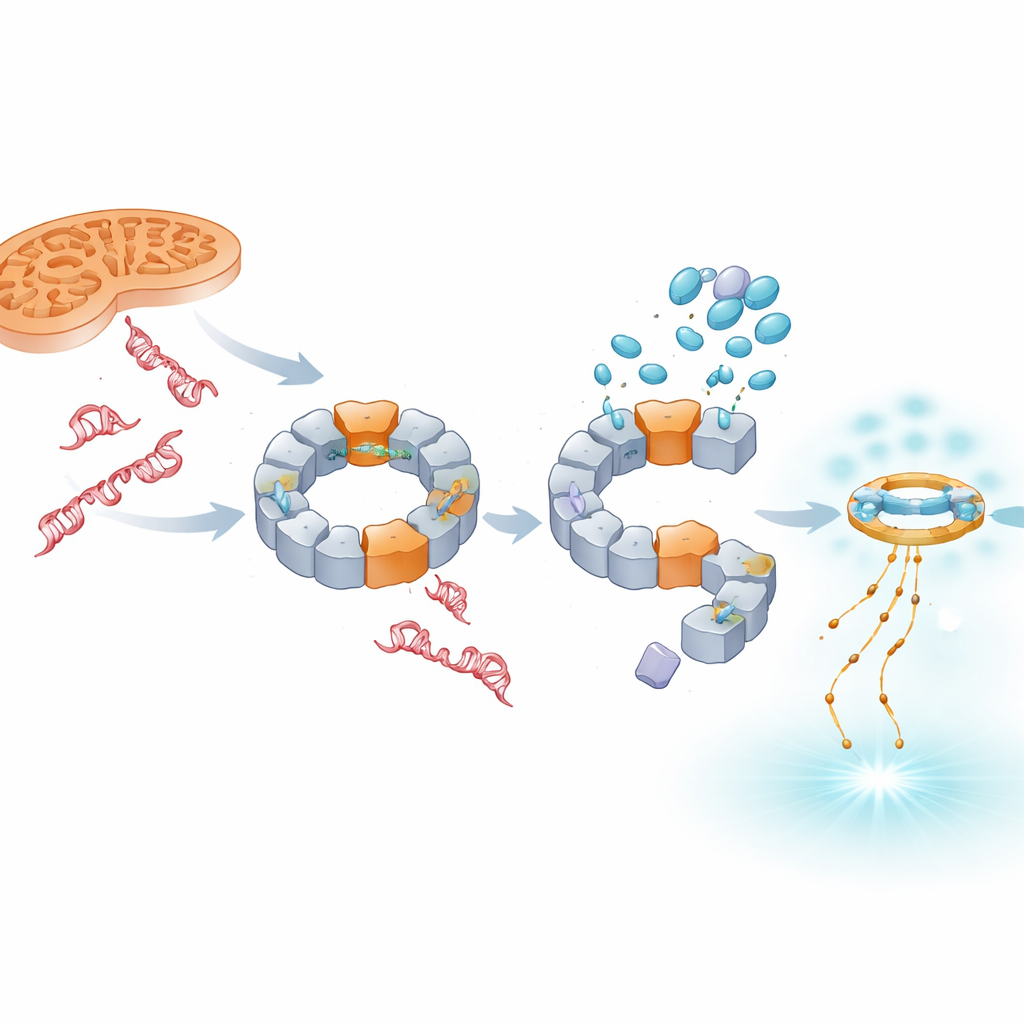
Смещение сигнала в сторону антивирусной защиты
Блокирование NLRP3 не устраняет повреждённую ДНК; напротив, её объём, особенно ядерной ДНК, увеличивается в цитозоле клетки. Исследование показывает, что эта избыточная ДНК захватывается другой сенсорной системой, cGAS–STING, которая обычно реагирует на вирусные геномы. В присутствии TH5487, SU0268 или TH10785 уровни активированного STING и антивирусного медиатора IFN‑β повышаются как в модельных клетках, так и в первичных клетках крови человека. Важно, что это усиление происходит даже при генетическом удалении NLRP3, что указывает на то, что cGAS–STING действует как независимая резервная система оповещения. Таким образом, эти соединения подавляют воспаление, вызванное IL‑1β, одновременно смещая иммунный ответ в сторону интерферон‑опосредованной сигнализации, которая может быть более защитной при хронических заболеваниях.
Перспективы при трудноизлечимом наследственном воспалении
Особенно показательным оказался тест на Семейном холодовом аутовоспалительном синдроме (FCAS) — редком расстройстве, при котором мутации в NLRP3 делают его гиперактивным и резистентным к ведущему экспериментальному ингибитору MCC950. В иммунных клетках от мышей и пациентов с этими мутациями MCC950 не смог снизить выделение IL‑1β. TH5487 и SU0268, однако, значительно уменьшали эту чрезмерную продукцию при дозах, сохранявших жизнеспособность клеток. Это указывает на то, что нацеливание на поверхность NLRP3, распознающую окисленную ДНК, а не на его традиционное каталитическое ядро, может обойти резистентность и предложить новые варианты лечения для пациентов, у которых в настоящее время ограничены таргетные терапевтические опции.
Что эти выводы значат для будущих терапий
Для неспециалиста ключевая мысль такова: исследователи обнаружили новый «выключатель» для мощного воспалительного механизма внутри наших клеток. Перепрофилируя препараты для ремонта ДНК, чтобы блокировать способ, которым NLRP3 ощущает повреждённую митохондриальную и ядерную ДНК, они могут подавить важный источник хронического воспаления, позволяя другой системе взять на себя роль и выработать антивирусные интерферон‑сигналы. Если эта стратегия подтвердит безопасность в дальнейших исследованиях, она может открыть путь к целенаправленным лечениям не только для редких наследственных лихорадочных синдромов, таких как FCAS, но и для более широких состояний «воспалительного старения» (inflammaging), при которых устойчивое низкоуровневое воспаление способствует развитию заболеваний.
Цитирование: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
Ключевые слова: инфламмасома NLRP3, окисленная митохондриальная ДНК, TH5487, путь cGAS-STING, аутовоспалительное заболевание