Clear Sky Science · ar
TH5487 يستهدف NLRP3 تحديدًا في مرضى FCAS المقاومين لـ MCC950
لماذا يهم تهدئة الالتهاب الجامح
العديد من الأمراض المزمنة، من الحُمَّى النادرة إلى اضطرابات المرتبطة بالتقدّم في السن، تُدفع بواسطة نظام إنذار مناعي يرفض الإيقاف. تستكشف هذه الدراسة مرشحات دوائية جديدة يمكنها إسكات واحد من أقوى مفاتيح الالتهاب في الجسم، المسمى NLRP3، من دون تعطيل دفاعاتنا تمامًا. عبر إعادة تفكير في جزيئات موجودة كانت مخصصة أصلاً لإصلاح الحمض النووي، يكشف المؤلفون عن طريقة جديدة لكبح الالتهاب الضار وحتى تحويله نحو استجابة أكثر وقائية على نمط مضاد للفيروسات.
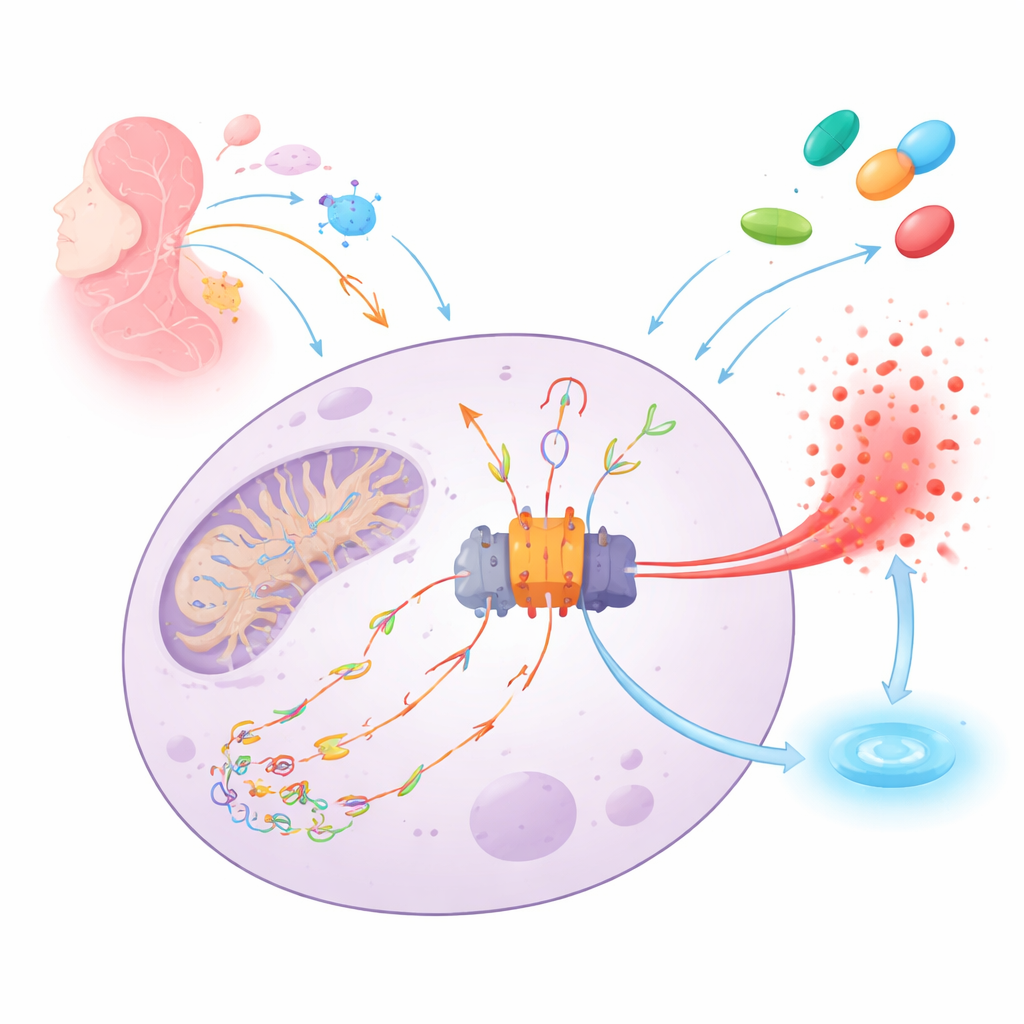
إنذار الحريق في الجسم والشرارة المسببة له
يتصرف NLRP3 مثل كاشف دخان جزيئي داخل الخلايا المناعية. عندما يستشعر الخطر — من العدوى إلى تلف الأنسجة — يجمع آلة بروتينية كبيرة (الالتهاب الجسيمي) تُطلق إشارة إنذار قوية هي IL‑1β وقد تؤدي لانفجار الخلية لتحذير الجيران. شرارة أساسية لهذا الإنذار هي الحمض النووي الميتوكوندري التالف الذي تُحدث فيه شقوق وتأكسد بواسطة أنواع أكسجين تفاعلية. يمكن لهذه شظايا الحمض النووي المتضرر أن تتسرَّب من الميتوكوندريا، وتطفو داخل الخلية، وتلتصق بـ NLRP3، مما يدفع لتجميع الالتهاب الجسيمي وموت الخلية الالتهابي.
أدوية إصلاح الحمض النووي القديمة، أدوار مضادة للالتهاب جديدة
فحص المؤلفون جزيئات صغيرة صُممت في الأصل لاستهداف إنزيم إصلاح الحمض النووي المسمى hOGG1، الذي يزيل القواعد المؤكسدة من الحمض النووي. وبشكل مفاجئ، تتفاعل هذه الأدوية — TH5487 وSU0268 ومنبه اسمه TH10785 — أيضًا مع NLRP3. في خلايا الدم المناعية البشرية وخطوط خلوية نموذجية، قللت جرعات منخفضة ميكرومولارية من TH5487 وSU0268 بشكل حاد من إفراز IL‑1β ومن تفعيل الكاسبيز‑1، الإنزيم الذي ينضج هذا السيتوكين. أظهرت تجارب شد البروتين المفصّلة والتصوير أن هذه الأدوية تمنع NLRP3 من تجميع مجمع الالتهاب الجسيمي الكامل: فهي تعيق تجنيد الشركاء الرئيسيين (ASC وNEK7 والبرو‑كاسبيز‑1) وتقلل من تكوّن «النقاط» اللامعة التي تدل على التهاب جسيمي نشط.
قطع الوصلة بين الحمض النووي التالف والالتهاب الجسيمي
نظرًا لأن تلف الميتوكوندريا هو محرك رئيسي لنشاط NLRP3، اختبر الفريق ما إذا كانت الأدوية يمكن أن تمنع تفعيل الالتهاب الجسيمي الناتج عن إجهاد الميتوكوندريا. مركب يعطل مصانع الطاقة الخلوية ويزيد أنواع الأكسجين التفاعلية عادةً يوجّه الحمض النووي الميتوكوندري المؤكسد نحو NLRP3 ويرفع مستويات IL‑1β بشدة. لم يقتصر أثر TH5487 وSU0268 على تقليل إفراز IL‑1β في هذه الظروف فحسب، بل قلّلا أيضًا من كمية NLRP3 الموجودة عند الميتوكوندريا. أكدت الميكروسكوبية الإلكترونية بالتبريد أن NLRP3 يمكنه تشكيل مجمع حلقي كبير يربط فعليًا الحمض النووي الميتوكوندري، وأشارت النمذجة الحاسوبية إلى أن مجال البيرين في البروتين يتعرف على الحمض النووي أحادي الشريطة المؤكسد عبر رقعة سطح موجبة الشحنة. تتداخل الأدوية مع خطوة استشعار الحمض النووي هذه، فتكسر وصلة حاسمة بين الحمض النووي المتضرر والالتهاب الجامح.
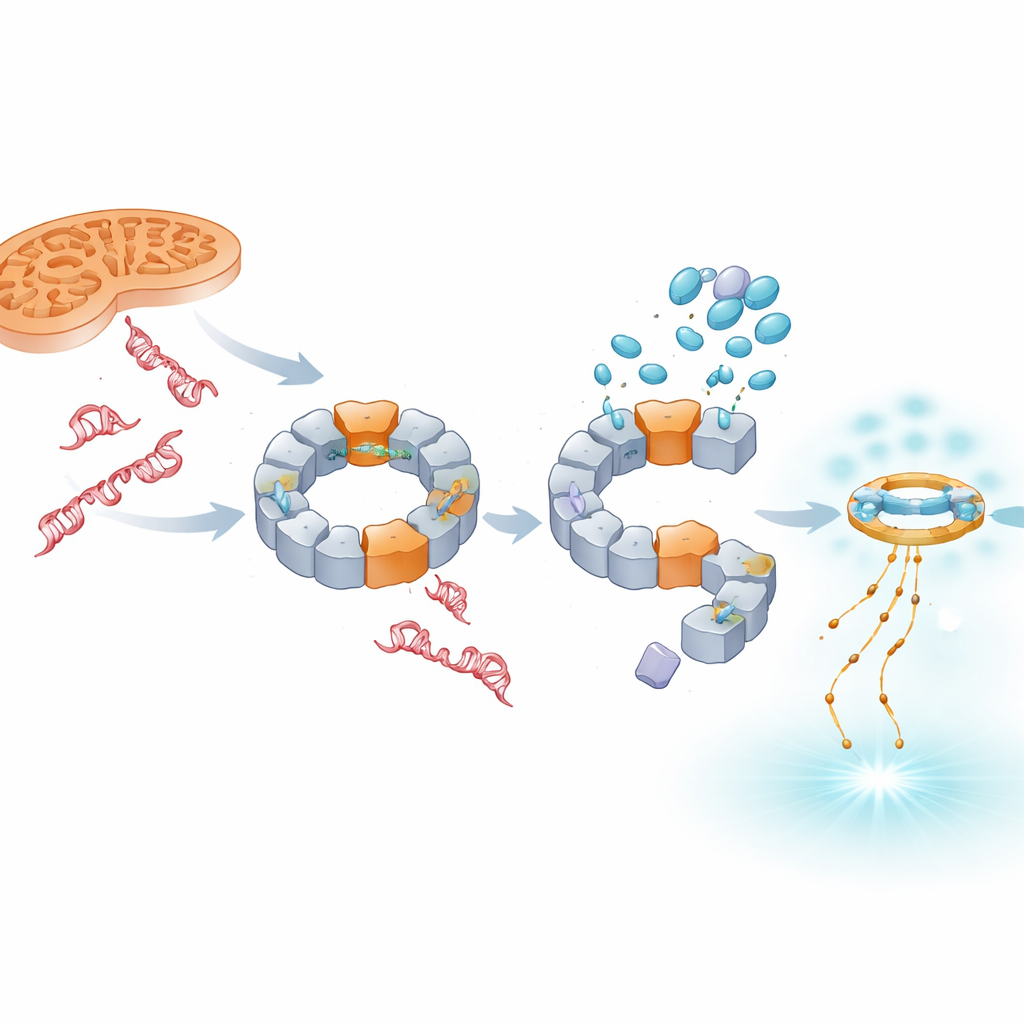
تحويل الإشارة نحو دفاعات على نمط مضاد للفيروسات
إيقاف NLRP3 لا يجعل الحمض النووي التالف يختفي؛ بدلاً من ذلك، يتراكم المزيد منه، لا سيما القادم من النواة، في سائل الخلية. تُظهر الدراسة أن هذا الحمض النووي الزائد تُلتقطه منظومة استشعار أخرى، cGAS–STING، التي تستجيب عادةً للجينومات الفيروسية. عند وجود TH5487 أو SU0268 أو TH10785، ترتفع مستويات STING المنشط والمرسال المضاد للفيروسات IFN‑β في كل من الخلايا النموذجية وخلايا الدم البشرية الأولية. ومن المهم أن هذا التعزيز يحدث حتى عند إزالة NLRP3 وراثيًا، مما يشير إلى أن cGAS–STING يعمل كإنذار احتياطي مستقل. هكذا، تُسكت هذه المركبات الالتهاب المدفوع بـ IL‑1β بينما تميل الاستجابة المناعية نحو إشارات إنترفيرون قد تكون أكثر حماية في المرض المزمن.
أمل لالتهابات وراثية صعبة المعالجة
اختبار لافت خاص شمل متلازمة الحمى الذاتية العائلية الباردة (FCAS)، اضطراب نادر تجعل فيه طفرات في NLRP3 البروتين مفرط النشاط ومقاومًا لمثبط تجريبي رائد، MCC950. في خلايا مناعية مأخوذة من فئران ومرضى بشر يحملون هذه الطفرات، فشل MCC950 في كبح إفراز IL‑1β. أما TH5487 وSU0268 فقلّلا بشكل ملحوظ هذا الإنتاج المفرط بجرعات حافظت على بقاء الخلايا. يشير ذلك إلى أن استهداف سطح استشعار الحمض النووي المؤكسد في NLRP3، بدلًا من نواته الإنزيمية التقليدية، قد يتجاوز المقاومة ويقدّم خيارات علاجية جديدة لمرضى لا تتوفر لهم حاليًا علاجات مستهدفة كثيرة.
ماذا تعني هذه النتائج للعلاجات المستقبلية
بالنسبة لشخص غير متخصص، الرسالة الأساسية هي أن الباحثين وجدوا "مفتاح إيقاف" جديدًا لماكينة التهابية قوية داخل خلايانا. عن طريق إعادة استخدام أدوية إصلاح الحمض النووي لحجب كيفية استشعار NLRP3 للحمض النووي الميتوكوندري والنووي التالف، يمكنهم تخفيف مصدر رئيسي للالتهاب المزمن مع السماح بمسار آخر لتولي زمام المبادرة وإنتاج إشارات إنترفيرون المضادة للفيروسات. إذا ثبتت سلامة هذه الاستراتيجية في دراسات لاحقة، فقد تفتح أبوابًا لعلاجات مستهدفة ليس فقط لمتلازمات الحمى الوراثية النادرة مثل FCAS، ولكن أيضًا لحالات أوسع من "الالتهاب المرتبط بالشيخوخة" حيث يغذي الالتهاب المزمن منخفض الدرجة المرض.
الاستشهاد: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
الكلمات المفتاحية: المرتكز الالتهابي NLRP3, حمض نووي ميتوكوندري مؤكسد, TH5487, مسار cGAS‑STING, أمراض التهابية ذاتية