Clear Sky Science · it
TH5487 prende di mira specificamente NLRP3 nei pazienti FCAS resistenti a MCC950
Perché è importante calmare l’infiammazione fuori controllo
Molte malattie croniche, dalle febbri rare ai disturbi legati all’invecchiamento, sono guidate da un sistema d’allarme immunitario che rifiuta di spegnersi. Questo studio esplora nuovi candidati farmacologici in grado di silenziare uno dei più potenti interruttori dell’infiammazione del corpo, chiamato NLRP3, senza però azzerare le nostre difese. Ripensando molecole esistenti originariamente destinate alla riparazione del DNA, gli autori scoprono un approccio inedito per contenere l’infiammazione dannosa e persino riconvertirla in una risposta più protettiva di tipo antivirale.
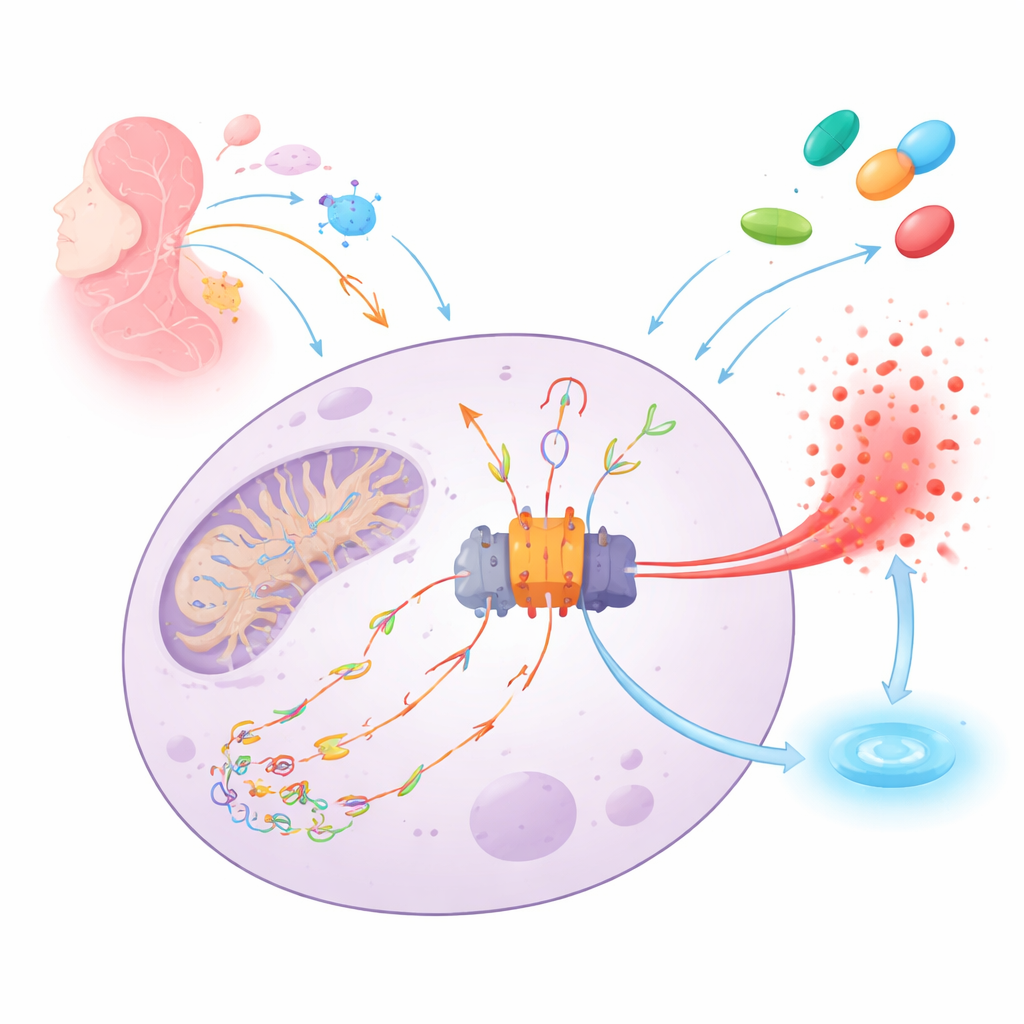
L’allarme antincendio del corpo e la sua scintilla
NLRP3 funziona come un rilevatore molecolare di fumo all’interno delle cellule immunitarie. Quando avverte un pericolo—dalle infezioni ai danni tissutali—si assembla in una grande macchina proteica (l’inflammasoma) che scatena il rilascio del potente segnale d’allarme IL‑1β e può provocare la lisi cellulare per avvertire le cellule vicine. Una scintilla chiave per questo allarme è rappresentata dal DNA mitocondriale danneggiato, inciso e ossidato da specie reattive dell’ossigeno. Questi frammenti di DNA danneggiato possono fuoriuscire dai mitocondri, muoversi nel citosol, legare NLRP3 e promuovere l’assemblaggio dell’inflammasoma e la morte infiammatoria della cellula.
Vecchi farmaci per la riparazione del DNA, nuovi ruoli antiinfiammatori
Gli autori hanno esaminato piccole molecole concepite inizialmente per colpire un enzima di riparazione del DNA chiamato hOGG1, che rimuove basi ossidate dal DNA. Sorprendentemente, questi farmaci—TH5487, SU0268 e un attivatore denominato TH10785—interagiscono anche con NLRP3. In cellule immunitarie del sangue umano e in linee cellulari modello, dosi micromolari basse di TH5487 e SU0268 hanno ridotto nettamente il rilascio di IL‑1β e l’attivazione della caspasi‑1, l’enzima che matura questa citochina. Esperimenti dettagliati di pull‑down proteico e di imaging hanno mostrato che i farmaci impediscono a NLRP3 di assemblare il complesso completo dell’inflammasoma: bloccano il reclutamento di partner chiave (ASC, NEK7 e pro‑caspasi‑1) e riducono la formazione delle luminose “speck” che indicano un inflammasoma attivo.
Recidere il collegamento tra DNA danneggiato e inflammasoma
Poiché il danno mitocondriale è un importante motore dell’attività di NLRP3, il gruppo ha verificato se i farmaci potessero bloccare l’attivazione dell’inflammasoma indotta dallo stress mitocondriale. Un composto che compromette le centrali energetiche della cellula e aumenta le specie reattive dell’ossigeno normalmente indirizza il DNA mitocondriale ossidato verso NLRP3 e aumenta fortemente i livelli di IL‑1β. TH5487 e SU0268 non solo hanno ridotto il rilascio di IL‑1β in queste condizioni, ma hanno anche diminuito la quantità di NLRP3 localizzata nei mitocondri. La crio‑microscopia elettronica ha confermato che NLRP3 può formare un grande complesso ad anello che lega fisicamente il DNA mitocondriale, e la modellizzazione al computer ha suggerito che il dominio pirina della proteina riconosce il DNA a filamento singolo ossidato tramite una superficie carica positivamente. I farmaci interferiscono con questo passaggio di riconoscimento del DNA, recidendo un collegamento cruciale tra DNA danneggiato e infiammazione fuori controllo.
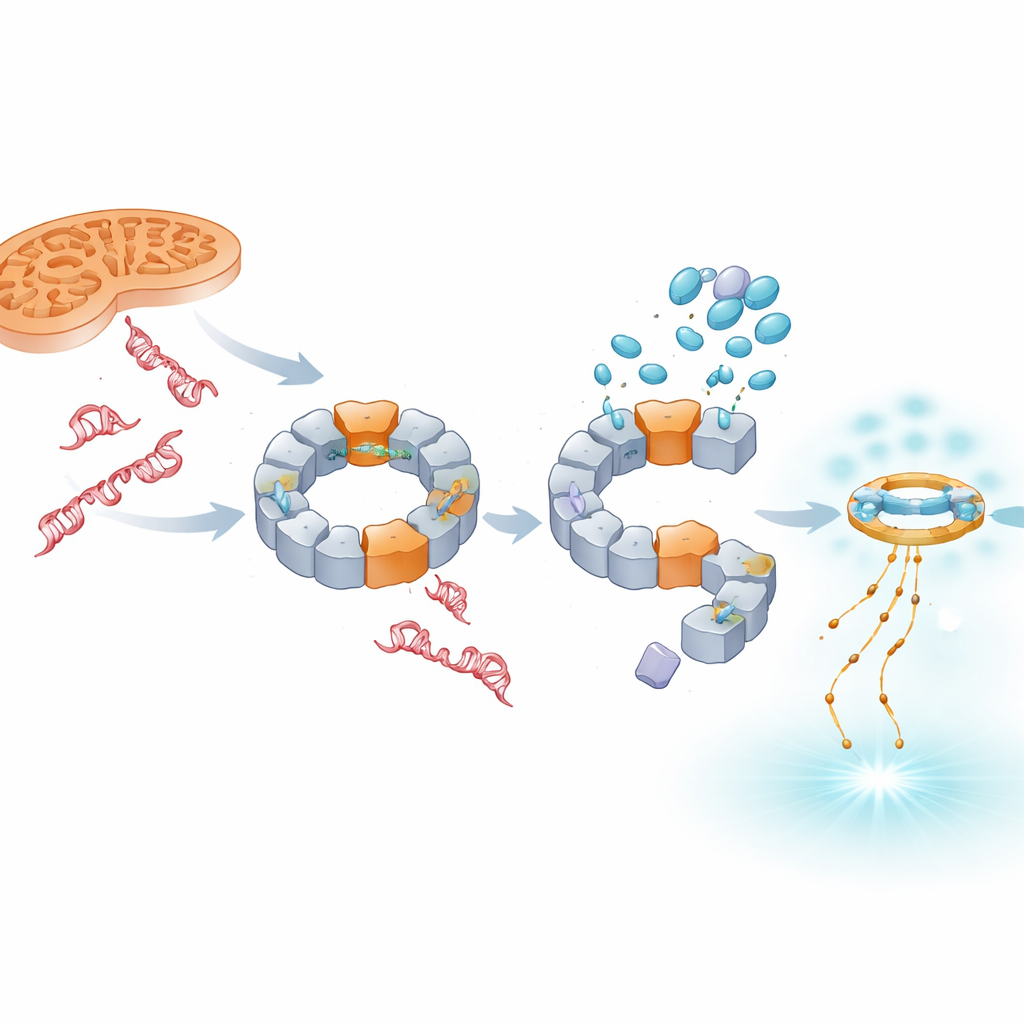
Riorientare il segnale verso difese di tipo antivirale
Bloccare NLRP3 non fa sparire il DNA danneggiato; al contrario, una maggiore quantità di DNA, in particolare di origine nucleare, si accumula nel fluido cellulare. Lo studio mostra che questo DNA in eccesso viene captato da un altro sistema sensore, cGAS–STING, che normalmente risponde ai genomi virali. In presenza di TH5487, SU0268 o TH10785 aumentano i livelli di STING attivato e del messaggero antivirale IFN‑β sia nelle cellule modello sia nelle cellule del sangue umano primarie. È importante sottolineare che questo incremento avviene anche quando NLRP3 è rimosso geneticamente, indicando che cGAS–STING agisce come un allarme di riserva indipendente. Pertanto, questi composti attenuano l’infiammazione guidata da IL‑1β pur spostando la risposta immunitaria verso una segnalazione a interferoni che potrebbe essere più protettiva nelle malattie croniche.
Promesse per l’infiammazione ereditaria difficile da trattare
Un test particolarmente significativo ha riguardato la Sindrome Autoinfiammatoria Familiare da Freddo (FCAS), un disturbo raro in cui mutazioni di NLRP3 la rendono iperattiva e resistente a un inibitore sperimentale di punta, MCC950. Nelle cellule immunitarie di topi e pazienti umani portatori di queste mutazioni, MCC950 non è riuscito a contenere il rilascio di IL‑1β. TH5487 e SU0268, invece, hanno ridotto in modo significativo questa sovrapproduzione a dosi che non compromettevano la vitalità cellulare. Ciò suggerisce che mirare la superficie di NLRP3 che riconosce il DNA ossidato, piuttosto che il suo nucleo enzimatica più tradizionale, potrebbe aggirare la resistenza e offrire nuove opzioni terapeutiche per pazienti per i quali oggi le terapie mirate sono limitate.
Cosa significano questi risultati per le terapie future
Per un non specialista, il messaggio principale è che i ricercatori hanno individuato un nuovo “interruttore” per una potente macchina infiammatoria nelle nostre cellule. Ripropongendo farmaci per la riparazione del DNA per bloccare il modo in cui NLRP3 sente il DNA mitocondriale e nucleare danneggiato, è possibile attenuare una fonte importante di infiammazione cronica permettendo a un’altra via di subentrare e produrre segnali interferonici antivirali. Se questa strategia si dimostrerà sicura in ulteriori studi, potrebbe aprire trattamenti mirati non solo per sindromi febbrili ereditarie rare come la FCAS, ma anche per condizioni più ampie di “inflammaging” in cui un’infiammazione persistente e di basso grado alimenta la malattia.
Citazione: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
Parole chiave: inflammasoma NLRP3, DNA mitocondriale ossidato, TH5487, via cGAS-STING, malattia autoinfiammatoria