Clear Sky Science · ja
TH5487はMCC950に耐性を示すFCAS患者で特異的にNLRP3を標的とする
暴走する炎症を鎮めることが重要な理由
稀な発熱性疾患から加齢関連障害に至るまで、多くの慢性疾患はオフにできない免疫の警報システムによって駆動されます。本研究は、NLRP3と呼ばれる体内で最も強力な炎症スイッチの一つを、防御機能を完全に停止させることなく鎮められる新たな薬剤候補を探ります。DNA修復を標的にしていた既存の分子を再考することで、著者らは有害な炎症を抑え、さらにはそれをより保護的な抗ウイルス様応答へと向け直す新しい方法を明らかにします。
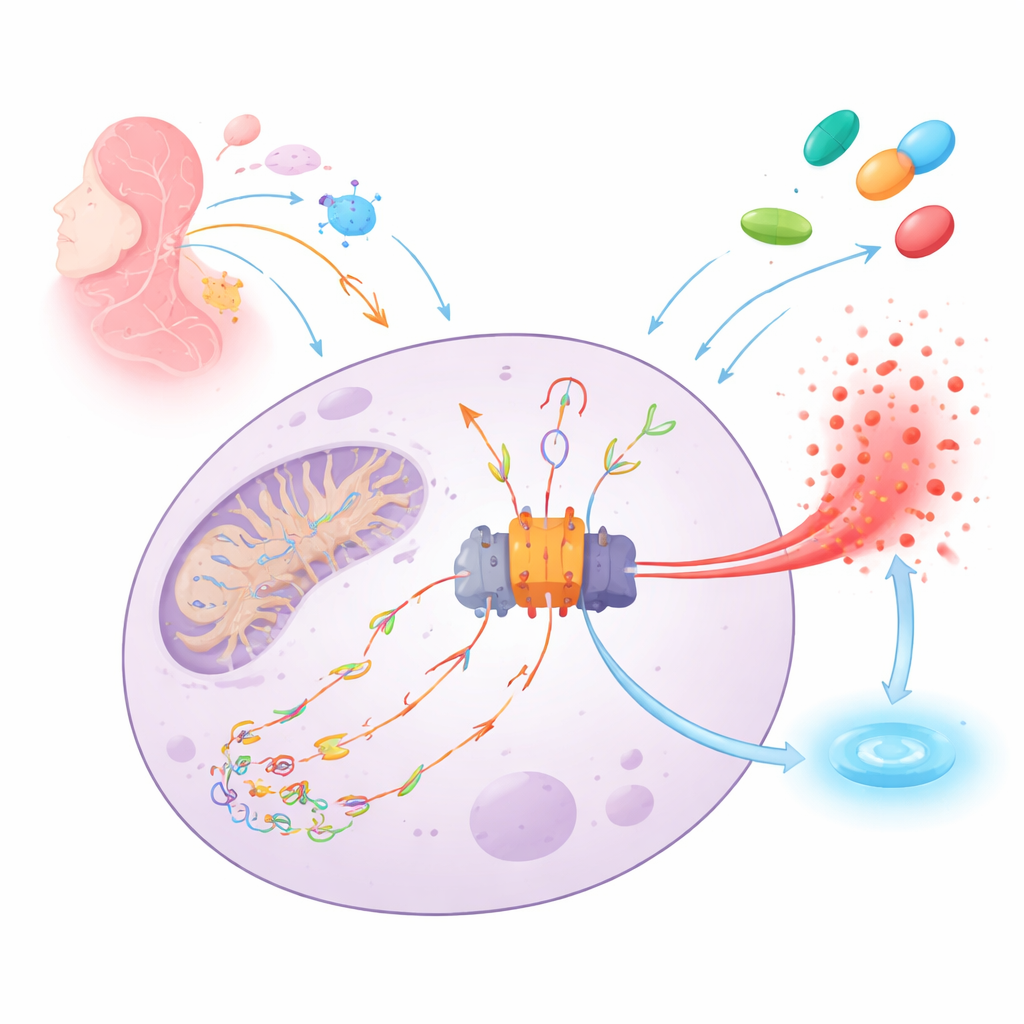
体内の火災報知機とその火花
NLRP3は免疫細胞内の分子的煙検出器のように作用します。感染から組織損傷に至るまでの危険を感知すると、大きなタンパク質機構(インフラマソーム)を組み立て、強力な警報シグナルであるIL‑1βの放出を引き起こし、隣接細胞に警告するために細胞を破裂させることがあります。この警報の主要な火花は、活性酸素種によって切断・酸化された損傷ミトコンドリアDNAです。これらの損傷DNA断片はミトコンドリアから漏出して細胞内を漂い、NLRP3に結合してインフラマソームの組立てと炎症性細胞死を促進します。
古いDNA修復薬の新たな抗炎症作用
著者らは、酸化塩基を除去するDNA修復酵素hOGG1を標的に設計された小分子を調べました。驚くべきことに、これらの薬剤—TH5487、SU0268、および活性化剤であるTH10785—はNLRP3とも相互作用します。ヒト末梢血免疫細胞およびモデル細胞株で、低マイクロモル濃度のTH5487とSU0268はIL‑1βの放出とこのサイトカインを成熟させる酵素カスパーゼ‑1の活性化を著しく抑制しました。詳細なタンパク質プルダウンとイメージング実験により、これらの薬剤はNLRP3が完全なインフラマソーム複合体を組み立てるのを阻害することが示されました:ASC、NEK7、プロカスパーゼ‑1といった重要なパートナーの動員を遮断し、活性インフラマソームを示す明るい「スペック」の形成を減少させます。
損傷DNAとインフラマソームをつなぐ結び目を断つ
ミトコンドリア損傷がNLRP3活性の主要な駆動因子であるため、研究チームはこれらの薬剤がミトコンドリアストレスによって誘導されるインフラマソーム活性化を阻止できるかを検証しました。細胞のエネルギー工場を撹乱し活性酸素種を増加させる化合物は通常、酸化されたミトコンドリアDNAをNLRP3へ送ってIL‑1βレベルを強く上昇させます。TH5487とSU0268はこうした条件下でIL‑1βの放出を抑えるだけでなく、ミトコンドリアに存在するNLRP3の量も減少させました。クライオ電子顕微鏡は、NLRP3がミトコンドリアDNAに物理的に結合する大きな環状複合体を形成し得ることを確認し、計算モデルはタンパク質のパイリン領域が正に帯電した表面パッチを介して酸化された一本鎖DNAを認識することを示唆しました。これらの薬剤はこのDNA検知段階に干渉し、損傷DNAと暴走する炎症との重要な結び目を断ちます。
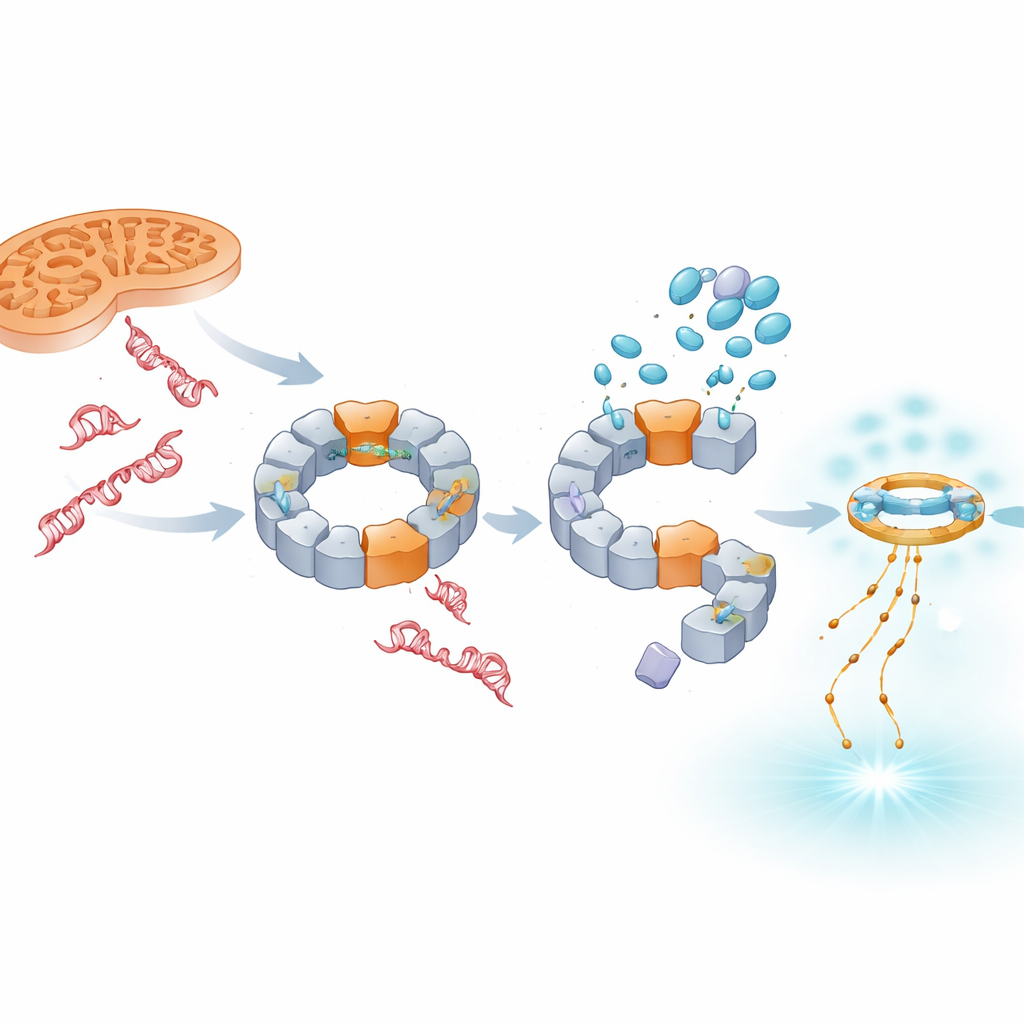
抗ウイルス様防御へ信号をシフトする
NLRP3を遮断しても損傷DNAが消えるわけではなく、代わりに特に核由来のDNAが細胞質内に蓄積します。本研究は、この過剰なDNAが通常はウイルスゲノムに応答する別のセンサー系であるcGAS–STINGによって検出されることを示します。TH5487、SU0268、TH10785が存在すると、モデル細胞および一次ヒト血液細胞の両方で活性化されたSTINGと抗ウイルス性メッセンジャーIFN‑βのレベルが上昇します。重要なのは、この増強がNLRP3を遺伝的に除去した場合でも起こることで、cGAS–STINGが独立したバックアップの警報として作用することを示しています。したがって、これらの化合物はIL‑1β駆動の炎症を静めつつ、慢性疾患でより保護的である可能性のあるインターフェロンベースのシグナルへ免疫応答を傾けます。
治療が困難な遺伝性炎症への期待
特に注目すべき試験は家族性寒冷自己炎症症候群(FCAS)で行われました。これはNLRP3の変異が過剰活性を引き起こし、主要な実験的阻害剤MCC950に耐性を示す稀な疾患です。これらの変異を持つマウスおよびヒト患者由来の免疫細胞では、MCC950はIL‑1β放出を抑制できませんでした。しかしTH5487とSU0268は、細胞生存性を損なうことなく過剰産生を有意に低下させました。これは、NLRP3の従来の酵素中心部ではなく酸化DNAを感知する表面を標的にすることで、耐性を回避し、現在標的療法が限られる患者に新たな治療選択肢を提供し得ることを示唆します。
将来の治療への示唆
専門外の読者にとっての核心は、研究者らが細胞内の強力な炎症機構に対する新たな「オフスイッチ」を見つけたという点です。DNA修復薬を再利用してNLRP3が損傷したミトコンドリアおよび核DNAを感知する方法を遮断することで、慢性炎症の主要な原因を抑えつつ別の経路が代わりに抗ウイルス的なインターフェロン信号を生成できるようにします。この戦略がさらに安全性の検証に耐えられれば、FCASのような稀な遺伝性発熱症候群だけでなく、持続的で低度の炎症が疾患を助長する「炎症性老化(inflammaging)」のようなより広い状態に対する標的治療の道を開く可能性があります。
引用: Lackner, A., Picucci, S.I., Jiang, W. et al. TH5487 specifically targets NLRP3 in FCAS patients resistant to MCC950. Commun Biol 9, 528 (2026). https://doi.org/10.1038/s42003-026-10008-2
キーワード: NLRP3インフラマソーム, 酸化ミトコンドリアDNA, TH5487, cGAS-STING経路, 自己炎症性疾患