Clear Sky Science · zh
连接组蛋白 H1 抑制由 H4 尾部乙酰化诱导的 H3 尾部乙酰化并改变其动力学
为什么微小的蛋白尾端对我们的 DNA 很重要
在每个细胞内部,近两米长的 DNA 被压缩装入一个微小的细胞核中。实现这一折叠的工作由称为组蛋白的一类梭状蛋白承担,它们帮助决定基因是被开启还是关闭。本研究探讨了这些组蛋白上的小型化学标记与另一种称为连接组蛋白 H1 的蛋白如何协同作用,或使 DNA 为基因表达开放,或将其保持封闭。理解这种平衡有助于阐明细胞如何在长期内记住哪些基因应当保持活跃或沉默。
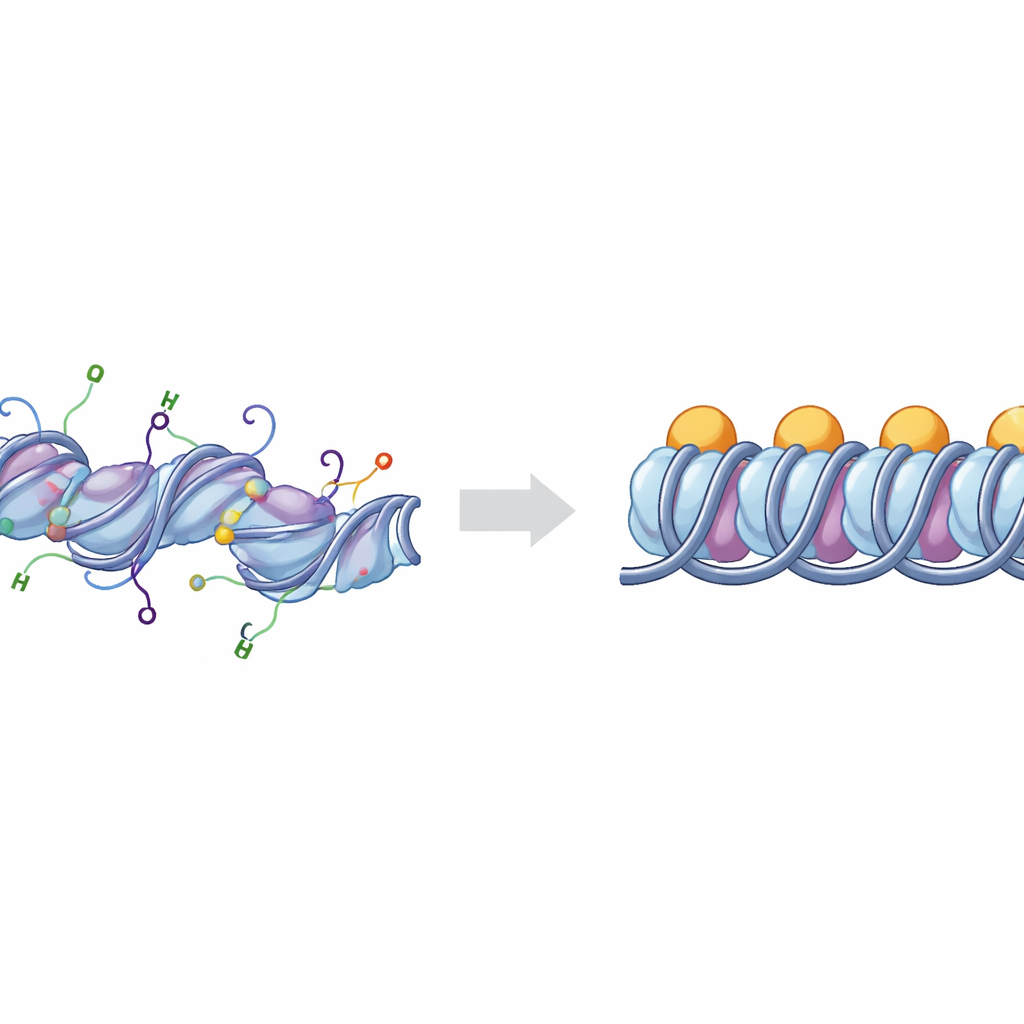
DNA 打包的基本构件
我们的染色体中的 DNA 绕在组蛋白簇上形成称为核小体的结构单元。当一块额外的蛋白——连接组蛋白 H1——结合在 DNA 进入和退出核小体的部位时,该结构被称为染色体小体(chromatosome)。染色体小体可以成组叠加和折叠,形成通常不太活跃的高密度 DNA 区域。细胞通过在从组蛋白伸出的柔性“尾部”上施加化学标记来微调这种打包状态。最重要的两个尾部属于组蛋白 H3 和 H4,它们的化学修饰与 DNA 区域表现为活跃、开放的“常染色质”还是沉默、致密的“异染色质”密切相关。
一个尾部的改变如何影响另一个尾部
早期研究显示,在 H4 尾部添加四个乙酰基——统称为 H4‑4Kac——倾向于也使邻近的 H3 尾更易被乙酰化,但这些研究主要是在没有连接组蛋白 H1 的情况下进行的。新的研究询问了在存在 H1 的情况下会发生什么,这更接近细胞内的真实情形。通过冷冻电子显微镜,作者解析了携带乙酰化 H4 尾的染色体小体的高分辨率结构。令人惊讶的是,与未修饰的染色体小体相比,核心 DNA 与组蛋白的整体形态几乎没有变化。H1 蛋白仍位于相同的中心位置,缠绕的 DNA 也几乎相同,这表明任何重要效应很可能来自可摆动的组蛋白尾部如何移动并接触 DNA 的变化。
用模拟与磁共振追踪可动部件
为捕捉这些快速而微妙的运动,团队将计算机模拟与核磁共振(NMR)光谱相结合。粗粒化分子动力学模拟模拟了 H3 与 H4 尾部如何擦过缠绕的 DNA 以及连接核小体间的暴露链接 DNA。在染色体小体中,H1 的存在自然使两条 H3 尾表现出差异:一条主要接触包裹核心的 DNA,而另一条也接触暴露的链接 DNA。当 H4 被乙酰化时,它自身的尾部会从 DNA 上剥离,变得更灵活并更多暴露于溶剂中。这种释放会略微改变 H1 的长尾和两条 H3 尾探索 DNA 表面的方式,但模拟显示接触模式的平均变化只是适度的。
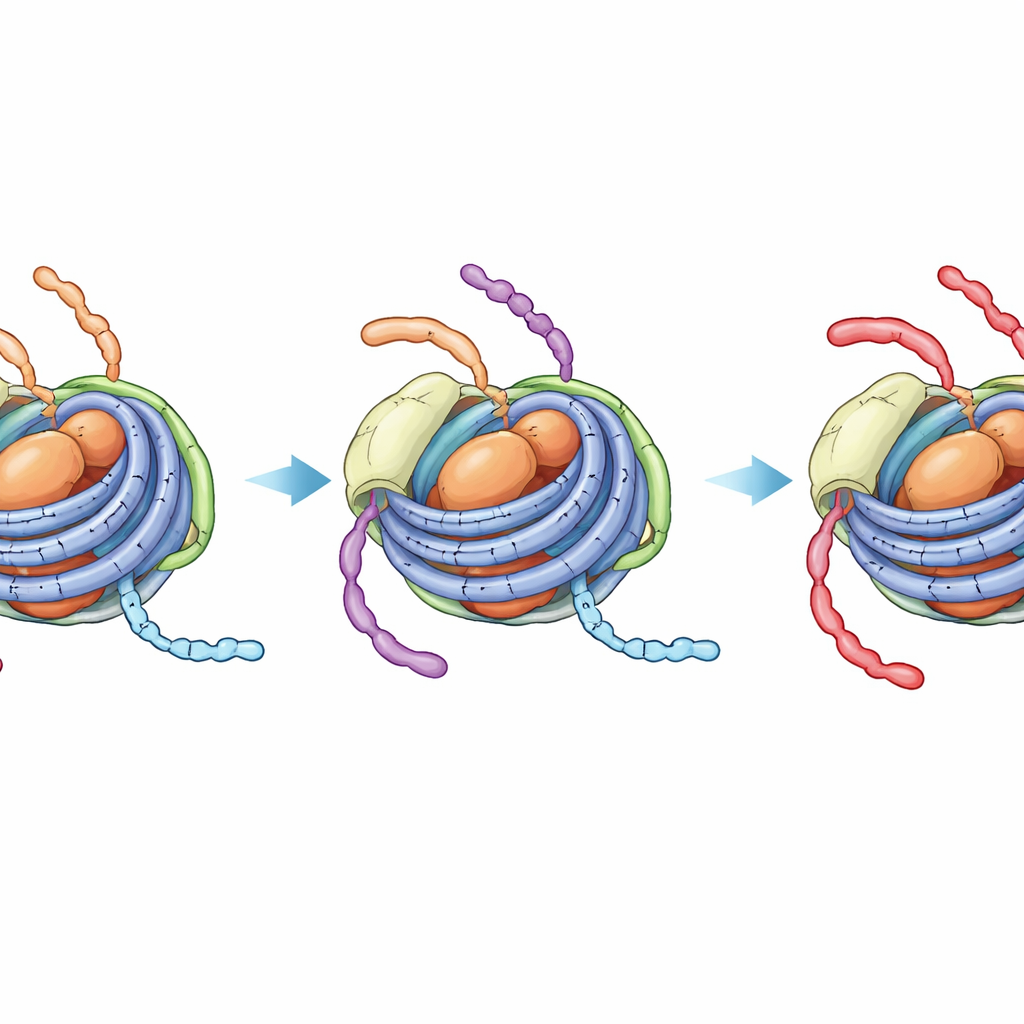
阻止进一步改变的隐性更紧致状态
核磁共振光谱学能够感知特定原子的局部环境,揭示出更为显著的效应。在未修饰的染色体小体中,来自 H3 尾的信号显示出两种动态状态的混合——一种类似较开放的核小体(与链接 DNA 有接触),另一种类似更紧密的仅含核心的核小体颗粒。在酶促反应的时间尺度上,这些状态会互相转换,因此能乙酰化 H3 尾上 K14 位点的酶仍能接触到暴露于链接 DNA 的片段。相比之下,当 H4 尾携带四个乙酰基且存在 H1 时,H3 尾的信号塌缩为单一且稳定的状态,看起来像紧密结合核心 DNA 的形式。对乙酰化反应的直接 NMR 监测证实,此时 H3 K14 的修饰速度明显变慢,几乎与完全没有链接 DNA 的封闭核小体相同。
这对基因开关意味着什么
综合来看,结果表明在连接组蛋白 H1 存在的情况下,H4 尾的乙酰化反而有助于将邻近的 H3 尾锁定在核心 DNA 上,而不是释放它们以便进一步修饰。通过促进这种稳定的、拥抱 DNA 的状态并大幅放慢 H3 的额外乙酰化,H1 似乎抵消了开放、活跃染色质的扩散,转而有利于更致密、沉默的区域。通俗地说,这项研究表明一组化学标记和一个额外的蛋白就能决定邻近的 DNA 区域是保持可用状态还是被折叠存储,从而为理解细胞如何随时间维持其身份提供了新的见解。
引用: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
关键词: 染色质结构, 组蛋白乙酰化, 连接组蛋白 H1, 核小体动力学, 表观遗传调控