Clear Sky Science · tr
Bağlayıcı histon H1, H4 kuyruğu asetilasyonu ile tetiklenen H3 kuyruk asetilasyonunu baskılar ve dinamiklerini değiştirir
DNA’mız için küçük protein kuyruklarının neden önemi var
Her hücrenin içinde, neredeyse iki metre uzunluğundaki DNA mikroskobik bir çekirdeğe paketlenmiştir. Bu katlama işi, genlerin açık mı kapalı mı olacağına karar vermede rol oynayan histon adı verilen makara benzeri proteinler tarafından yapılır. Yeni çalışma, bu histonların üzerindeki küçük kimyasal işaretlerin ve bağlayıcı histon H1 adlı başka bir proteinin bir arada nasıl işleyip DNA’yı gen etkinliği için açtığını ya da kilitlediğini araştırdı. Bu dengelerin anlaşılması, hücrelerin hangi genlerin uzun vadede aktif veya sessiz kalacağını nasıl “hafızada” tutabildiğine ışık tutuyor.
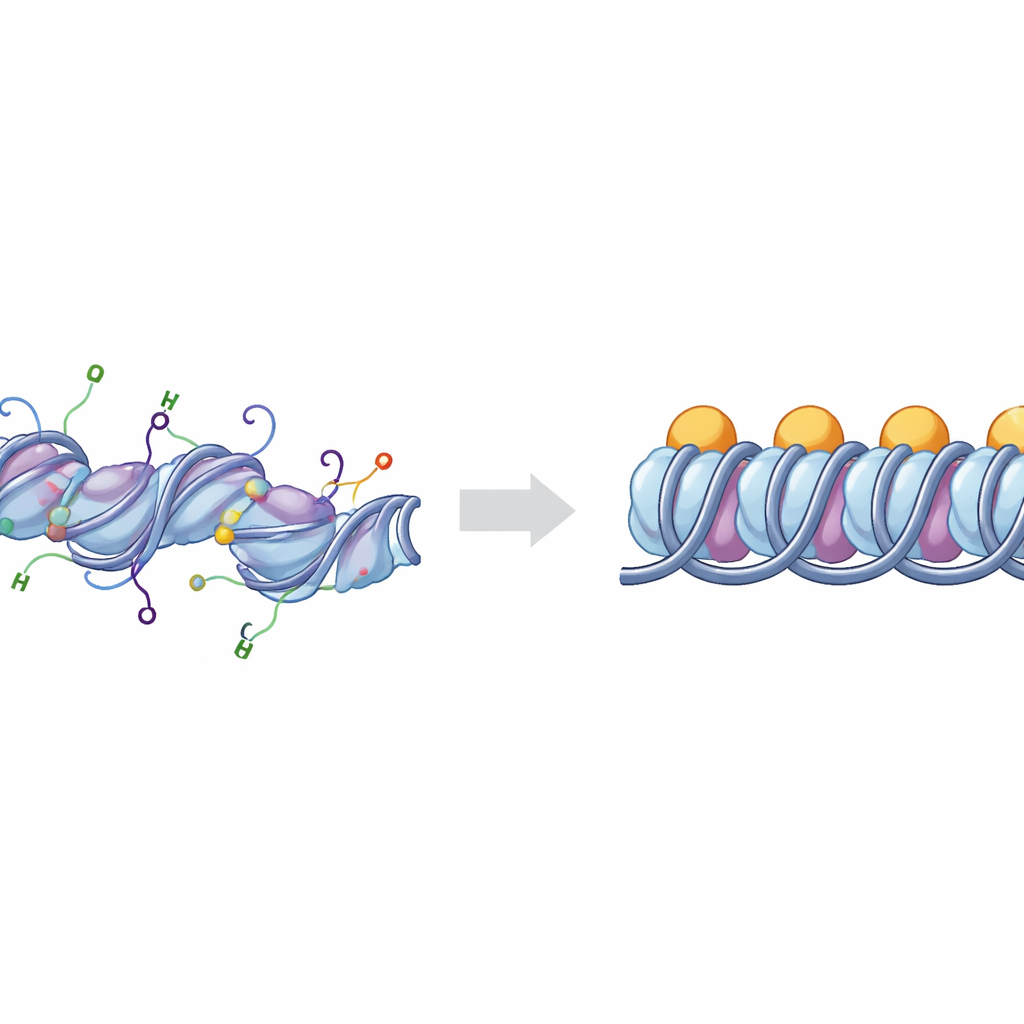
DNA paketlemenin temel yapı taşları
Kromozomlarımızdaki DNA, nükleozom adı verilen histon protein kümelerinin etrafına sarılır. Ek bir protein olan bağlayıcı histon H1, DNA’nın nükleozoma giriş ve çıkış noktalarına bağlandığında yapı kromatosom olarak adlandırılır. Kromatosom grupları üst üste konup katlanarak genellikle daha az aktif olan sıkı paketlenmiş DNA bölgelerini oluşturabilir. Hücreler, histonlardan çıkan esnek “kuyruklara” konan kimyasal işaretlerle bu paketlemeyi ince ayarlar. En önemli kuyruklardan ikisi H3 ve H4 histonlarına aittir; bunların kimyasal değişiklikleri, DNA bölgelerinin açık, aktif “öukromatin” mi yoksa sessiz, kompakt “heterokromatin” mi olduğu ile güçlü biçimde ilişkilidir.
Bir kuyruğun değişimi diğerini nasıl etkiler
Önceki çalışmalar, H4 kuyruğuna dört asetil grubunun eklenmesinin—toplu olarak H4‑4Kac olarak bilinen—komşu H3 kuyruğunun da asetileşmesini kolaylaştırma eğiliminde olduğunu göstermişti, ancak bunlar ağırlıklı olarak bağlayıcı histon H1 olmadan incelenmişti. Yeni araştırma, H1’in var olduğu durumda ne olduğunu, yani canlı hücrelerde daha gerçekçi bir durumu sordu. Kriy-elektron mikroskobu kullanarak yazarlar, asetillenmiş H4 kuyruğu taşıyan kromatosomların yüksek çözünürlüklü yapısını çözdüler. Şaşırtıcı biçimde, çekirdek DNA ve histon proteinlerinin genel şekli, değiştirilmemiş kromatosomlarla neredeyse aynı kaldı. H1 proteini hâlâ aynı merkezi konumda oturuyor ve sarılı DNA neredeyse aynı görünüyordu; bu da önemli etkilerin gevşek histon kuyruklarının DNA ile nasıl hareket edip temas ettiğindeki değişikliklerden kaynaklanması gerektiğini düşündürdü.
Hareketli parçaları simülasyonlar ve mıknatıslarla izlemek
Bu hızlı, ince hareketleri yakalamak için ekip bilgisayar simülasyonlarını nükleer manyetik rezonans (NMR) spektroskopisi ile birleştirdi. Kaba taneli moleküler dinamik simülasyonlar, H3 ve H4 kuyruklarının sarılı DNA ile ve nükleozomları birbirine bağlayan ek DNA uzantılarıyla nasıl sürtündüğünü modelledi. Kromatosomlarda H1’in varlığı, doğal olarak iki H3 kuyruğunun farklı davranmasına yol açtı: biri ağırlıklı olarak çekirdeğe sarılmış DNA ile temas etme eğilimindeyken, diğeri ayrıca açığa çıkmış bağlayıcı DNA ile de temas etti. H4 asetillenince, kendi kuyruğu DNA’dan ayrılıp daha esnek ve çözücüye açık hale geldi. Bu serbestleşme, H1’in uzun kuyruğunun ve H3 kuyruklarının DNA yüzeyini keşfetme biçimini bir miktar kaydırdı, ancak simülasyonlar ortalama temas desenlerinde yalnızca mütevazı değişiklikler olduğunu öne sürdü.
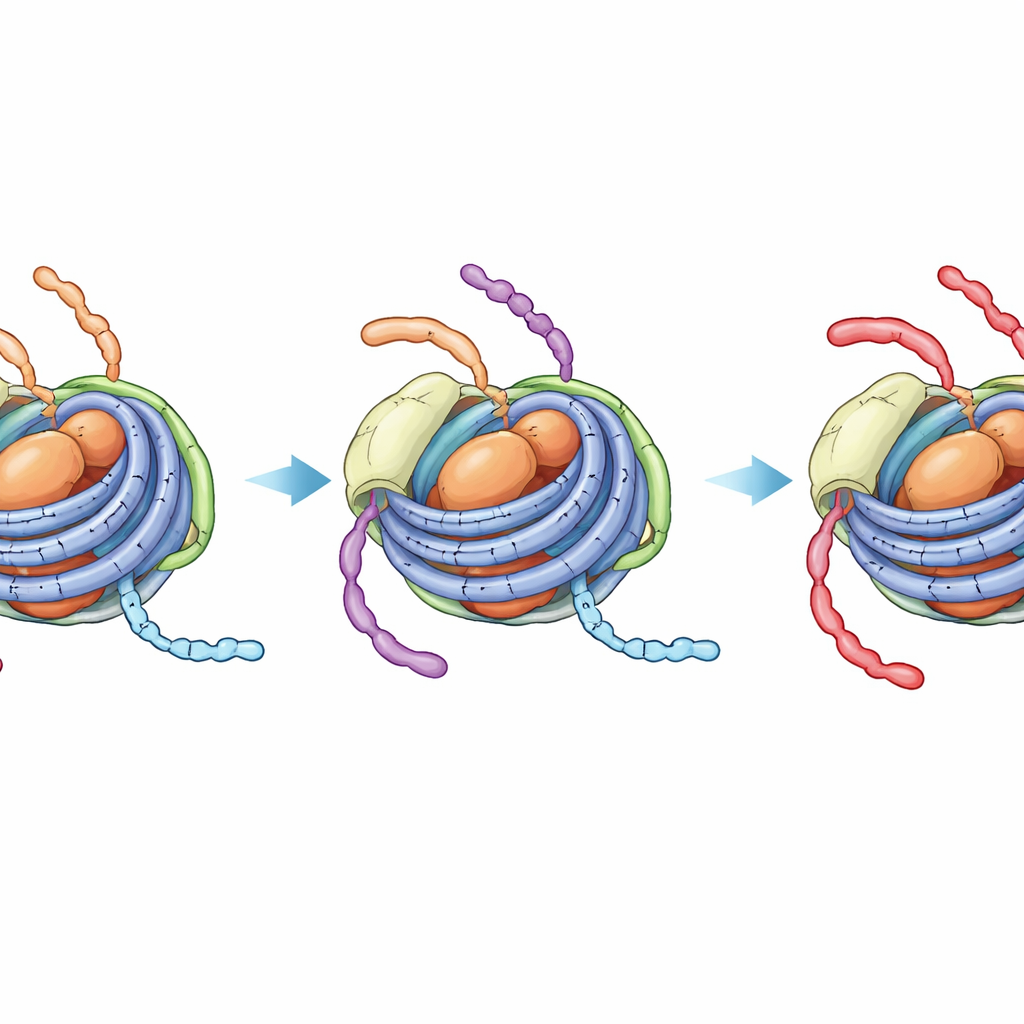
İlave değişikliği engelleyen gizli, daha sıkı bir durum
Belli atomların yerel ortamını algılayan NMR spektroskopisi daha çarpıcı bir etki ortaya koydu. Değiştirilmemiş kromatosomlarda H3 kuyruğundan gelen sinyaller iki dinamik durumun karışımını gösteriyordu—biri bağlayıcı DNA ile teması olan daha açık nükleozoma benzer, diğeri ise daha sıkı yalnızca çekirdek nükleozom partikülüne benzer. Bir enzim reaksiyonunun zaman ölçeğinde bu durumlar birbirinin yerine geçiyor, böylece H3 kuyruğundaki K14 pozisyonunu asetilleyen enzim hâlâ bağlayıcıyla açığa çıkmış segmentlere erişebiliyordu. Buna karşılık, H4 kuyruğu dört asetil grubunu taşıdığında ve H1 mevcut olduğunda H3 kuyruk sinyalleri tek, sağlam bir duruma çöktü; bu durum sıkıca bağlanmış çekirdek‑DNA formuna benziyordu. Asetilasyon reaksiyonunun doğrudan NMR izlemesi, H3 K14’ün o zaman çok daha yavaş modifiye olduğunu; neredeyse hiç bağlayıcı DNA olmayan kapalı nükleozom çekirdeğinden ayırt edilemeyecek bir hızda gerçekleştiğini doğruladı.
Bu gen açma/kapatma anahtarları için ne anlama geliyor
Bir araya getirildiğinde bulgular, H4 kuyruğunun asetilasyonunun, bağlayıcı histon H1 varlığında paradoksal olarak komşu H3 kuyruklarını daha fazla değişiklik için serbest bırakmak yerine çekirdek DNA’ya karşı kilitlemeye yardımcı olduğunu öne sürüyor. Bu stabil, DNA’ya sarılan durumu teşvik ederek ve H3’ün ilave asetilasyonunu büyük ölçüde yavaşlatarak H1, açık ve aktif kromatinin yayılmasına karşı duruyor ve bunun yerine daha kompakt, sessiz bölgeleri destekliyor gibi görünüyor. Günlük anlatımla, çalışma bir dizi kimyasal işaretin ve tek bir ek proteinin, yakınlardaki DNA parçalarının iş yapmaya açık mı kalacağına yoksa uzun vadeli depolama için katlanıp kaldırılacağına karar verebileceğini gösteriyor; bu da hücrelerin kimliklerini zaman içinde nasıl koruduklarına dair yeni bir anlayış katmanı ekliyor.
Atıf: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Anahtar kelimeler: kromatin yapısı, histon asetilasyonu, bağlayıcı histon H1, nükleozom dinamikleri, epigenetik düzenleme