Clear Sky Science · es
La histona de enlace H1 reprime la acetilación de la cola de H3 inducida por la acetilación de la cola de H4 y altera su dinámica
Por qué importan las pequeñas colas de las proteínas para nuestro ADN
Dentro de cada célula, casi dos metros de ADN se empaquetan en un núcleo microscópico. Este logro de plegamiento lo gestionan carretes de proteínas llamadas histonas, que ayudan a decidir si los genes están encendidos o apagados. El nuevo estudio explora cómo pequeñas marcas químicas en estas histonas, y la presencia de otra proteína llamada histona de enlace H1, actúan conjuntamente para abrir el ADN y permitir la actividad génica o para mantenerlo cerrado. Comprender este equilibrio arroja luz sobre cómo las células mantienen la memoria a largo plazo de qué genes deben permanecer activos o silenciados.
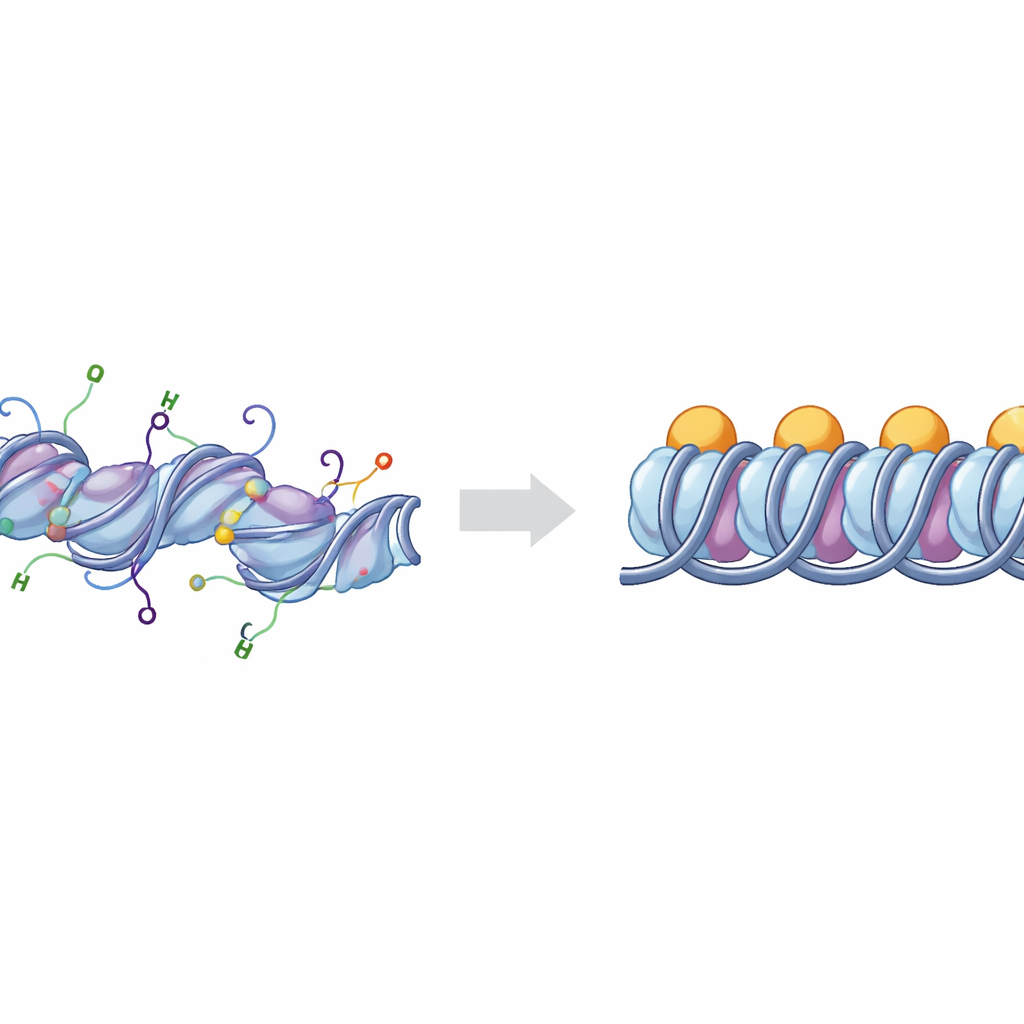
Los bloques básicos del empaquetamiento del ADN
El ADN en nuestros cromosomas se enrolla alrededor de conjuntos de proteínas histonas para formar unidades conocidas como nucleosomas. Cuando una proteína extra, la histona de enlace H1, se une en los puntos donde el ADN entra y sale del nucleosoma, la estructura recibe el nombre de cromatosoma. Grupos de cromatosomas pueden apilarse y plegarse para crear regiones de ADN densamente empaquetadas que, por lo general, son menos activas. Las células afinan este empaquetamiento con marcas químicas colocadas en las “colas” flexibles que se extienden desde las histonas. Dos de las colas más importantes pertenecen a las histonas H3 y H4, cuyos cambios químicos están fuertemente ligados a si las regiones de ADN se comportan como euchromatina abierta y activa o como heterocromatina compacta y silenciosa.
Cómo el cambio en una cola afecta a otra
Trabajos anteriores mostraron que añadir cuatro grupos acetilo a la cola de H4—en posiciones conocidas colectivamente como H4‑4Kac—tiende a facilitar también la acetilación de la cola vecina H3, pero eso se estudió principalmente sin la histona de enlace H1. La nueva investigación preguntó qué sucede cuando H1 está presente, una situación más realista en las células vivas. Usando criomicroscopía electrónica, los autores resolvieron estructuras de alta resolución de cromatosomas que portaban la cola de H4 acetilada. Sorprendentemente, la forma global del ADN central y de las histonas apenas cambió en comparación con cromatosomas no modificados. La proteína H1 seguía situada en la misma posición central y el ADN arrollado se veía casi idéntico, lo que sugiere que los efectos importantes deben proceder de cambios en cómo se mueven las colas flexibles de las histonas y cómo contactan con el ADN.
Siguiendo las piezas móviles con simulaciones y imanes
Para capturar estos movimientos rápidos y sutiles, el equipo combinó simulaciones por ordenador con espectroscopía de resonancia magnética nuclear (RMN). Simulaciones de dinámica molecular a grano grueso modelaron cómo las colas de H3 y H4 rozan el ADN arrollado y los tramos adicionales de ADN que enlazan nucleosomas. En los cromatosomas, la presencia de H1 hace que naturalmente las dos colas H3 se comporten de forma distinta: una tiende a tocar principalmente el ADN envuelto alrededor del núcleo, mientras que la otra también contacta con el ADN exposado del enlace. Cuando H4 está acetilada, su propia cola se desprende del ADN, volviéndose más flexible y expuesta al disolvente. Esta liberación desplaza ligeramente la forma en que tanto la larga cola de H1 como las colas de H3 exploran la superficie del ADN, pero las simulaciones sugirieron solo cambios promedio modestos en los patrones de contacto.
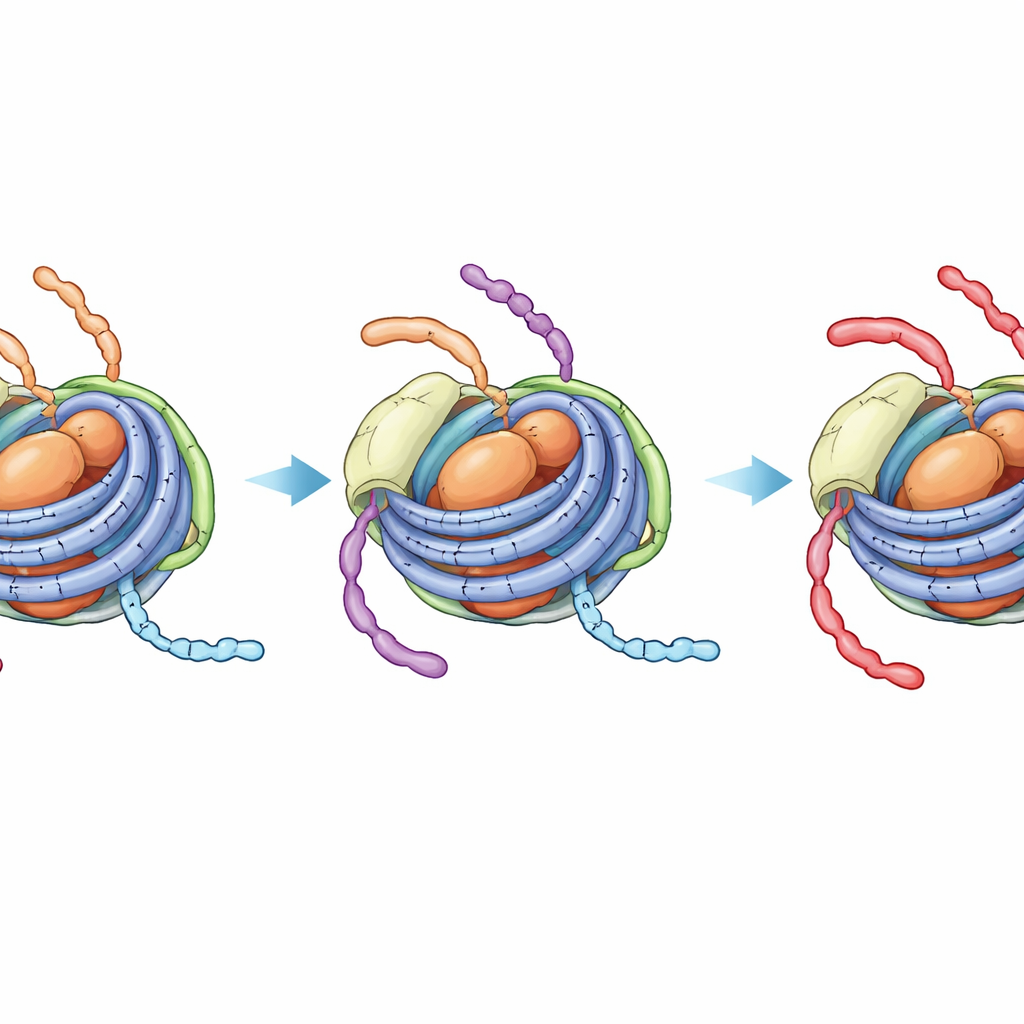
Un estado oculto y más apretado que bloquea cambios adicionales
La RMN, que detecta el entorno local de átomos específicos, reveló un efecto más llamativo. En los cromatosomas no modificados, las señales de la cola H3 muestran una mezcla de dos estados dinámicos—uno que se parece al nucleosoma más abierto (con contacto con el ADN de enlace) y otro que recuerda a la partícula más compacta del nucleosoma solo con el núcleo. En la escala temporal de una reacción enzimática, estos estados se intercambian, por lo que la enzima que acetila la posición K14 en la cola de H3 aún puede acceder a los segmentos expuestos al ADN de enlace. En contraste, cuando la cola de H4 porta cuatro grupos acetilo y H1 está presente, las señales de la cola H3 colapsan en un único estado robusto que se asemeja a la forma firmemente ligada al ADN del núcleo. La monitorización directa por RMN de la reacción de acetilación confirmó que la K14 de H3 entonces se modifica mucho más lentamente, a una velocidad casi indistinguible de la del nucleosoma cerrado sin ningún ADN de enlace.
Qué significa esto para los interruptores de encendido/apagado génicos
En conjunto, los resultados sugieren que la acetilación de la cola de H4, en presencia de la histona de enlace H1, paradójicamente ayuda a bloquear las colas vecinas de H3 contra el ADN del núcleo en lugar de liberarlas para cambios adicionales. Al promover este estado estable y abrazador del ADN y ralentizar mucho la acetilación adicional de H3, H1 parece contrarrestar la expansión de cromatina abierta y activa y, en su lugar, favorecer regiones más compactas y silenciosas. En términos cotidianos, el estudio muestra que un conjunto de marcas químicas y una sola proteína adicional pueden decidir si tramos cercanos de ADN permanecen abiertos para la actividad o se pliegan para almacenamiento a largo plazo, añadiendo una nueva capa de comprensión sobre cómo las células preservan su identidad a lo largo del tiempo.
Cita: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Palabras clave: estructura de la cromatina, acetilación de histonas, histona de enlace H1, dinámica del nucleosoma, regulación epigenética