Clear Sky Science · ja
リンカーヒストンH1はH4テールのアセチル化によって誘導されるH3テールのアセチル化を抑制し、その動態を変える
なぜ小さなタンパク質のテールがDNAに重要なのか
すべての細胞の内部では、ほぼ二メートルのDNAが微小な核内に折りたたまれて収められています。この折りたたみはヒストンと呼ばれるタンパク質のスプールによって担われ、どの遺伝子がオンになるかオフになるかを決める助けをしています。本研究は、これらヒストンに付く小さな化学的タグと、リンカーヒストンH1という別のタンパク質がどのように協働してDNAを開いて遺伝子発現を可能にするか、あるいは閉じて抑制するかを探りました。このバランスを理解することは、細胞がどのようにして長期にわたりどの遺伝子を活性または不活性として記憶するかを解き明かす手がかりになります。
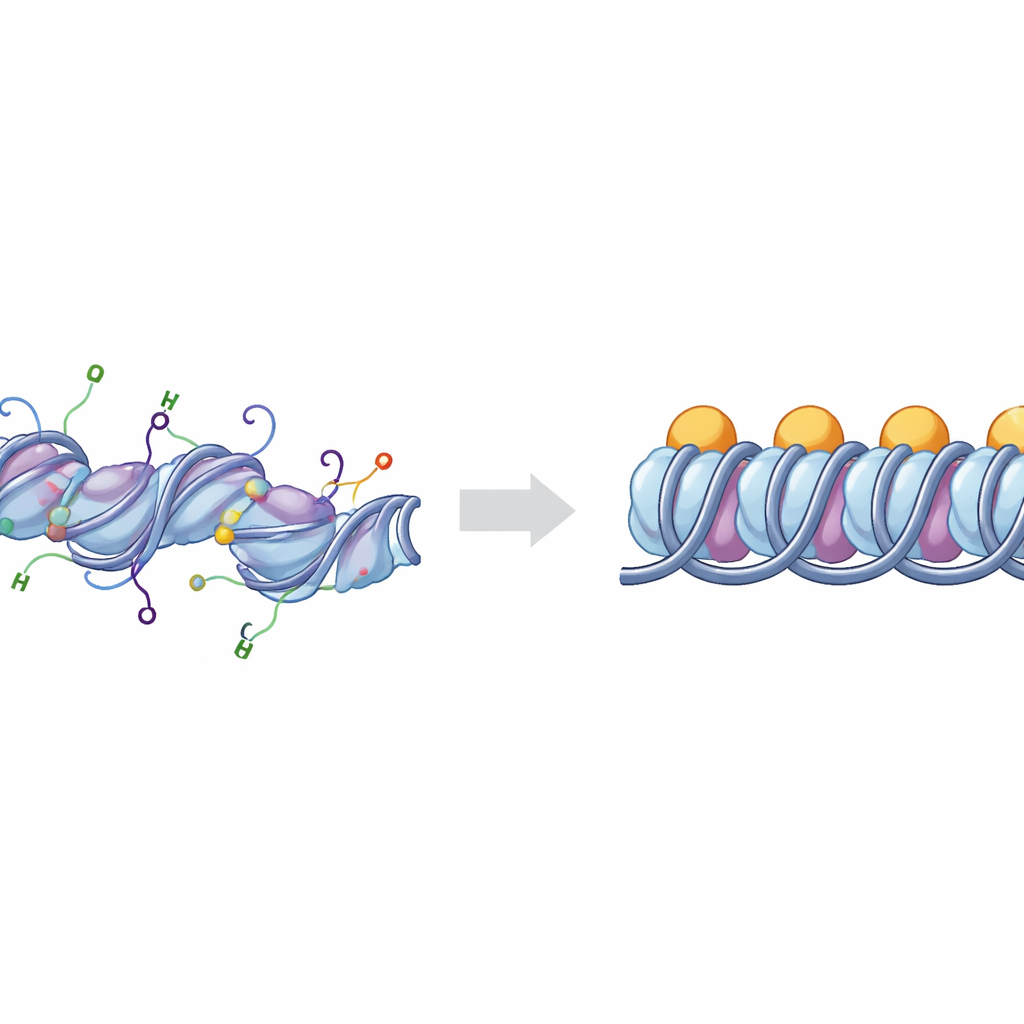
DNA収納の基本ブロック
染色体中のDNAはヒストンタンパク質のクラスターに巻き付いてヌクレオソームという単位を形成します。そこにさらにリンカーヒストンH1が、DNAがヌクレオソームに出入りする位置に結合すると、その構造はクロマトソームと呼ばれます。クロマトソームが連なって折りたたまれると、一般に活性の低い高密度の領域が作られます。細胞はヒストンから伸びる柔軟な「テール」に付けられる化学的マークでこの収納状態を微調整します。特に重要なのがH3とH4のテールで、これらの化学変化は領域が活性で開いた「ユークロマチン」か、沈黙して凝縮した「ヘテロクロマチン」かに強く関連しています。
一方のテールの変化がもう一方にどう影響するか
以前の研究は、H4テールに4つのアセチル基が付く(総称してH4‑4Kac)と、隣接するH3テールもアセチル化されやすくなる傾向があることを示していましたが、これは主にリンカーヒストンH1の不在下で調べられていました。本研究では、より生理的な状況であるH1存在下で何が起きるかを問いました。クライオ電子顕微鏡を用いて、アセチル化されたH4テールを持つクロマトソームの高解像度構造を解明したところ、驚くべきことにコアのDNAとヒストン蛋白の全体形状は非修飾のクロマトソームとほとんど変わりませんでした。H1は依然として同じ中心位置に座し、巻き付いたDNAもほぼ同一に見えたため、重要な効果は可動なヒストンテールの動きやDNAとの接触の変化から生じるに違いないことが示唆されました。
シミュレーションと磁気で動く部品を追う
こうした素早く微妙な運動をとらえるために、研究チームは計算機シミュレーションと核磁気共鳴(NMR)分光を組み合わせました。粗視化分子動力学シミュレーションで、H3およびH4のテールが巻き付いたDNAやヌクレオソームをつなぐ露出したリンカーDNAにどのように触れるかをモデル化しました。クロマトソームでは、H1の存在が自然に二本のH3テールに非対称性を生じさせます:一方は主にコアに巻き付くDNAに接触し、もう一方は露出したリンカーDNAにも接触します。H4がアセチル化されると、そのテールはDNAから剥がれやすくなり、より柔軟で溶媒に露出した状態になります。この放出はH1の長いテールやH3テールがDNA表面を探索する様子をわずかにシフトさせますが、シミュレーションでは接触パターンの平均的な変化は控えめであることが示唆されました。
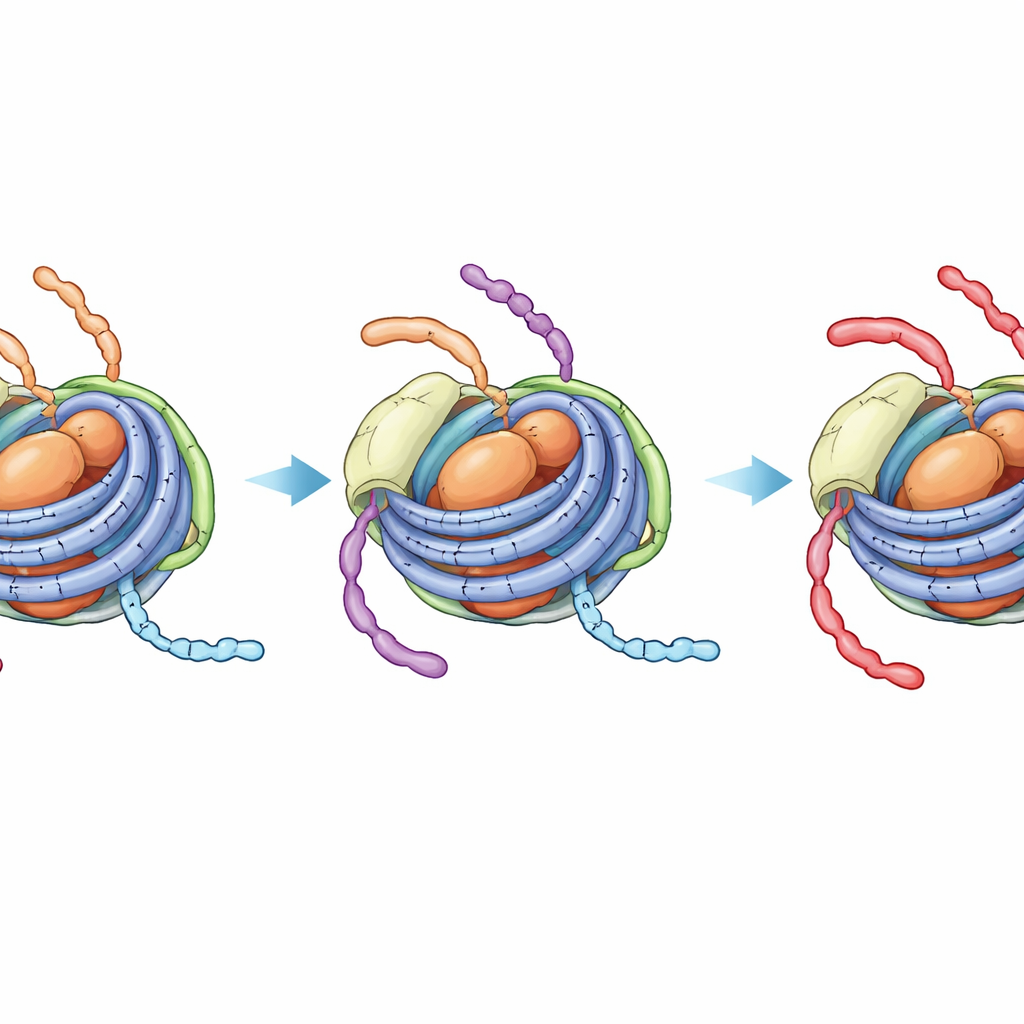
さらに変化を阻む隠れた、より緊密な状態
特定の原子の局所環境を感知するNMR分光は、より際立った効果を明らかにしました。非修飾のクロマトソームでは、H3テールからの信号は二つの動的状態の混合を示します—リンカーDNAと接触するより開いたヌクレオソームに似た状態と、コアのみと結合したより緊密なヌクレオソーム粒子に似た状態です。酵素反応の時間スケールではこれらの状態は入れ替わるため、H3テールのK14位置をアセチル化する酵素はリンカーに露出したセグメントにまだアクセスできます。対照的に、H4テールに4つのアセチル基がありH1が存在すると、H3テールの信号は単一で頑健な状態に収束し、コアDNAに密着した緊密な形に似たものになります。アセチル化反応をNMRで直接追跡すると、H3 K14の修飾は著しく遅くなり、リンカーDNAが全くない閉じたヌクレオソームコアの場合とほとんど区別できない速度になることが確認されました。
遺伝子のオン/オフスイッチにとっての意味
総合すると、H4テールのアセチル化はリンカーヒストンH1の存在下で隣接するH3テールを解放するのではなく、逆にコアDNAに密着させて固定するのを助ける、という逆説的な効果を示唆します。この安定したDNAに抱きつく状態を促進し、H3のさらなるアセチル化を著しく遅らせることで、H1は開いた活性クロマチンの広がりに対抗し、むしろより凝縮した不活性領域を好むように見えます。日常的に言えば、この研究は一連の化学的マークと一つの追加タンパク質が、近傍のDNA領域を活動的に保つか長期保存のために折りたたむかを決めることができると示しており、細胞が時間を超えて自己の同一性を保持する仕組みに新たな層での理解を加えます。
引用: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
キーワード: クロマチン構造, ヒストンのアセチル化, リンカーヒストンH1, ヌクレオソームのダイナミクス, エピジェネティック制御