Clear Sky Science · pt
Histona ligadora H1 reprime a acetilação da cauda de H3 induzida pela acetilação da cauda de H4 e altera sua dinâmica
Por que pequenas caudas protéicas importam para o nosso DNA
Dentro de cada célula, quase dois metros de DNA são compactados em um núcleo microscópico. Essa façanha de dobramento é gerida por carretéis de proteínas chamados histonas, que ajudam a decidir se genes são ativados ou reprimidos. O novo estudo investigou como pequenas marcas químicas nessas histonas, e a presença de outra proteína chamada histona ligadora H1, atuam em conjunto para abrir o DNA para atividade gênica ou mantê‑lo bloqueado. Entender esse equilíbrio esclarece como as células preservam a memória de longo prazo sobre quais genes devem permanecer ativos ou silenciosos.
Os blocos básicos do empacotamento do DNA
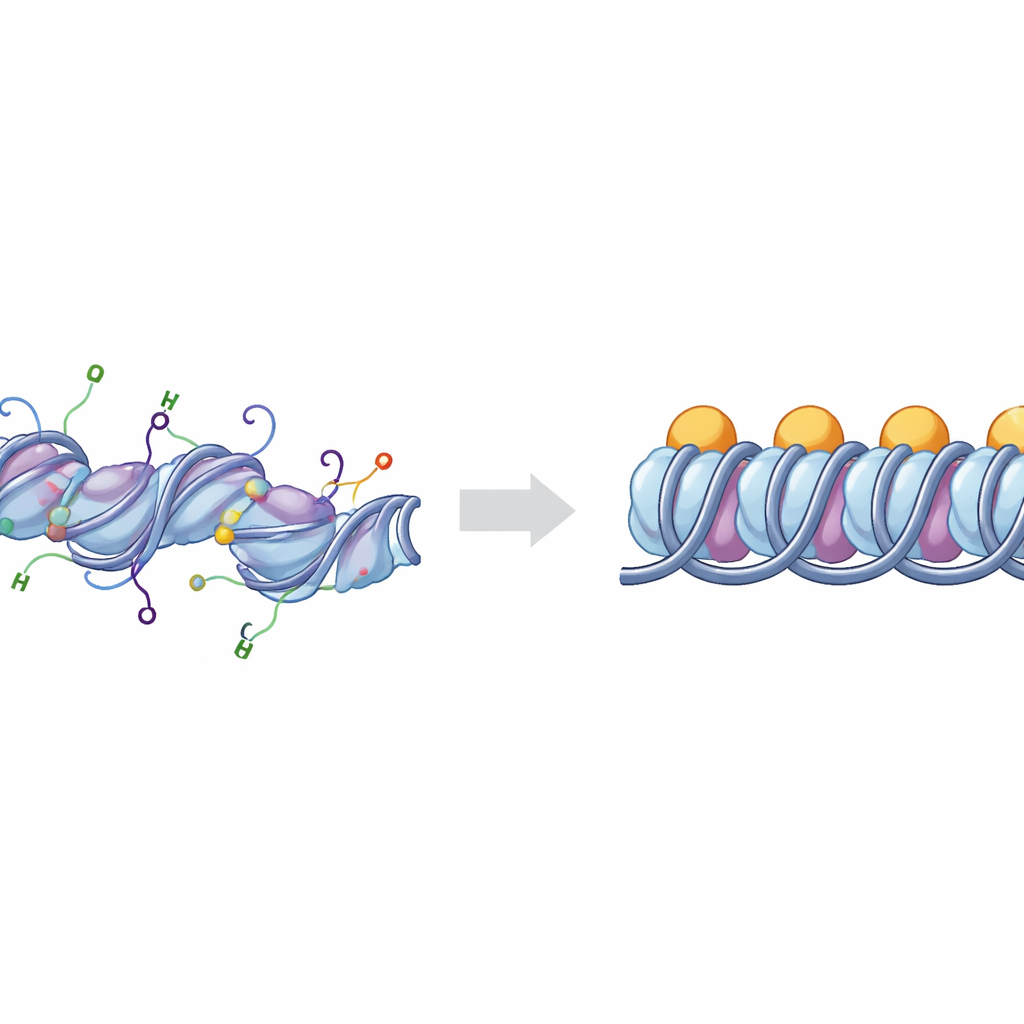
O DNA em nossos cromossomos enrola‑se ao redor de aglomerados de proteínas histonas para formar unidades conhecidas como nucleossomos. Quando uma proteína adicional, a histona ligadora H1, se liga nos pontos onde o DNA entra e sai do nucleossomo, a estrutura é chamada de cromatossomo. Grupos de cromatossomos podem empilhar‑se e dobrar‑se para criar regiões de DNA fortemente compactadas que, em geral, são menos ativas. As células ajustam finamente esse empacotamento com marcas químicas colocadas nas “caudas” flexíveis que se estendem das histonas. Duas das caudas mais importantes pertencem às histonas H3 e H4, cujas modificações químicas estão fortemente ligadas ao comportamento das regiões de DNA como eucromatina aberta e ativa ou heterocromatina compacta e silenciosa.
Como a mudança de uma cauda afeta outra
Trabalhos anteriores mostraram que adicionar quatro grupos acetil ao terminal de H4 — em posições conhecidas coletivamente como H4‑4Kac — tende a tornar a cauda vizinha H3 mais fácil de acetilar também, mas isso foi estudado principalmente sem a histona ligadora H1. A nova pesquisa perguntou o que acontece quando H1 está presente, uma situação mais realista nas células vivas. Usando criomicroscopia eletrônica, os autores resolveram estruturas de alta resolução de cromatossomos carregando a cauda de H4 acetilada. Surpreendentemente, a forma geral do DNA central e das proteínas histonas permaneceu quase inalterada em comparação com cromatossomos não modificados. A proteína H1 continuou situada na mesma posição central, e o DNA enrolado parecia quase idêntico, sugerindo que os efeitos importantes devem surgir de mudanças em como as caudas flexíveis das histonas se movem e tocam o DNA.
Seguindo partes móveis com simulações e ímãs
Para capturar esses movimentos rápidos e sutis, a equipe combinou simulações computacionais com espectroscopia de ressonância magnética nuclear (RMN). Simulações de dinâmica molecular em nível grosseiro modelaram como as caudas de H3 e H4 roçam o DNA enrolado e os trechos extras de DNA que ligam nucleossomos entre si. Em cromatossomos, a presença de H1 naturalmente faz com que as duas caudas de H3 se comportem de forma diferente: uma tende a tocar principalmente o DNA enrolado no núcleo, enquanto a outra também estabelece contato com o DNA exposto de ligação. Quando H4 é acetilada, sua própria cauda se desprende do DNA, tornando‑se mais flexível e exposta ao solvente. Essa liberação desloca ligeiramente a forma como tanto a longa cauda de H1 quanto as caudas de H3 exploram a superfície do DNA, mas as simulações sugeriram apenas mudanças médias modestas nos padrões de contato.
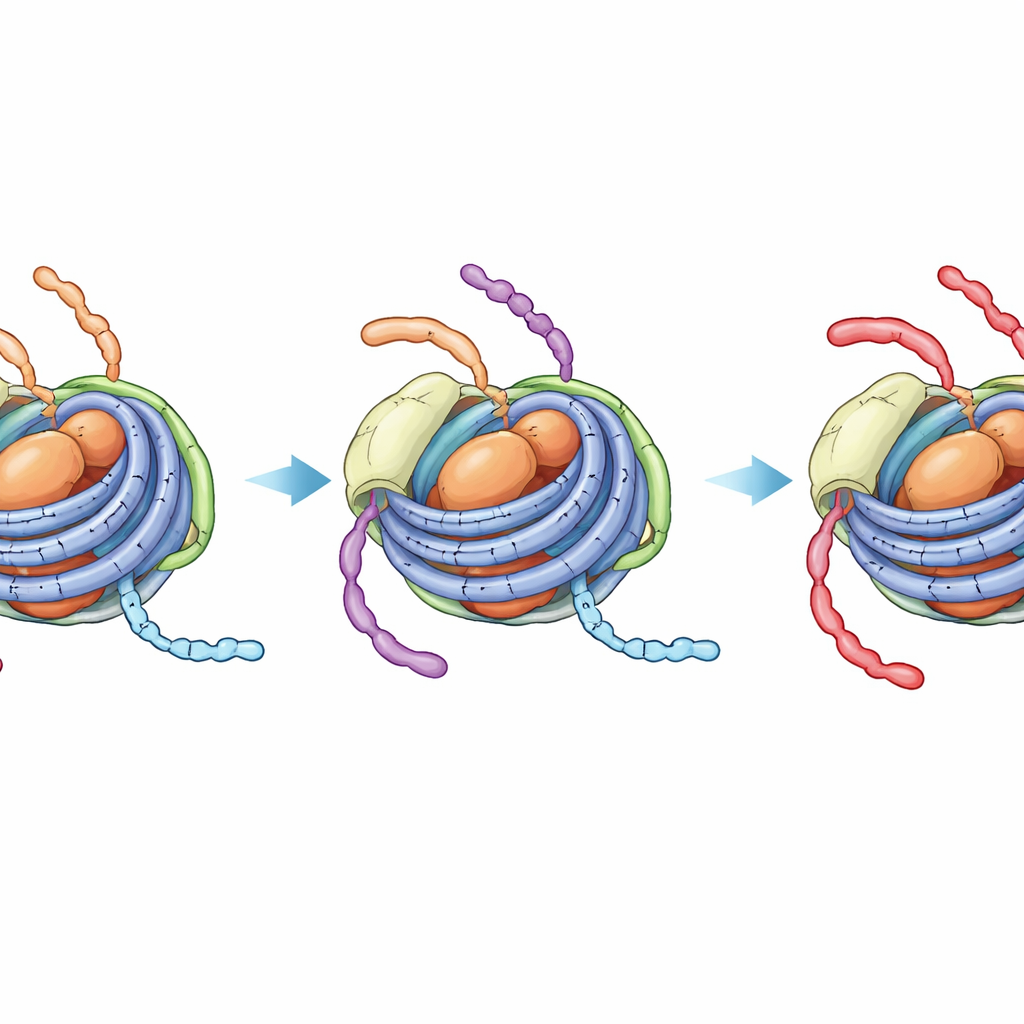
Um estado oculto e mais apertado que bloqueia alterações adicionais
A espectroscopia de RMN, que detecta o ambiente local de átomos específicos, revelou um efeito mais marcante. Em cromatossomos não modificados, sinais da cauda de H3 mostram uma mistura de dois estados dinâmicos — um assemelhado ao nucleossomo mais aberto (com contato ao DNA ligador) e outro parecido com a partícula de nucleossomo mais fechada, apenas com o núcleo. Na escala de tempo de uma reação enzimática, esses estados se alternam, de modo que a enzima que acetila a posição K14 na cauda de H3 ainda pode acessar segmentos expostos ao DNA ligador. Em contraste, quando a cauda de H4 carrega quatro acetilas e H1 está presente, os sinais da cauda de H3 colapsam em um único estado robusto que se parece com a forma fortemente ligada ao DNA do núcleo. Monitoramento direto por RMN da reação de acetilação confirmou que H3 K14 é então modificado muito mais lentamente, a uma taxa quase indistinguível daquela do núcleo fechado do nucleossomo sem qualquer DNA ligador.
O que isso significa para os interruptores liga/desliga de genes
Tomados em conjunto, os resultados sugerem que a acetilação da cauda de H4, na presença da histona ligadora H1, paradoxalmente ajuda a prender as caudas vizinhas de H3 contra o DNA do núcleo em vez de liberá‑las para alterações adicionais. Ao promover esse estado estável de abraço ao DNA e desacelerar muito a acetilação adicional de H3, H1 parece contrariar a propagação de cromatina aberta e ativa e, em vez disso, favorecer regiões mais compactas e silenciosas. Em termos cotidianos, o estudo mostra que um conjunto de marcas químicas e uma única proteína adicional podem decidir se trechos próximos de DNA permanecem abertos para uso ou são dobrados para armazenamento de longo prazo, adicionando uma nova camada de compreensão sobre como as células preservam sua identidade ao longo do tempo.
Citação: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Palavras-chave: estrutura da cromatina, acetilação de histonas, histona ligadora H1, dinâmica do nucleossomo, regulação epigenética