Clear Sky Science · de
Linker-Histon H1 unterdrückt durch H4-Schwanz induzierte H3-Schwanz-Acetylierung und verändert dessen Dynamik
Warum winzige Proteinschwänze für unsere DNA wichtig sind
In jeder Zelle sind fast zwei Meter DNA in einem mikroskopisch kleinen Zellkern verpackt. Dieses Faltkunststück erledigen Spulen aus Proteinen, sogenannte Histone, die mitentscheiden, ob Gene ein‑ oder ausgeschaltet werden. Die neue Studie untersuchte, wie kleine chemische Markierungen an diesen Histonen und die Anwesenheit eines weiteren Proteins, des Linker‑Histons H1, zusammenwirken, um DNA entweder für Genaktivität zu öffnen oder verschlossen zu halten. Das Verständnis dieses Gleichgewichts wirft Licht darauf, wie Zellen langfristig speichern, welche Gene aktiv oder stumm bleiben sollen.
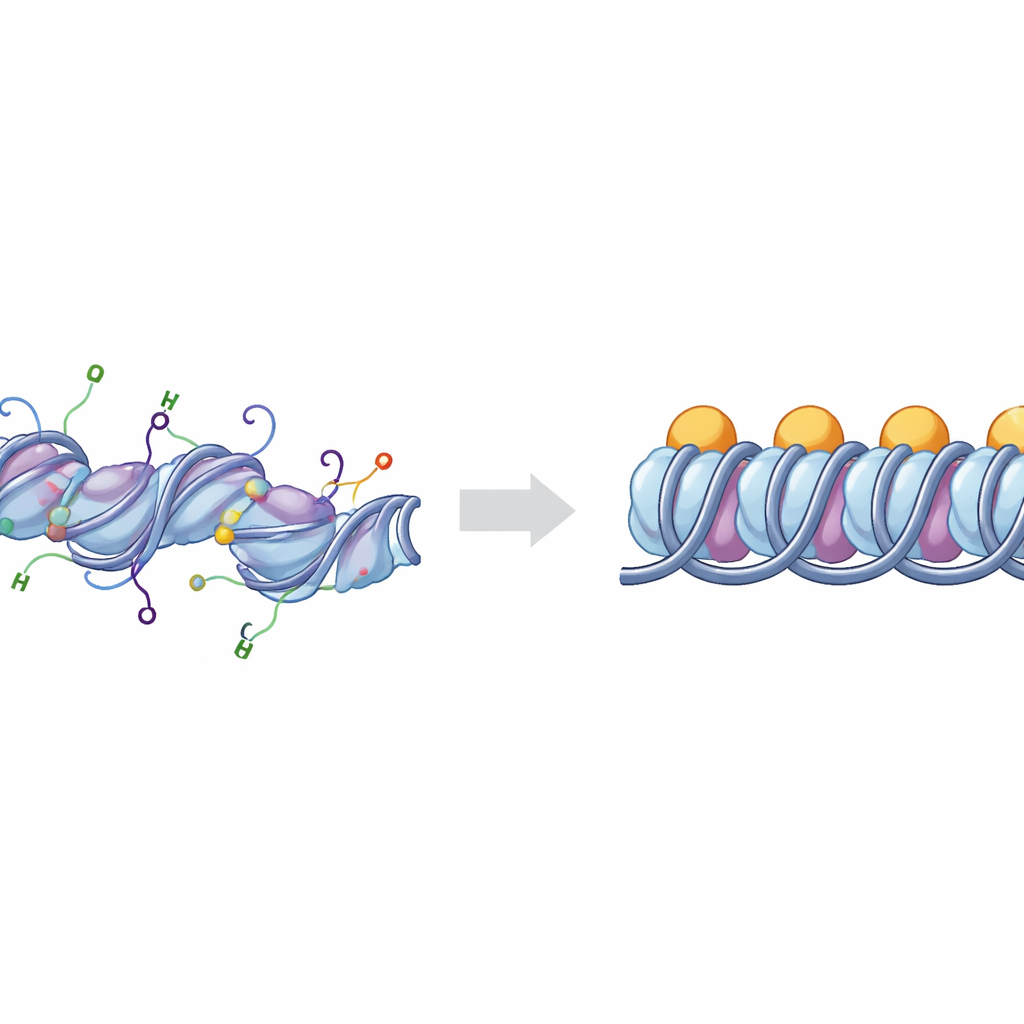
Die grundlegenden Bausteine der DNA‑Verpackung
Die DNA in unseren Chromosomen ist um Cluster von Histonproteinen aufgewickelt und bildet Einheiten, die als Nukleosomen bekannt sind. Wenn ein zusätzliches Protein, das Linker‑Histon H1, an den Stellen bindet, an denen die DNA in das Nukleosom eintritt und es verlässt, spricht man von einem Chromatosom. Gruppen von Chromatosomen können sich stapeln und falten, um dicht gepackte Bereiche der DNA zu bilden, die in der Regel weniger aktiv sind. Zellen justieren diese Verpackung mit chemischen Markierungen an flexiblen „Schwänzen“, die von den Histonen ausgehen. Zwei der wichtigsten Schwänze gehören zu den Histonen H3 und H4; deren chemische Veränderungen stehen in engem Zusammenhang damit, ob DNA‑Regionen als offene, aktive „Euchromatin“ oder als stille, kompakte „Heterochromatin“ auftreten.
Wie die Veränderung eines Schwanzes den anderen beeinflusst
Frühere Arbeiten zeigten, dass das Anhängen von vier Acetylgruppen an den H4‑Schwanz — an Positionen, die zusammen als H4‑4Kac bezeichnet werden — dazu neigt, den benachbarten H3‑Schwanz ebenfalls leichter acetylierbar zu machen; diese Untersuchungen erfolgten jedoch überwiegend ohne das Linker‑Histon H1. Die neue Forschung fragte, was passiert, wenn H1 vorhanden ist — ein realistischeres Szenario in lebenden Zellen. Mithilfe der Kryo‑Elektronenmikroskopie lösten die Autoren hochaufgelöste Strukturen von Chromatosomen mit acetylierter H4‑Schwanzsequenz auf. Überraschenderweise blieb die Gesamtgestalt der Kern‑DNA und der Histonproteine im Vergleich zu unveränderten Chromatosomen nahezu unverändert. Das H1‑Protein saß weiterhin an derselben zentralen Position, und die umwickelte DNA sah fast identisch aus. Das deutet darauf hin, dass wichtige Effekte eher von Änderungen in der Beweglichkeit der flexiblen Histonschwänze und deren Kontakten zur DNA ausgehen müssen.
Verfolgung beweglicher Teile mit Simulationen und Magneten
Um diese schnellen, subtilen Bewegungen einzufangen, kombinierte das Team Computersimulationen mit kernmagnetischer Resonanzspektroskopie (NMR). Grobkörnige Molekulardynamik‑Simulationen modellierten, wie die H3‑ und H4‑Schwänze die umwickelte DNA und die zusätzlichen DNA‑Abschnitte, die Nukleosomen verbinden, streifen. In Chromatosomen bewirkt die Anwesenheit von H1 auf natürliche Weise, dass sich die beiden H3‑Schwänze unterschiedlich verhalten: Der eine berührt überwiegend die kernumwickelte DNA, während der andere zusätzlich Kontakt zur exponierten Linker‑DNA hat. Wenn H4 acetymiert ist, löst sich dessen eigener Schwanz von der DNA, wird flexibler und stärker dem Lösungsmittel ausgesetzt. Diese Freisetzung verschiebt leicht, wie sowohl H1s langer Schwanz als auch die H3‑Schwänze die DNA‑Oberfläche erkunden, doch die Simulationen deuteten nur auf mäßige durchschnittliche Änderungen in den Kontaktmustern hin.
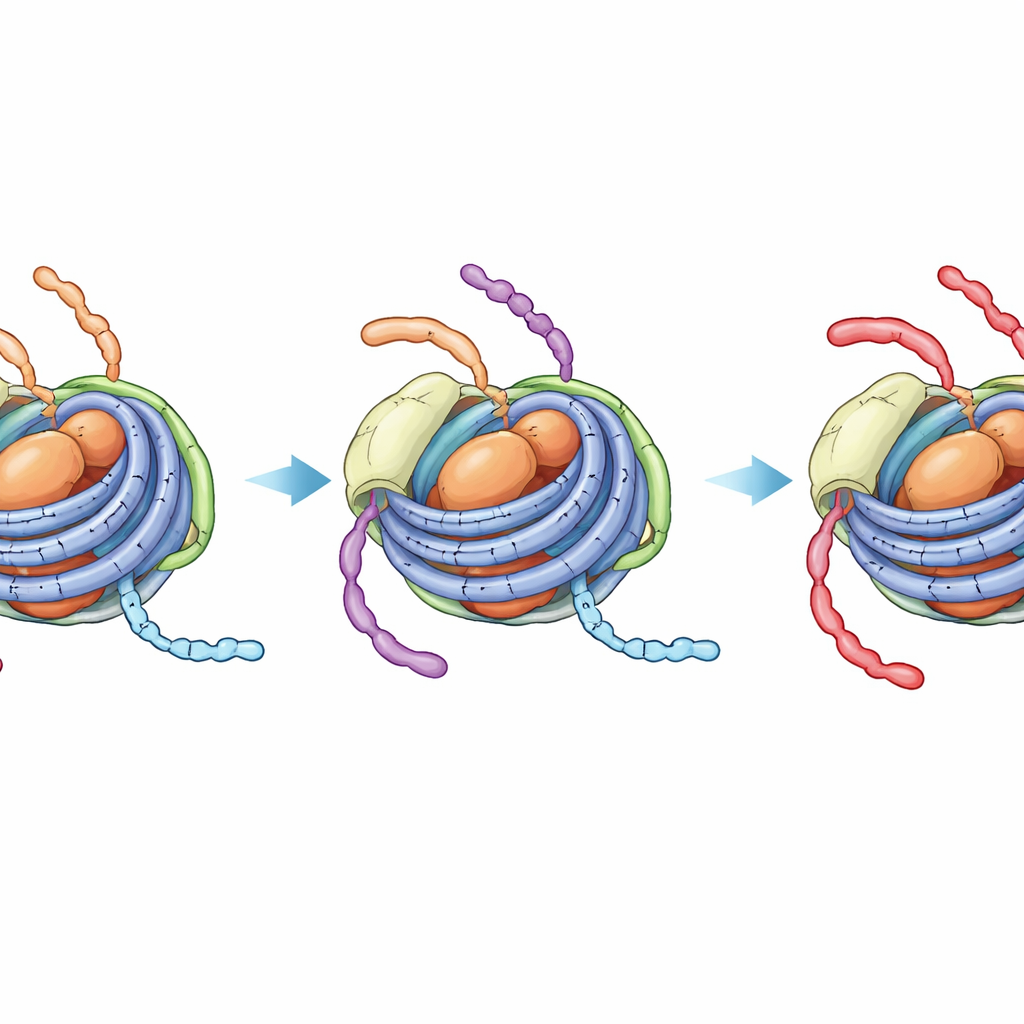
Ein verborgener, enger Zustand, der weitere Veränderungen blockiert
Die NMR‑Spektroskopie, die die lokale Umgebung bestimmter Atome wahrnimmt, zeigte einen markanteren Effekt. In unveränderten Chromatosomen zeigen Signale des H3‑Schwanzes eine Mischung aus zwei dynamischen Zuständen — einen, der dem offeneren Nukleosom ähnelt (mit Kontakt zur Linker‑DNA), und einen, der dem dichteren, nur aus dem Kern bestehenden Nukleosompartikel entspricht. Auf der Zeitskala einer Enzymreaktion wechseln diese Zustände einander ab, sodass das Enzym, das die Position K14 am H3‑Schwanz acetylieren kann, weiterhin auf linkerseitig exponierte Segmente zugreifen kann. Im Gegensatz dazu kollabieren bei vierfach acetyliertem H4‑Schwanz und Anwesenheit von H1 die H3‑Schwanzsignale zu einem einzigen, stabilen Zustand, der dem eng anliegenden Kern‑DNA‑Form ähnelt. Direkte NMR‑Beobachtungen der Acetylierungsreaktion bestätigten, dass H3 K14 dann wesentlich langsamer modifiziert wird — mit einer Rate, die kaum noch von der in einem geschlossenen Nukleosomkern ohne jegliche Linker‑DNA zu unterscheiden ist.
Was das für Ein/Aus‑Schalter von Genen bedeutet
In der Summe deuten die Ergebnisse darauf hin, dass die Acetylierung des H4‑Schwanzes in Anwesenheit des Linker‑Histons H1 paradoxerweise dazu beiträgt, die benachbarten H3‑Schwänze an die Kern‑DNA zu binden, anstatt sie für weitere Veränderungen freizugeben. Indem dieser stabile, DNA‑umarmende Zustand gefördert und zusätzliche Acetylierungen an H3 erheblich verlangsamt werden, scheint H1 die Ausbreitung offenen, aktiven Chromatins zu bremsen und stattdessen kompaktere, stille Regionen zu begünstigen. Einfach ausgedrückt zeigt die Studie, dass ein Satz chemischer Markierungen und ein einzelnes zusätzliches Protein darüber entscheiden können, ob benachbarte DNA‑Abschnitte offen und aktiv bleiben oder für die langfristige Speicherung weggefaltet werden — und liefert damit eine neue Einsicht, wie Zellen ihre Identität im Laufe der Zeit bewahren.
Zitation: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Schlüsselwörter: Chromatinstruktur, Histon‑Acetylierung, Linker‑Histon H1, Nukleosomdynamik, epigenetische Regulation