Clear Sky Science · pl
Histon łącznikowy H1 hamuje acetylację ogona H3 wywołaną acetylacją ogona H4 i zmienia jego dynamikę
Dlaczego drobne ogony białkowe mają znaczenie dla naszej DNA
W każdej komórce prawie dwa metry DNA zmieścić trzeba w mikroskopijnym jądrze. To składanie odbywa się dzięki bębenkom białkowym zwanym histonami, które pomagają zdecydować, czy geny są włączone czy wyłączone. Nowe badanie badało, jak małe chemiczne znaczniki na tych histonach oraz obecność innego białka, histonu łącznikowego H1, współdziałają, by albo udostępnić DNA do aktywności genowej, albo utrzymać je w stanie zablokowanym. Zrozumienie tej równowagi wyjaśnia, jak komórki zachowują długoterminową pamięć dotyczącą tego, które geny powinny pozostawać aktywne, a które – ciche.
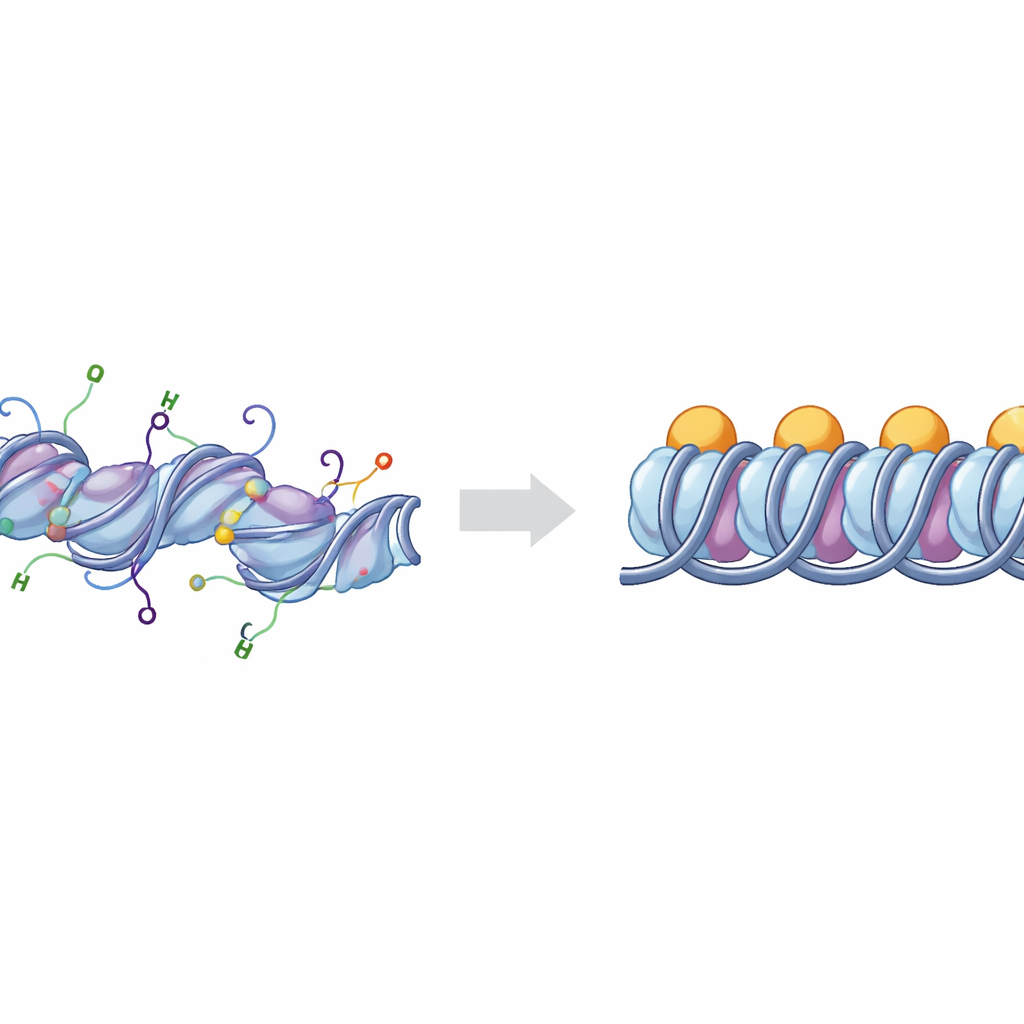
Podstawowe cegiełki upakowania DNA
DNA w naszych chromosomach owinięte jest wokół skupisk białek histonowych, tworząc jednostki znane jako nukleosomy. Gdy dodatkowe białko, histon łącznikowy H1, wiąże się w punktach, gdzie DNA wchodzi i wychodzi z nukleosomu, strukturę tę nazywa się chromatosomem. Grupy chromatosomów mogą się układać i składać, tworząc silnie upakowane regiony DNA, które zwykle są mniej aktywne. Komórki precyzyjnie regulują to upakowanie za pomocą chemicznych znaków umieszczanych na giętkich „ogonach” wystających z histonów. Dwa z najważniejszych ogonów należą do histonów H3 i H4, których modyfikacje chemiczne są silnie powiązane z tym, czy regiony DNA zachowują się jak aktywna, otwarta euchromatyna, czy cicha, zwarta heterochromatyna.
Jak zmiana jednego ogona wpływa na drugi
Wcześniejsze prace pokazały, że dodanie czterech grup acetylowych do ogona H4 — w miejscach zbiorczo nazywanych H4‑4Kac — zwykle ułatwia również acetylację sąsiedniego ogona H3, lecz badania te przeprowadzono głównie bez histonu łącznikowego H1. Nowe badanie pytało, co się dzieje, gdy H1 jest obecny, co jest bardziej realistyczne dla warunków komórkowych. Korzystając z krioelektronowej mikroskopii, autorzy otrzymali struktury chromatosomów z acetylowanym ogonem H4 o wysokiej rozdzielczości. Ku zaskoczeniu, ogólny kształt rdzenia DNA i białek histonowych pozostał prawie niezmieniony w porównaniu z niezmodyfikowanymi chromatosomami. Białko H1 nadal zajmowało tę samą centralną pozycję, a owinięte DNA wyglądało niemal identycznie, co sugeruje, że istotne efekty muszą wynikać ze zmian w ruchliwości giętkich ogonów histonowych i ich oddziaływań z DNA.
Śledzenie ruchomych elementów za pomocą symulacji i magnesów
Aby uchwycić te szybkie, subtelne ruchy, zespół połączył symulacje komputerowe z spektroskopią magnetycznego rezonansu jądrowego (NMR). Gruboskórne symulacje dynamiki molekularnej modelowały, jak ogony H3 i H4 ocierają się o owinięte DNA i dodatkowe odcinki DNA łączące nukleosomy. W chromatosomach obecność H1 naturalnie powoduje, że dwa ogony H3 zachowują się odmiennie: jeden ma tendencję do kontaktu głównie z rdzeniem owiniętego DNA, podczas gdy drugi dodatkowo styka się z odsłoniętym DNA łącznikowym. Gdy H4 jest acetylowany, jego ogon odkleja się od DNA, stając się bardziej elastycznym i wystawionym na rozpuszczalnik. To uwolnienie nieznacznie przesuwa sposób, w jaki zarówno długi ogon H1, jak i ogony H3 eksplorują powierzchnię DNA, ale symulacje sugerowały jedynie umiarkowane średnie zmiany w wzorcach kontaktów.
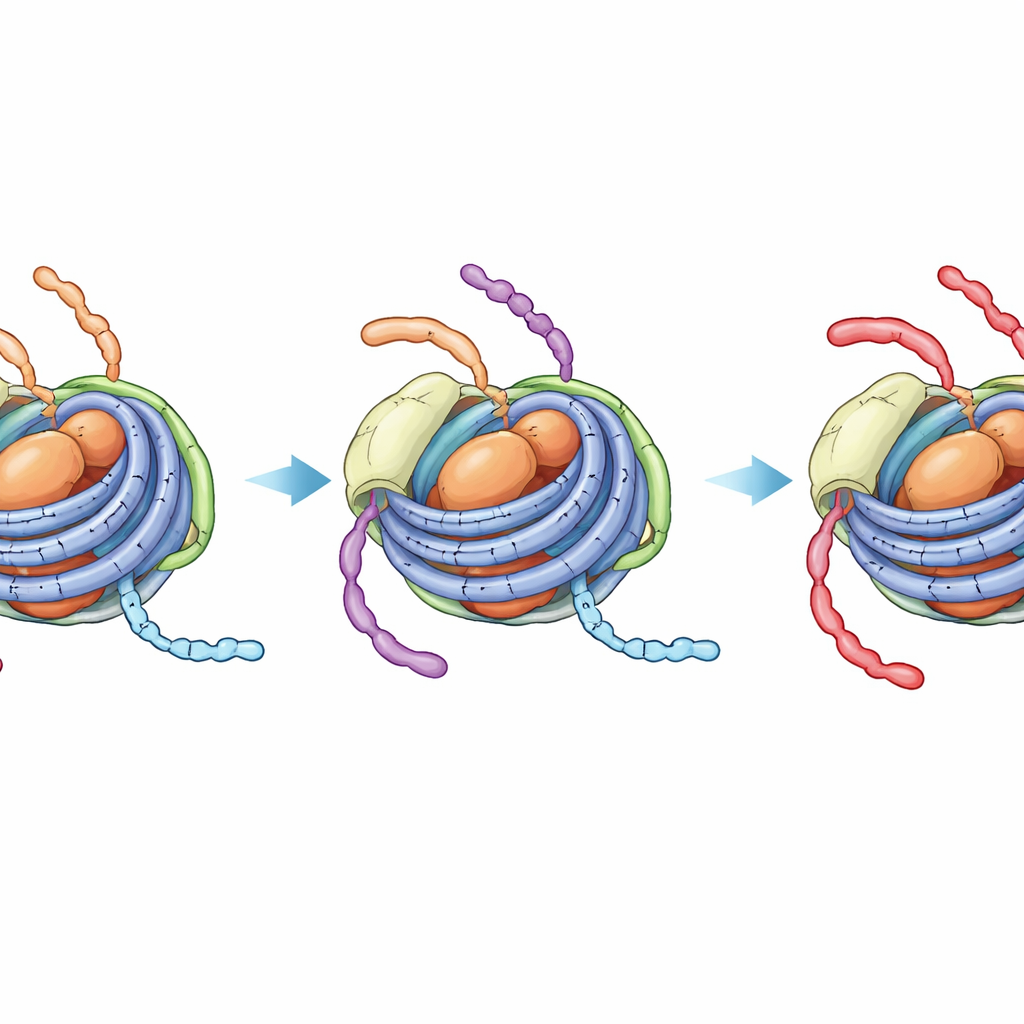
Ukryty, bardziej zwarty stan, który blokuje dalsze zmiany
NMR, który wyczuwa lokalne środowisko konkretnych atomów, ujawnił bardziej uderzający efekt. W niezmodyfikowanych chromatosomach sygnały z ogona H3 pokazują mieszankę dwóch stanów dynamicznych — jeden przypominający bardziej otwarty nukleosom (z kontaktem do DNA łącznikowego) oraz drugi przypominający bardziej zwarty cząsteczkowy rdzeń nukleosomu. W skali czasu reakcji enzymatycznej te stany się przeplatają, więc enzym acetylujący pozycję K14 na ogonie H3 wciąż ma dostęp do odsłoniętych segmentów łącznikowych. Natomiast gdy ogon H4 nosi cztery grupy acetylowe i obecny jest H1, sygnały H3 zlewają się w pojedynczy, wyraźny stan przypominający ciasno związany z rdzeniowym DNA. Bezpośrednie monitorowanie reakcji acetylacji przez NMR potwierdziło, że wtedy modyfikacja H3 K14 przebiega znacznie wolniej, z szybkością niemal nieodróżnialną od zamkniętego rdzenia nukleosomu pozbawionego jakiegokolwiek DNA łącznikowego.
Co to oznacza dla włączników/wyłączników genów
Sumarycznie wyniki sugerują, że acetylacja ogona H4 w obecności histonu łącznikowego H1 paradoksalnie pomaga przycisnąć sąsiednie ogony H3 do rdzeniowego DNA, zamiast je uwalniać do dalszych modyfikacji. Poprzez promowanie tego stabilnego, „przytulonego do DNA” stanu i znaczące spowolnienie dalszej acetylacji H3, H1 wydaje się przeciwdziałać rozprzestrzenianiu się otwartej, aktywnej chromatyny i zamiast tego faworyzować bardziej zwarte, ciche regiony. Mówiąc obrazowo, badanie pokazuje, że jeden zestaw chemicznych znaków i pojedyncze dodatkowe białko mogą zdecydować, czy pobliskie odcinki DNA pozostaną otwarte do działania, czy zostaną złożone na długotrwałe przechowanie, dodając nową warstwę zrozumienia tego, jak komórki zachowują swoją tożsamość w czasie.
Cytowanie: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Słowa kluczowe: struktura chromatyny, acetylacja histonów, histon łącznikowy H1, dynamika nukleosomu, regulacja epigenetyczna