Clear Sky Science · sv
Linkerhiston H1 dämpar H3‑tailsacetylering som induceras av H4‑tailsacetylering och förändrar dess dynamik
Varför små proteintails har betydelse för vårt DNA
Inuti varje cell packas nästan två meter DNA in i en mikroskopisk kärna. Detta veckningsarbete sköts av spolar av proteiner kallade histoner, som hjälper till att avgöra om gener är på eller av. Den nya studien undersökte hur små kemiska markörer på dessa histoner, och närvaron av ett annat protein kallat linkerhiston H1, samverkar för att antingen öppna upp DNA för genaktivitet eller hålla det låst. Att förstå denna balans ger insikt i hur celler bevarar långtidsminnet av vilka gener som ska vara aktiva eller tysta.
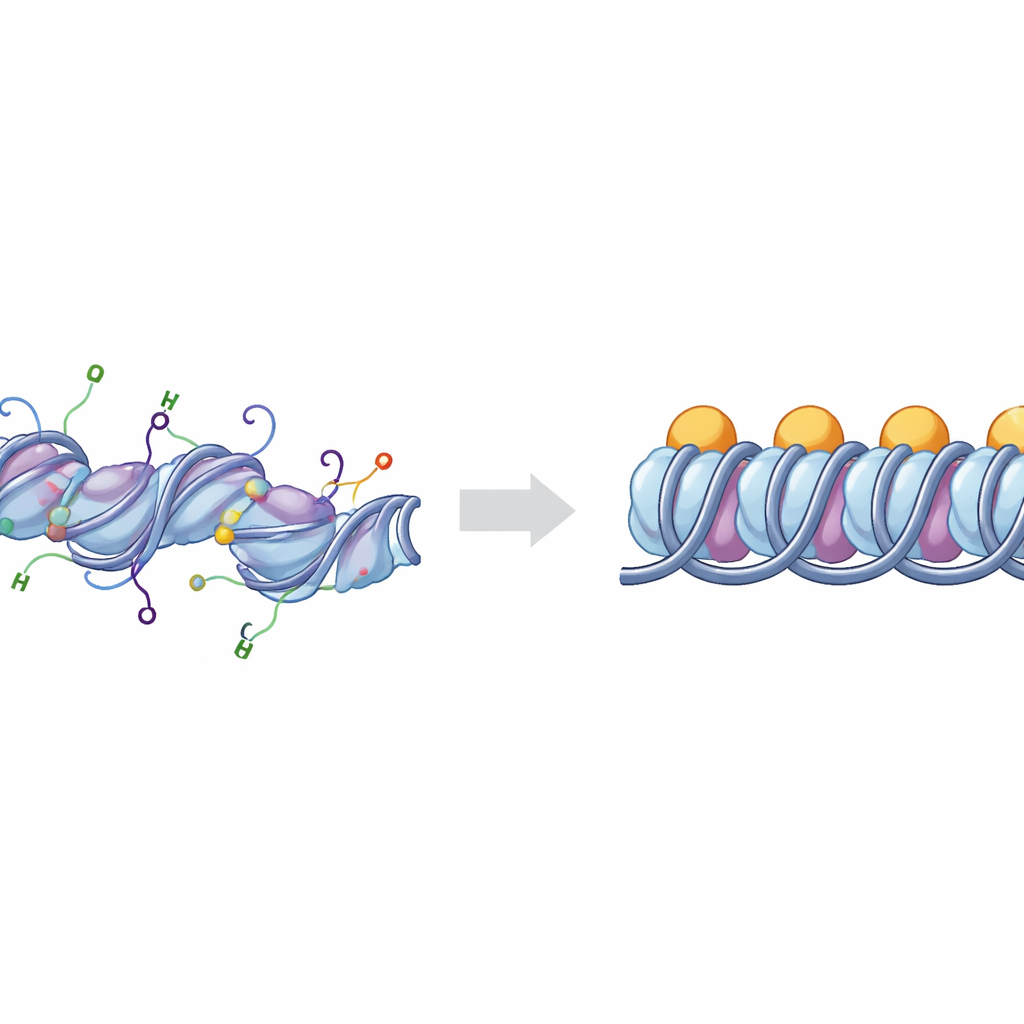
De grundläggande byggstenarna för DNA‑packning
DNA i våra kromosomer är lindat runt kluster av histonproteiner för att bilda enheter kända som nukleosomer. När ett extra protein, linkerhiston H1, binder vid de punkter där DNA går in och ut ur nukleosomen kallas strukturen en kromatosom. Grupper av kromatosomer kan staplas och vikas för att skapa tätt packade DNA‑regioner som i allmänhet är mindre aktiva. Celler finjusterar denna packning med kemiska märken placerade på flexibla ”tails” som sträcker sig från histonerna. Två av de viktigaste tails tillhör histonerna H3 och H4, vars kemiska förändringar starkt kopplas till om DNA‑regioner beter sig som aktiva, öppna euchromatin eller tysta, kompakt heterochromatin.
Hur en tails förändring påverkar en annan
Tidigare arbete visade att tillägg av fyra acetylgrupper på H4‑tailen—på positioner kända kollektivt som H4‑4Kac—tenderar att göra den intilliggande H3‑tailen lättare att acetylera också, men det studerades huvudsakligen utan linkerhiston H1. Den nya forskningen frågade vad som händer när H1 är närvarande, en mer realistisk situation i levande celler. Med hjälp av kryoelektronmikroskopi löste författarna högupplösta strukturer av kromatosomer som bar den acetylerade H4‑tailen. Förvånande nog förblev den övergripande formen hos kärn‑DNA:t och histonproteinerna nästan oförändrad jämfört med omodifierade kromatosomer. H1‑proteinet satt fortfarande på samma centrala position, och det lindade DNA:t såg nära nog identiskt ut, vilket tyder på att eventuella viktiga effekter måste komma från förändringar i hur de rörliga histontailsen rör sig och berör DNA:t.
Att följa rörliga delar med simuleringar och magneter
För att fånga dessa snabba, subtila rörelser kombinerade teamet datorsimuleringar med nukleär magnetresonans (NMR)‑spektroskopi. Grovskalig molekylär dynamiksimulering modellerade hur H3‑ och H4‑tails borstar mot det lindade DNA:t och de extra DNA‑sträckor som länkar nukleosomerna. I kromatosomer gör närvaron av H1 att de två H3‑tailsen naturligt beter sig olika: den ena tenderar att huvudsakligen nå det core‑lindade DNA:t, medan den andra också kontaktar det exponerade linker‑DNA:t. När H4 är acetylerad lossnar dess egen tail från DNA:t, blir mer flexibel och mer exponerad för lösningsmediet. Denna frigörelse förändrar något hur både H1:s långa tail och H3‑tailsen utforskar DNA‑ytan, men simuleringarna antydde bara måttliga genomsnittliga förändringar i kontaktmönstren.
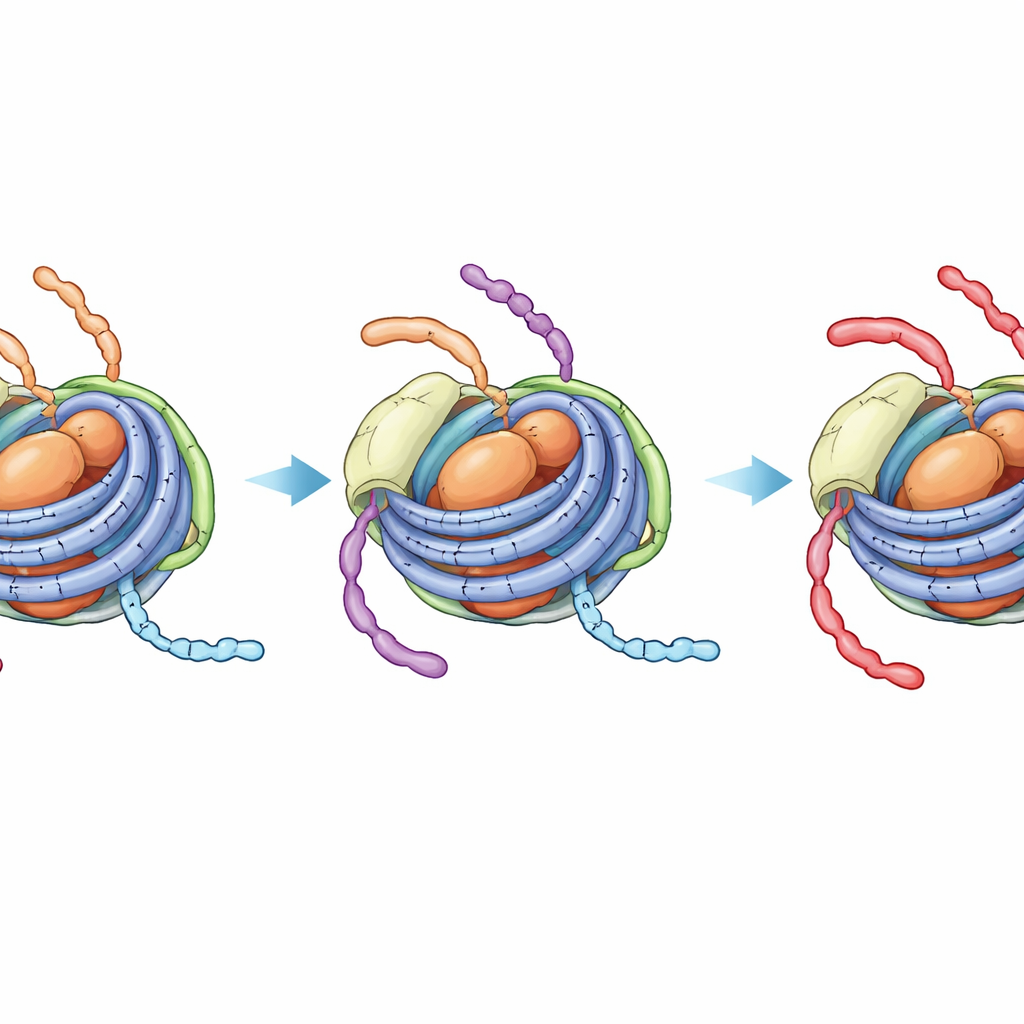
En dold, tätare tillstånd som blockerar vidare förändring
NMR‑spektroskopi, som känner av den lokala miljön kring specifika atomer, avslöjade en mer slående effekt. I omodifierade kromatosomer visar signaler från H3‑tailen en blandning av två dynamiska tillstånd—ett som liknar den mer öppna nukleosomen (med kontakt till linker‑DNA) och ett som liknar den tätare core‑endast nukleosompartikeln. Över tidskalan för en enzymreaktion växlar dessa tillstånd sinsemellan, så enzymet som acetylerar position K14 på H3‑tailen kan fortfarande nå de linker‑exponerade segmenten. I kontrast, när H4‑tailen bär fyra acetylgrupper och H1 är närvarande, kollapsar H3‑tailsignalerna till ett enda, robust tillstånd som ser ut som det tätt bundna core‑DNA‑formatet. Direkt NMR‑övervakning av acetyleringsreaktionen bekräftade att H3 K14 då modifieras mycket långsammare, i en hastighet nästan omöjlig att skilja från den slutna nukleosomkärnan utan något linker‑DNA alls.
Vad detta betyder för geners på/av‑strömbrytare
Tillsammans tyder resultaten på att acetylering av H4‑tailen, i närvaro av linkerhiston H1, paradoxalt nog hjälper till att låsa de intilliggande H3‑tailsen mot core‑DNA i stället för att frigöra dem för vidare förändring. Genom att främja detta stabila, DNA‑kramande tillstånd och avsevärt bromsa ytterligare acetylering av H3, verkar H1 motverka spridningen av öppet, aktivt kromatin och istället gynna mer kompakt, tyst regioner. I enklare termer visar studien att en uppsättning kemiska markörer och ett enda extra protein kan avgöra om närliggande DNA‑sträckor förblir öppna för aktivitet eller viks undan för långtidslagring, vilket lägger till ett nytt lager i förståelsen av hur celler bevarar sin identitet över tid.
Citering: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Nyckelord: kromatinstruktur, histonacetylering, linkerhiston H1, nukleosomdynamik, epigenetisk reglering