Clear Sky Science · he
היסטון קישורי H1 מדכא אצטילציה של זנב H3 שהושרה על ידי אצטילציה של זנב H4 ומשנה את הדינמיקה שלו
מדוע זנבות חלבונים זעירים חשובים ל‑DNA שלנו
בתוך כל תא, כמעט שני מטרים של DNA נארזים בתוך גרעין זעיר. המשימה הזו של קיפול מתבצעת על ידי גלגלות חלבוניות הנקראות היסטונים, שמסייעים לקבוע האם גנים יהיו פעילים או כבויים. המחקר החדש חקר כיצד תגיות כימיות קטנות על היסטונים אלה, ונוכחותו של חלבון נוסף הנקרא היסטון קישורי H1, פועלות יחד כדי לפתוח את ה‑DNA לפעילות גנטית או לשמור אותו נעול. הבנה של האיזון הזה מאירה כיצד תאים שומרים זיכרון ארוך‑טווח של אילו גנים צריכים להישאר פעילים או אילו צריכים להיות שקטים.
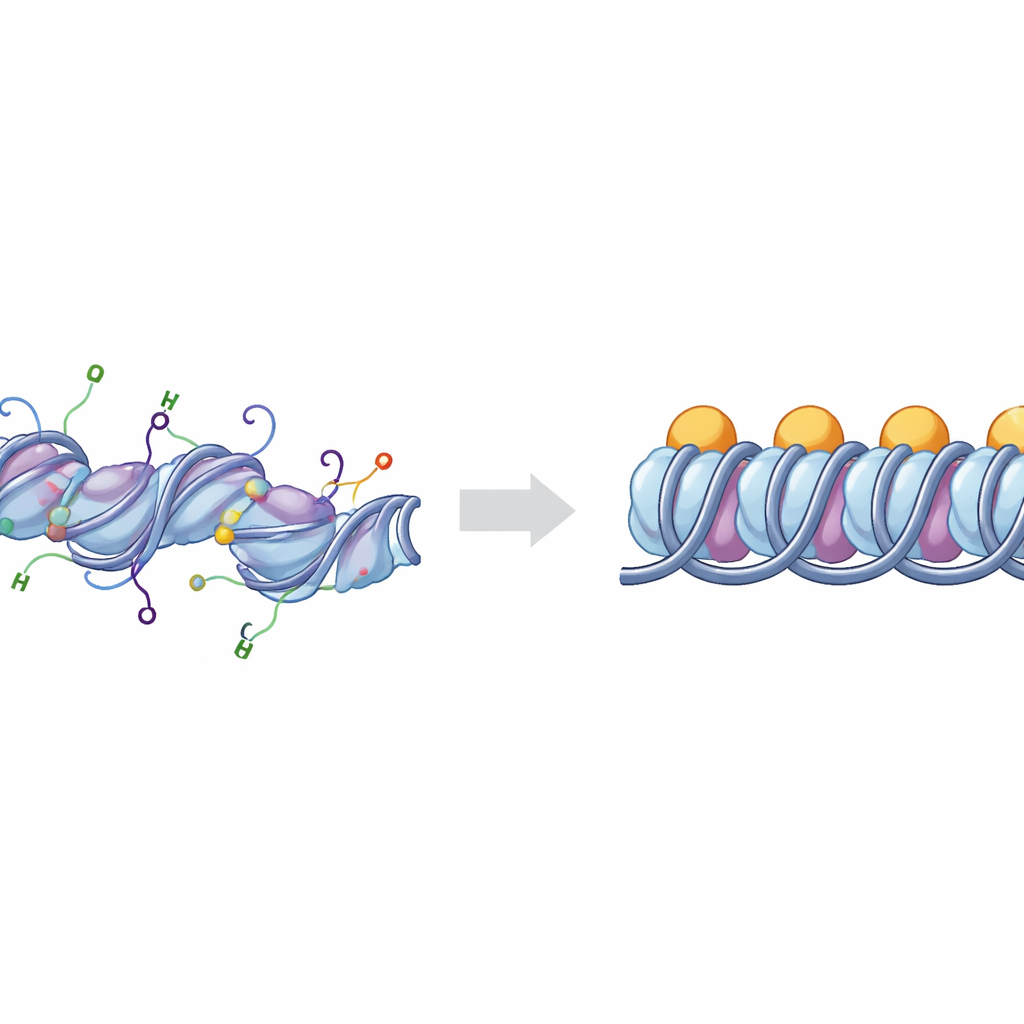
אבני הבנייה הבסיסיות של אריזת ה‑DNA
ה‑DNA בכרומוזומים שלנו מוּלָט סביב אשכולות של חלבוני היסטון כדי ליצור יחידות הידועות כנוקלאוזומים. כאשר חלבון נוסף, היסטון קישורי H1, נקשר בנקודות שבהן ה‑DNA נכנס ויוצא מהנוקלאוזום, המבנה נקרא כרומטוזום. קבוצות של כרומטוזומים יכולות לערום ולהתאחד ליצירת אזורים צפופים של DNA שבדרך‑כלל פחות פעילים. תאים מכוונים את האריזה הזו על‑ידי סימנים כימיים שממוקמים על "זנבות" גמישים שמרחיבים מן ההיסטונים. שניים מהזנבות החשובים ביותר שייכים להיסטונים H3 ו‑H4, ושינויים כימיים בהם מקושרים בעוצמה לקביעה אם אזורי DNA יתנהגו ככרומטין פתוח ופעיל (אאוכרומטין) או ככרומטין דחוס ושקט (הטרוכרומטין).
כיצד שינוי של זנב אחד משפיע על השני
עבודה קודמת הראתה כי הוספת ארבע קבוצות אצטיל לזנב H4 — במיקומים הידועים יחד כ‑H4‑4Kac — נוטה להקל גם על אצטילציה של זנב H3 השכן, אך זה נבדק בעיקר ללא היסטון קישורי H1. המחקר החדש שאל מה קורה בנוכחות H1, מצב מציאותי יותר בתאים חיים. באמצעות מיקרוסקופיית אלקטרונים קרים, החוקרים פתרו מבנים ברזולוציה גבוהה של כרומטוזומים הנושאים את זנב H4 האצטילט. למרבה ההפתעה, הצורה הכוללת של ה‑DNA וההיסטונים הגרעיניים נשארה כמעט ללא שינוי בהשוואה לכרומטוזומים בלתי‑מפורשים. חלבון H1 ישב עדיין באותו מיקום מרכזי, וה‑DNA העטוף נראה כמעט זהה, מה שמרמז שכל ההשפעות החשובות חייבות לנבוע משינויים באופן שבו זנבות ההיסטונים הרכים זזים ונוגעים ב‑DNA.
מעקב אחרי חלקים נעים בעזרת סימולציות ומגנטים
כדי לתפוס תנועות מהירות ומתוחכמות אלה, הצוות שילב סימולציות ממוחשבות עם ספקטרוסקופיית תהודה מגנטית גרעינית (NMR). סימולציות דינמיקה מולקולרית בקנה‑מידה גס דימו כיצד זנבות H3 ו‑H4 משפשפים כנגד ה‑DNA העטוף וכנגד מקטעי ה‑DNA החשופים שמקשרים בין נוקלאוזומים. בכרומטוזומים, נוכחות H1 מטבע הדברים גורמת לשני זנבות H3 להתנהגיות שונות: אחד נוטה לגעת בעיקר ב‑DNA העטוף בליבה, בעוד שהשני יוצר גם מגעים עם ה‑DNA הקישור החשוף. כאשר H4 מאצטל, זנבו מתנתק מעט מה‑DNA, נעשה גמיש יותר וחשוף יותר לממס. השחרור הזה משנה במעט את האופן שבו גם זנב ה‑H1 הארוך וגם זנבות H3 סורקים את פני השטח של ה‑DNA, אבל הסימולציות הציעו ששינויים ממוצעים בדפוסי המגע הם צנועים.
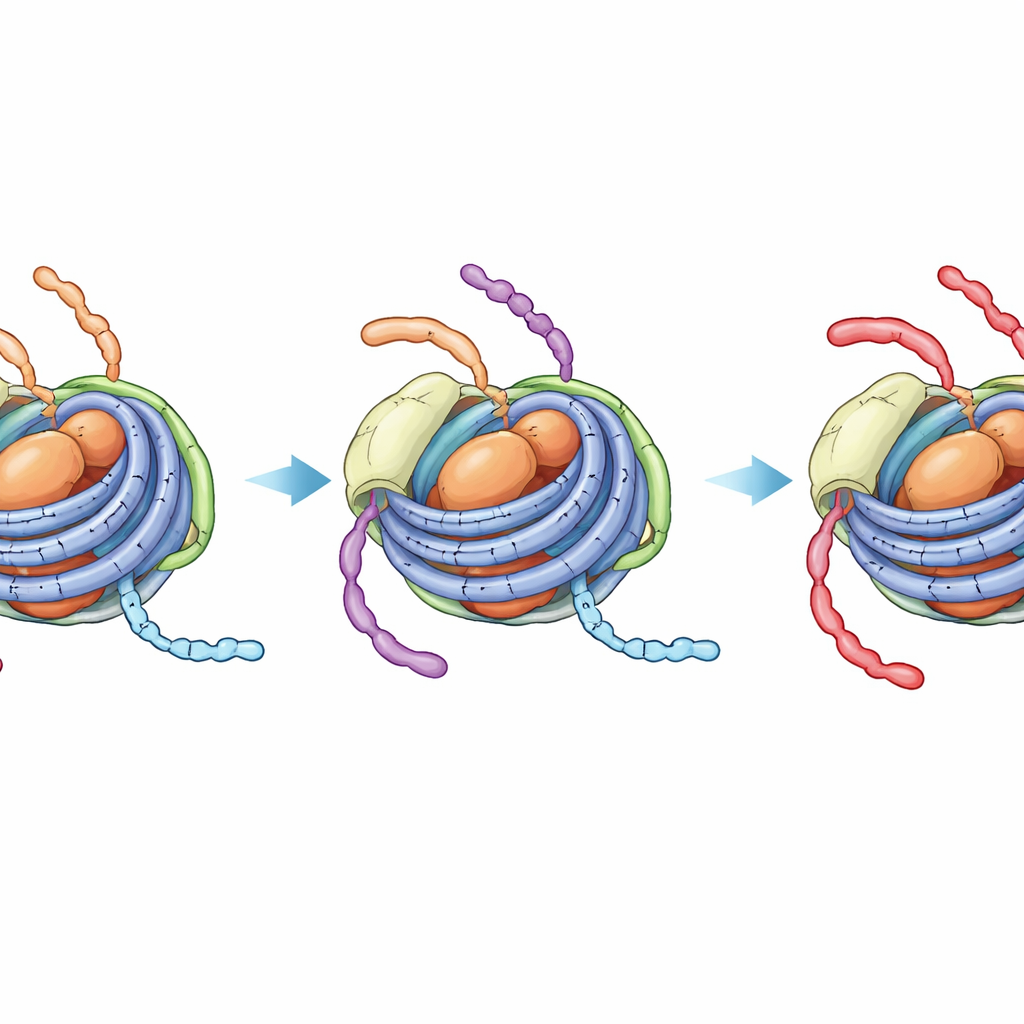
מצב סמוי ומדוקדק שחוסם שינויים נוספים
ספקטרוסקופיית NMR, שמודדת את הסביבה המקומית של אטומים ספציפיים, גילתה אפקט מפתיע יותר. בכרומטוזומים בלתי‑משופרים, האותות מזנב H3 מצביעים על תערובת של שני מצבי דינמיקה — אחד המזכיר את הנוקלאוזום הפתוח יותר (עם מגע ל‑linker DNA) ואחד המזכיר את חלקיק הנוקלאוזום הצפוף יותר שמכיל רק את הליבה. על משך הזמן של תגובת אנזים, המצבים האלה מתחלפים, כך שהאנזים שאצטיל את המיקום K14 על זנב H3 יכול עדיין לגשת למקטעים החשופים ל‑linker. לעומת זאת, כאשר זנב H4 נושא ארבע קבוצות אצטיל ובנוכחות H1, האותות של זנב H3 מתמזגים למצב יחיד וחזק שנראה כמו הצורה הדחוסה הצמודה ל‑DNA של הליבה. מדידה ישירה ב‑NMR של תגובת האצטילציה אישרה כי K14 של H3 מתקבל אז באיטיות רבה בהרבה, בקצב כמעט לא מובדל מהקצב בנוקלאוזום סגור לחלוטין שאין בו DNA קישור בכלל.
מה המשמעות של זה עבור מתגי גנים
במבט כולל, התוצאות מציעות שאצטילציה של זנב H4, בנוכחות היסטון קישורי H1, באופן פרדוקסלי מסייעת לנעול את זנבות H3 השכנים כנגד ה‑DNA של הליבה במקום לשחרר אותם לשינויים נוספים. על‑ידי קידום המצב היציב הזה שמתחבק עם ה‑DNA והאטה משמעותית של אצטילציות נוספות של H3, H1 נראה כגורם שמנוגד להתפשטות של כרומטין פתוח ופעיל ובמקום זאת מעדיף אזורים דחוסים ושקטים. במונחים פשוטים, המחקר מראה שקבוצת סימנים כימיים אחת וחלבון יחיד יכולים להכריע האם מקטעי DNA סמוכים יישארו פתוחים לזמן הקצר או יקופלו לאחסון ארוך‑טווח, ובכך מוסיף שכבה חדשה של הבנה לאופן שבו תאים שומרים על זהותם לאורך זמן.
ציטוט: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
מילות מפתח: מבנה הכרומטין, אצטילציה של היסטונים, היסטון קישורי H1, דינמיקת נוקלאוזומים, ויסות אפיגנטי