Clear Sky Science · ar
الهستون الرابط H1 يكبت أسيتلة ذيل H3 الناشئة عن أسيتلة ذيل H4 ويغير ديناميكياته
لماذا تهم ذيول البروتين الصغيرة حمضنا النووي
داخل كل خلية، يتم ضغط ما يقرب من مترين من الحمض النووي داخل نواة مجهرية. يتحمل لفّ هذا الحمض النووي بروتينات بلفافات تُسمى هستونات، التي تساعد في تقرير ما إذا كانت الجينات مشغلة أم مطفأة. استكشف البحث الجديد كيف تتعاون العلامات الكيميائية الصغيرة على هذه الهستونات، ووجود بروتين آخر يسمى الهستون الرابط H1، لفتح الحمض النووي لنشاط الجين أو إبقائه مغلقًا. فهم هذا التوازن يسلط الضوء على كيفية احتفاظ الخلايا بذاكرة طويلة الأمد حول أي الجينات يجب أن تبقى نشطة أو صامتة.
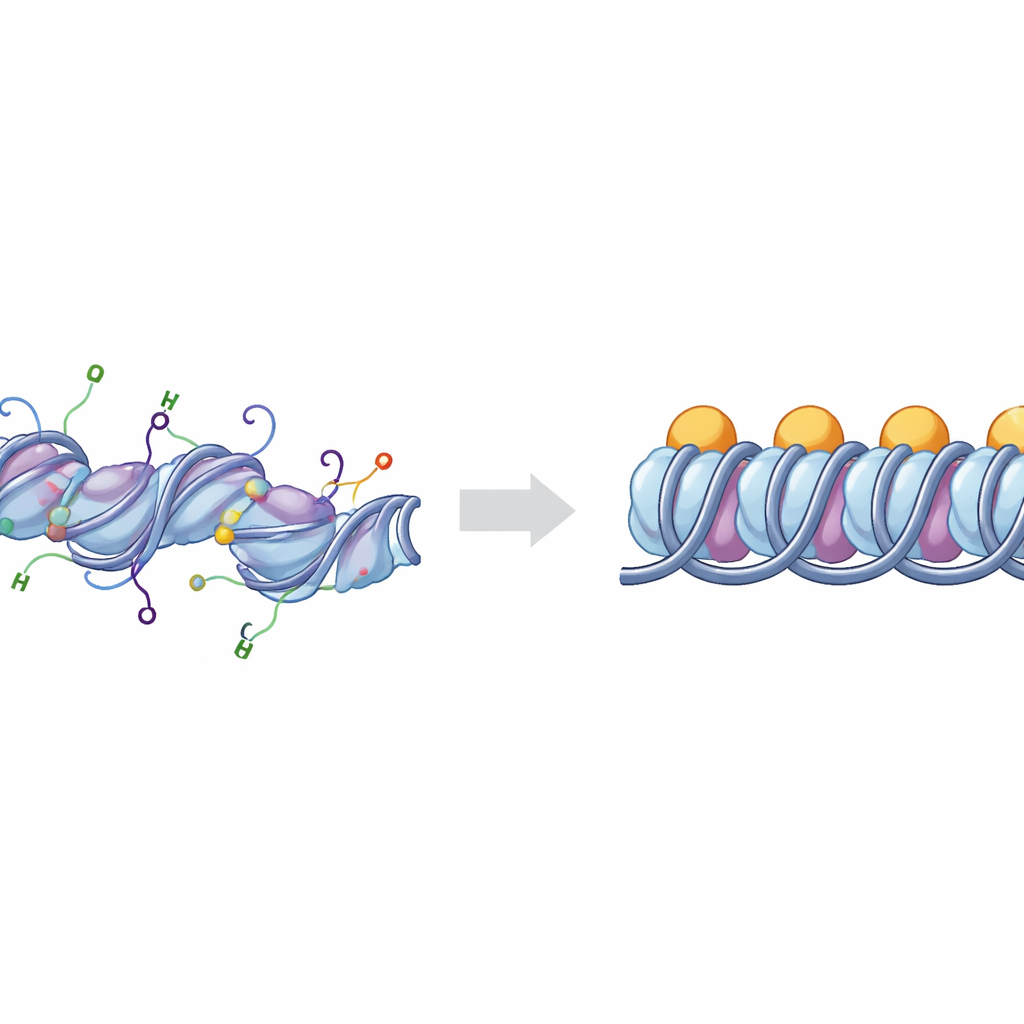
اللبنات الأساسية لتعبئة الحمض النووي
يلتف الحمض النووي في كروموسوماتنا حول مجموعات من بروتينات الهستون لتشكيل وحدات تعرف بالنوكليوسومات. عندما يرتبط بروتين إضافي، الهستون الرابط H1، عند نقاط دخول وخروج الحمض النووي من النوكليوسوم، تُسمى البنية كروماتوسوم. يمكن لمجموعات من الكروماتوسومات أن تتراص وتطوى لتكوّن مناطق محكمة التعبئة من الحمض النووي التي تكون عمومًا أقل نشاطًا. تضبط الخلايا هذه التعبئة بعلامات كيميائية توضع على "ذيول" مرنة تمتد من الهستونات. اثنتان من أهم هذه الذيول تنتمي للهستونين H3 وH4، حيث ترتبط التغييرات الكيميائية عليهما ارتباطًا قويًا بما إذا كانت مناطق الحمض النووي تتصرف ككروماتين نشط مفتوح (يوكروماتين) أو صامت مضغوط (هتيروكروماين).
كيف يؤثر تغيير ذيل واحد على الآخر
أظهرت أعمال سابقة أن إضافة أربع مجموعات أسيتيل إلى ذيل H4 — عند مواضع تعرف مجتمعة باسم H4‑4Kac — تميل إلى جعل ذيل H3 المجاور أسهل على نحو متزايد لأن يُأسَيتَل أيضًا، لكن ذلك فُحص أساسًا في غياب الهستون الرابط H1. البحث الجديد تساءل عما يحدث عندما يكون H1 حاضرًا، وهو وضع أقرب إلى الحالة الحقيقية في الخلايا الحية. باستخدام المجهر الإلكتروني بالتبريد، حلّل المؤلفون هياكل كروماتوسومات عالية الدقة تحمل ذيل H4 المؤستل. على نحو مفاجئ، ظل الشكل العام للحمض النووي والبروتينات الأساسية تقريبًا دون تغيير بالمقارنة مع الكروماتوسومات غير المعدلة. بقي بروتين H1 في نفس الموضع المركزي، وبدا الحمض النووي الملفوف متطابقًا تقريبًا، مما يشير إلى أن أي تأثيرات مهمة يجب أن تنشأ من تغيّر في كيفية تحرك ذيول الهستون المرنة واحتكاكها بالحمض النووي.
متابعة الأجزاء المتحركة بمحاكاة ومغناطيس
لالتقاط هذه الحركات السريعة والدقيقة، جمع الفريق بين محاكاة حاسوبية وطيف الرنين المغناطيسي النووي (NMR). نمذجة الديناميكا الجزيئية الخشنة المحببة مثلت كيف تفرك ذيول H3 وH4 السطح الملفوف من الحمض النووي والامتدادات الإضافية للحمض النووي التي تربط النوكليوسومات معًا. في الكروماتوسومات، يجعل وجود H1 ذيلي H3 يتصرفان بشكل مختلف بطبيعة الحال: يميل أحدهما إلى ملامسة الحمض النووي الملفوف في اللب أساسًا، بينما يتصل الآخر أيضًا بالحمض النووي الرابط المكشوف. عند أسيتلة H4، ينفصل ذيله عن الحمض النووي قليلاً، ويصبح أكثر مرونة ومكشوفًا للمذيب. هذا التحرر يغيّر قليلًا كيف يستكشف كل من ذيل H1 الطويل وذيول H3 سطح الحمض النووي، لكن المحاكيات اقترحت تغييرات متواضعة فقط في أنماط التلامس المتوسطة.
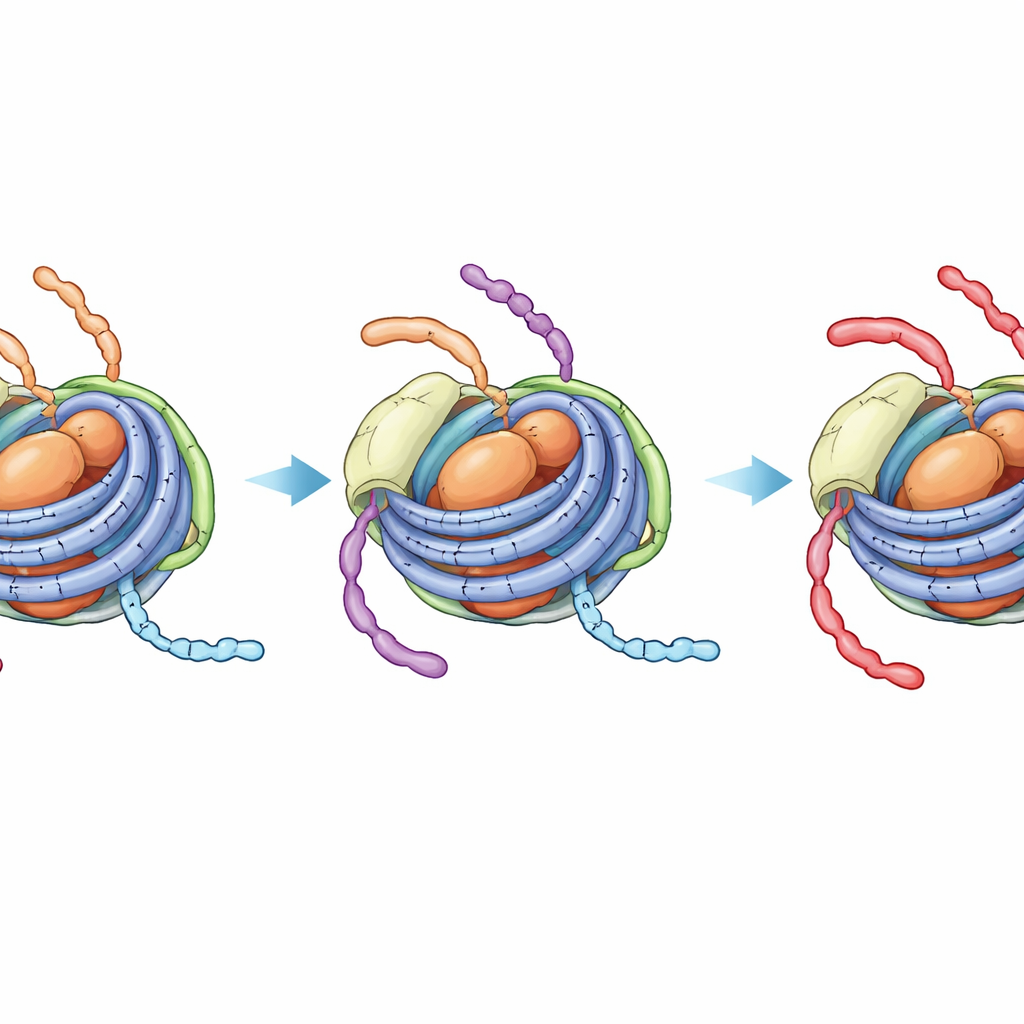
حالة مخفية أكثر إحكامًا تمنع التغيير الإضافي
كشف طيف الرنين المغناطيسي النووي، الذي يستشعر البيئة المحلية لذرات محددة، عن تأثير أكثر بروزًا. في الكروماتوسومات غير المعدلة، تُظهر إشارات ذيل H3 مزيجًا من حالتين ديناميكيتين — إحداهما تشبه النوكليوسوم الأكثر انفتاحًا (مع اتصال بالحمض النووي الرابط) والأخرى تشبه جسيم النوكليوسوم الأكثر إحكامًا الذي يلامس اللب فقط. وعلى مقياس زمن تفاعل إنزيمي، تتبادل هاتان الحالتان مواقعهما، لذلك يستطيع الإنزيم الذي يؤستِل الموضع K14 على ذيل H3 الوصول إلى المقاطع المعرضة للحمض النووي الرابط. بالمقابل، عندما يحمل ذيل H4 أربع مجموعات أسيتيل ويكون H1 حاضرًا، تنهار إشارات ذيل H3 إلى حالة واحدة قوية تشبه الشكل الملتصق بالحمض النووي اللبّي المحكم. وأكدت مراقبة NMR المباشرة لتفاعل الأسيتلة أن تعديل K14 على H3 يحدث بعد ذلك أبطأ بكثير، بمعدل لا يكاد يختلف عن النوكليوسوم المغلق في اللب بدون أي حمض نووي رابط على الإطلاق.
ماذا يعني هذا لمفاتيح تشغيل/إطفاء الجينات
تُشير النتائج مجتمعة إلى أن أسيتلة ذيل H4، بوجود الهستون الرابط H1، تساعد على نحو متناقض في تثبيت ذيول H3 المجاورة تجاه الحمض النووي اللبّي بدلاً من تحريرها لتغييرات إضافية. من خلال تعزيز هذه الحالة المستقرة الملتصقة بالحمض النووي وإبطاء الأسيتلة الإضافية لذيل H3 بشكل كبير، يبدو أن H1 يعمل ضد انتشار الكروماتين المفتوح النشط وبدلاً من ذلك يفضّل مناطق أكثر ضغطًا وصمتًا. ببساطة، تظهر الدراسة أن مجموعة من العلامات الكيميائية وبروتين إضافي واحد يمكن أن يقررا ما إذا كانت أجزاء قريبة من الحمض النووي ستبقى متاحة للعمل أم تُطوى للتخزين طويل الأمد، مضيفة طبقة جديدة من الفهم لكيفية حفاظ الخلايا على هويتها عبر الزمن.
الاستشهاد: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
الكلمات المفتاحية: بنية الكروماتين, أسيتلة الهستون, الهستون الرابط H1, ديناميكيات النوكليوسوم, تنظيم فوق جيني