Clear Sky Science · ru
Связывающий гистон H1 подавляет ацетилирование хвоста H3, индуцированное ацетилированием хвоста H4, и меняет его динамику
Почему важны крошечные хвосты белков для нашей ДНК
В каждой клетке почти два метра ДНК упакованы в микроскопическое ядро. Эту задачу сворачивания выполняют катушки белков, называемые гистонами, которые помогают определять, включены ли гены или выключены. Новое исследование изучало, как небольшие химические метки на этих гистонах и присутствие другого белка, связывающего гистона H1, совместно влияют на то, открывается ли ДНК для активности генов или остаётся запертой. Понимание этого баланса проливает свет на то, как клетки сохраняют долгосрочную память о том, какие гены должны оставаться активными или молчаливыми.
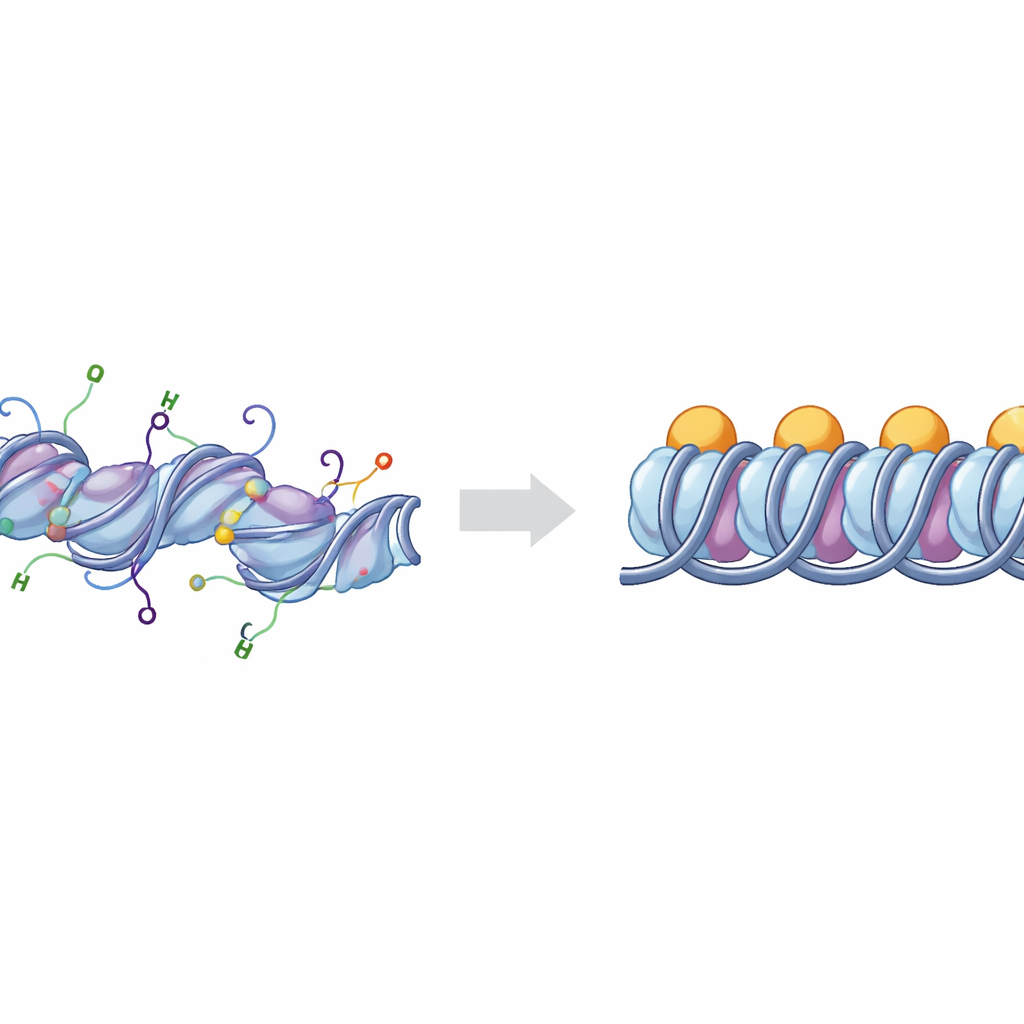
Основные строительные блоки упаковки ДНК
ДНК в наших хромосомах намотана на скопления гистоновых белков и формирует структуры, известные как нуклеосомы. Когда дополнительный белок — связывающий гистон H1 — присоединяется в точках входа и выхода ДНК из нуклеосомы, такая структура называется хроматосомой. Группы хроматосом могут укладываться и складываться, образуя туго упакованные участки ДНК, которые обычно менее активны. Клетки тонко настраивают эту упаковку с помощью химических меток, нанесённых на гибкие «хвосты», выступающие из гистонов. Два из наиболее важных хвостов принадлежат гистонам H3 и H4, и их химические модификации тесно связаны с тем, ведёт ли участок ДНК себя как активный, открытый «еуахроматин» или как молчаливый, плотный «гетерохроматин».
Как изменение одного хвоста влияет на другой
Предыдущие работы показали, что добавление четырёх ацетильных групп к хвосту H4 — в позициях, известных совместно как H4‑4Kac — как правило, делает соседний хвост H3 более доступным для ацетилирования, но это изучалось главным образом без связывающего гистона H1. Новое исследование поставило вопрос, что происходит в присутствии H1, что ближе к реалиям живой клетки. С помощью криоэлектронной микроскопии авторы получили высокоразрешающие структуры хроматосом с ацетилированным хвостом H4. Удивительно, но общая форма сердечников ДНК и гистонов почти не изменилась по сравнению с ненаправленными хроматосомами. Белок H1 по‑прежнему занимал ту же центральную позицию, а намотанная ДНК выглядела почти идентично, что указывает на то, что важные эффекты должны возникать из изменений в том, как подвижные хвосты гистонов двигаются и контактируют с ДНК.
Отслеживание движущихся частей с помощью симуляций и магнитов
Чтобы зафиксировать эти быстрые и тонкие движения, команда объединила компьютерные симуляции с ядерным магнитным резонансом (ЯМР) спектроскопией. Крупномасштабные молекулярно‑динамические симуляции моделировали, как хвосты H3 и H4 касаются намотанной ДНК и дополнительных участков связывающей ДНК между нуклеосомами. В хроматосомах наличие H1 естественным образом делает два хвоста H3 неэквивалентными: один склонен контактировать в основном с намотанной на сердечник ДНК, тогда как другой также взаимодействует с открытой связывающей ДНК. При ацетилировании H4 его собственный хвост отходит от ДНК, становясь более гибким и обратимым для растворителя. Это высвобождение немного сдвигает то, как длинный хвост H1 и хвосты H3 исследуют поверхность ДНК, но симуляции показали лишь умеренные средние изменения в шаблонах контактов.
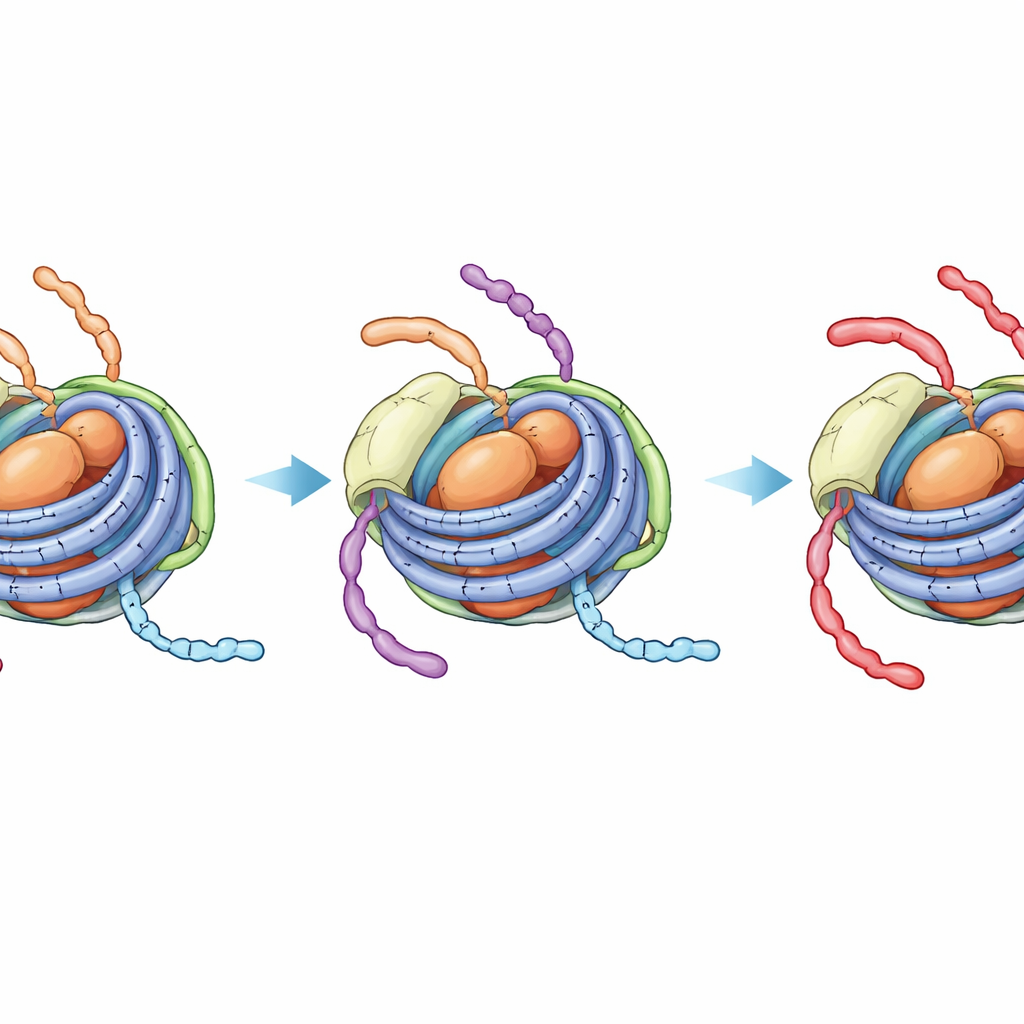
Скрытое, более плотное состояние, блокирующее дальнейшие изменения
ЯМР‑спектроскопия, чувствительная к локальной среде отдельных атомов, выявила более заметный эффект. В ненаправленных хроматосомах сигналы от хвоста H3 показывают смесь двух динамических состояний — одно напоминает более открытый нуклеосом (с контактом со связывающей ДНК), а другое напоминает более плотную частицу, контактирующую только с сердечниковой ДНК. На временной шкале ферментативной реакции эти состояния меняются, поэтому фермент, ацетилирующий позицию K14 на хвосте H3, по‑прежнему имеет доступ к сегментам, выставленным к связывающей ДНК. Напротив, когда хвост H4 несёт четыре ацетильные группы и присутствует H1, сигналы H3 схлопываются в одно устойчивое состояние, похожее на плотно связанный вариант с сердечниковой ДНК. Прямое ЯМР‑наблюдение реакции ацетилирования подтвердило, что модификация H3 K14 в этом случае происходит значительно медленнее — с частотой, почти неотличимой от закрытого нуклеосомного сердечника вовсе без связывающей ДНК.
Что это значит для переключателей включения/выключения генов
В совокупности результаты указывают на то, что ацетилирование хвоста H4 в присутствии связывающего гистона H1 парадоксальным образом способствует прижатию соседних хвостов H3 к сердечниковой ДНК, а не освобождению их для дальнейших изменений. Продвигая это стабильное, «обнимающее» ДНК состояние и сильно замедляя дополнительное ацетилирование H3, H1 по‑видимому противодействует распространению открытого, активного хроматина и вместо этого способствует образованию более компактных, молчаливых участков. Простыми словами, исследование показывает, что один набор химических меток и один дополнительный белок могут решить, останутся ли соседние участки ДНК открытыми для работы или будут сложены для долгосрочного хранения, добавляя новый уровень понимания того, как клетки сохраняют свою идентичность во времени.
Цитирование: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Ключевые слова: структура хроматина, ацетилирование гистонов, связывающий гистон H1, динамика нуклеосом, эпигенетическая регуляция