Clear Sky Science · fr
L’histone de liaison H1 réprime l’acétylation de la queue H3 induite par l’acétylation de la queue H4 et modifie sa dynamique
Pourquoi de petites queues protéiques importent pour notre ADN
À l’intérieur de chaque cellule, près de deux mètres d’ADN sont condensés dans un noyau microscopique. Cette prouesse de repliement est assurée par des bobines de protéines appelées histones, qui contribuent à décider si des gènes sont activés ou réprimés. La nouvelle étude a examiné comment de petits marquages chimiques sur ces histones, et la présence d’une autre protéine appelée histone de liaison H1, agissent de concert pour soit ouvrir l’ADN en vue d’une activité génique, soit le maintenir verrouillé. Comprendre cet équilibre éclaire la façon dont les cellules conservent une mémoire à long terme des gènes qui doivent rester actifs ou silencieux.
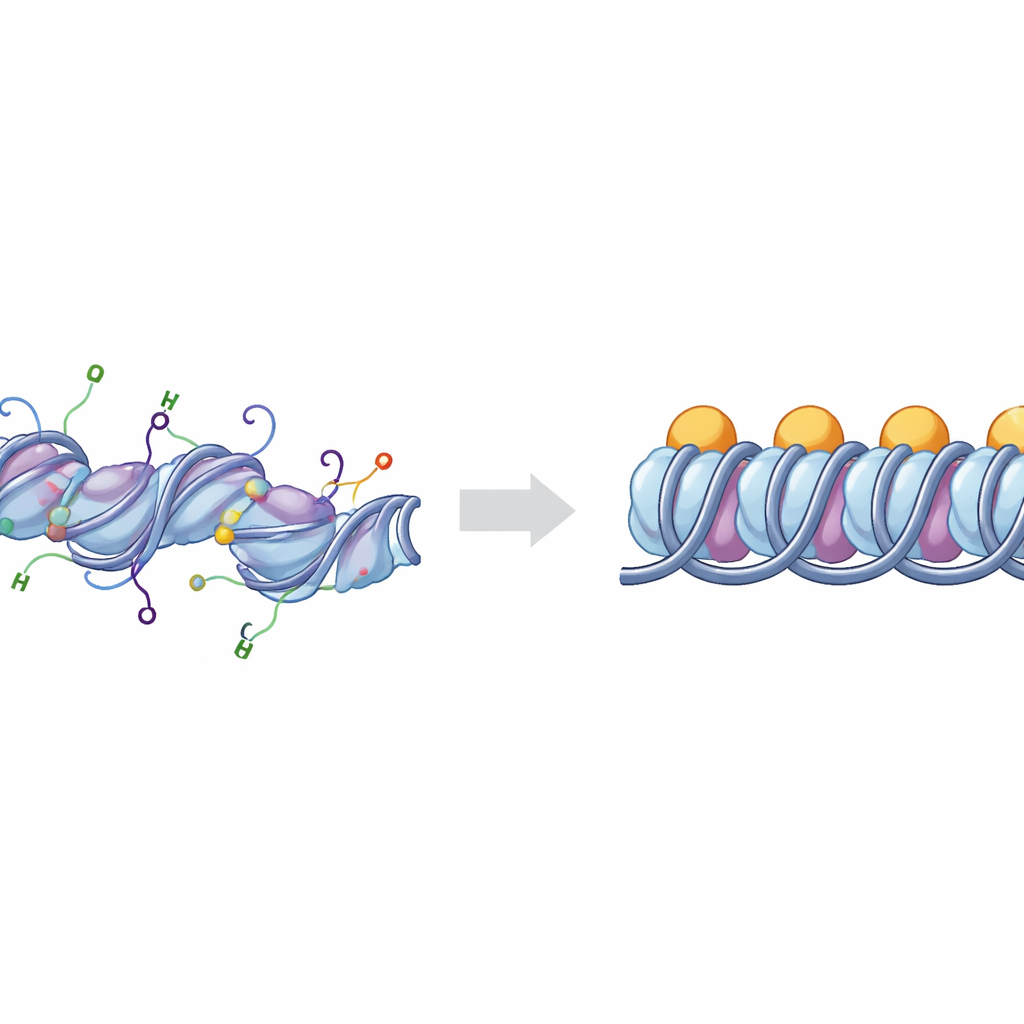
Les éléments de base du compactage de l’ADN
L’ADN de nos chromosomes s’enroule autour d’amas de protéines histones pour former des unités appelées nucléosomes. Lorsqu’une protéine supplémentaire, l’histone de liaison H1, se lie aux points d’entrée et de sortie de l’ADN sur le nucléosome, la structure est appelée chromatosome. Des groupes de chromatosomes peuvent s’empiler et se replier pour créer des régions d’ADN fortement compactées généralement moins actives. Les cellules ajustent finement ce compactage grâce à des marques chimiques placées sur des « queues » flexibles qui dépassent des histones. Deux des queues les plus importantes appartiennent aux histones H3 et H4, dont les modifications chimiques sont fortement liées au fait que des régions d’ADN se comportent comme une euchromatine active et ouverte ou comme une hétérochromatine compacte et silencieuse.
Comment la modification d’une queue affecte une autre
Des travaux antérieurs ont montré que l’ajout de quatre groupes acétyle à la queue de H4 — à des positions connues collectivement sous le nom de H4‑4Kac — tend à rendre la queue voisine H3 plus facilement acétylable également, mais cela avait été principalement étudié en l’absence de l’histone de liaison H1. La nouvelle recherche a demandé ce qui se passe lorsque H1 est présent, une situation plus réaliste in vivo. À l’aide de cryo‑microscopie électronique, les auteurs ont résolu des structures de chromatosomes à haute résolution portant la queue H4 acétylée. De manière surprenante, la forme globale de l’ADN enroulé et des protéines histones est restée presque inchangée par rapport aux chromatosomes non modifiés. La protéine H1 occupait toujours la même position centrale, et l’ADN enroulé paraissait quasi identique, ce qui suggère que les effets importants doivent provenir des changements dans la mobilité des queues d’histones flexibles et de leurs contacts avec l’ADN.
Suivre les éléments mobiles avec des simulations et des aimants
Pour capturer ces mouvements rapides et subtils, l’équipe a combiné des simulations informatiques et la spectroscopie par résonance magnétique nucléaire (RMN). Des simulations de dynamique moléculaire grossière ont modélisé comment les queues H3 et H4 frôlent l’ADN enroulé et les segments d’ADN liant exposés entre nucléosomes. Dans les chromatosomes, la présence de H1 rend naturellement les deux queues H3 hétérogènes : l’une tend à toucher principalement l’ADN enroulé autour du cœur, tandis que l’autre contacte aussi l’ADN de liaison exposé. Lorsque H4 est acétylée, sa propre queue se détache de l’ADN, devenant plus flexible et exposée au solvant. Ce relâchement modifie légèrement la façon dont la longue queue de H1 et les queues H3 explorent la surface de l’ADN, mais les simulations ont suggéré des changements moyens modestes dans les schémas de contact.
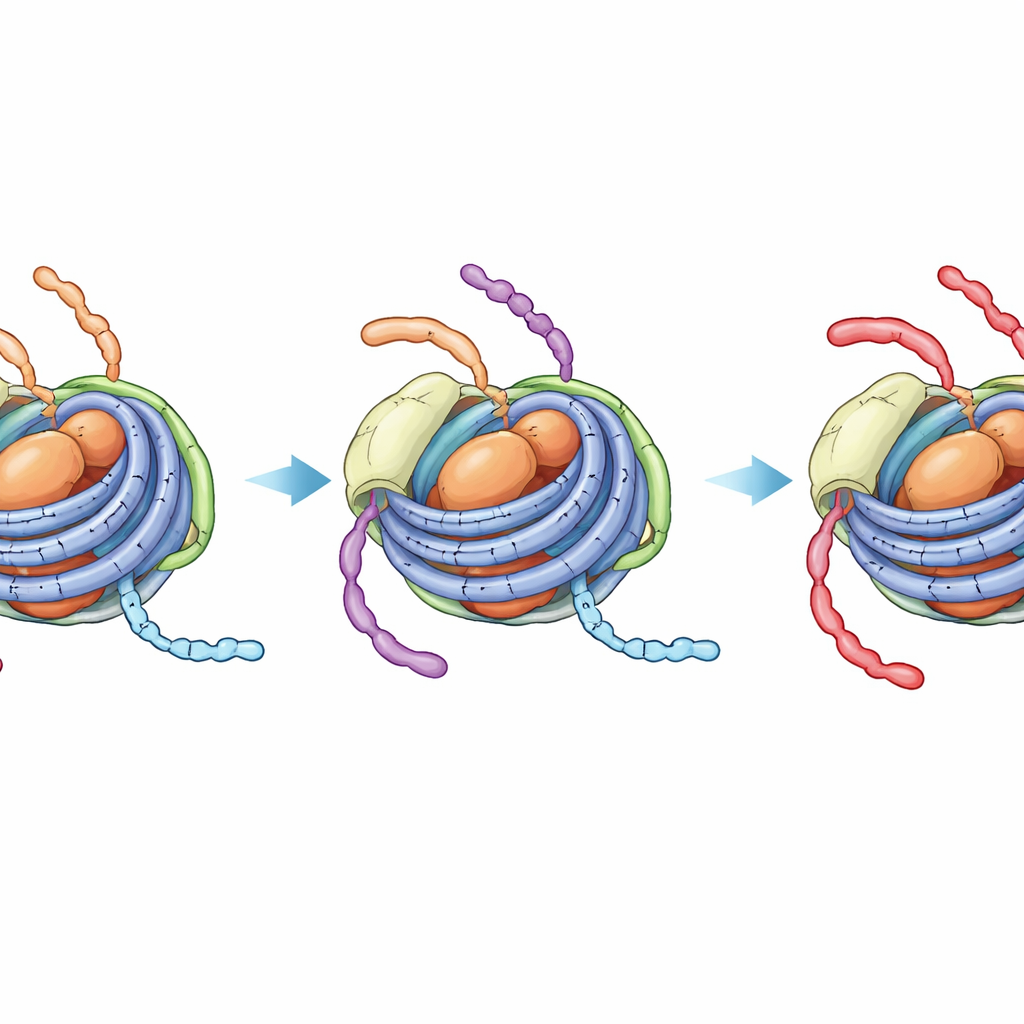
Un état caché et plus serré qui bloque d’autres changements
La RMN, qui détecte l’environnement local d’atomes spécifiques, a révélé un effet plus marqué. Dans les chromatosomes non modifiés, les signaux venant de la queue H3 montrent un mélange de deux états dynamiques — l’un ressemblant au nucléosome plus ouvert (avec contact à l’ADN de liaison) et l’autre au particule nucléosomale plus serrée limitée au cœur. À l’échelle temporelle d’une réaction enzymatique, ces états s’échangent, de sorte que l’enzyme qui acétyle la position K14 sur la queue H3 peut encore accéder aux segments exposés du lien. En revanche, lorsque la queue H4 porte quatre groupes acétyle et que H1 est présent, les signaux de la queue H3 s’effondrent en un seul état robuste qui ressemble à la forme étroitement liée à l’ADN du cœur. La surveillance directe par RMN de la réaction d’acétylation a confirmé que la K14 de H3 est alors modifiée beaucoup plus lentement, à un rythme presque indiscernable de celui du cœur nucléosomique fermé sans aucun ADN de liaison.
Ce que cela signifie pour les interrupteurs marche/arrêt des gènes
Pris ensemble, les résultats suggèrent que l’acétylation de la queue H4, en présence de l’histone de liaison H1, aide paradoxalement à verrouiller les queues H3 voisines contre l’ADN du cœur plutôt qu’à les libérer pour d’autres modifications. En favorisant cet état stable, « collé » à l’ADN, et en ralentissant fortement l’acétylation supplémentaire de H3, H1 semble s’opposer à la propagation d’une chromatine ouverte et active et privilégier des régions plus compactes et silencieuses. Pour dire les choses simplement, l’étude montre qu’un jeu de marques chimiques et une seule protéine supplémentaire peuvent décider si des segments d’ADN voisins restent ouverts pour l’activité ou sont repliés pour un stockage à long terme, ajoutant une couche supplémentaire de compréhension sur la façon dont les cellules préservent leur identité au fil du temps.
Citation: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Mots-clés: structure de la chromatine, acétylation des histones, histone de liaison H1, dynamique du nucléosome, régulation épigénétique