Clear Sky Science · it
L’istone linker H1 reprime l’acetilazione della coda di H3 indotta dall’acetilazione della coda di H4 e ne altera la dinamica
Perché le minuscole code proteiche sono importanti per il nostro DNA
All’interno di ogni cellula, quasi due metri di DNA sono compattati in un nucleo microscopico. Questa impresa di ripiegamento è gestita da avvolgimenti di proteine chiamate istoni, che contribuiscono a decidere se i geni vengono attivati o spenti. Il nuovo studio ha esplorato come piccoli marcatori chimici su questi istoni, insieme alla presenza di un’altra proteina chiamata istone linker H1, cooperino per aprire il DNA all’attività genica oppure per mantenerlo chiuso. Capire questo equilibrio fa luce su come le cellule mantengano una memoria a lungo termine di quali geni debbano rimanere attivi o silenti.
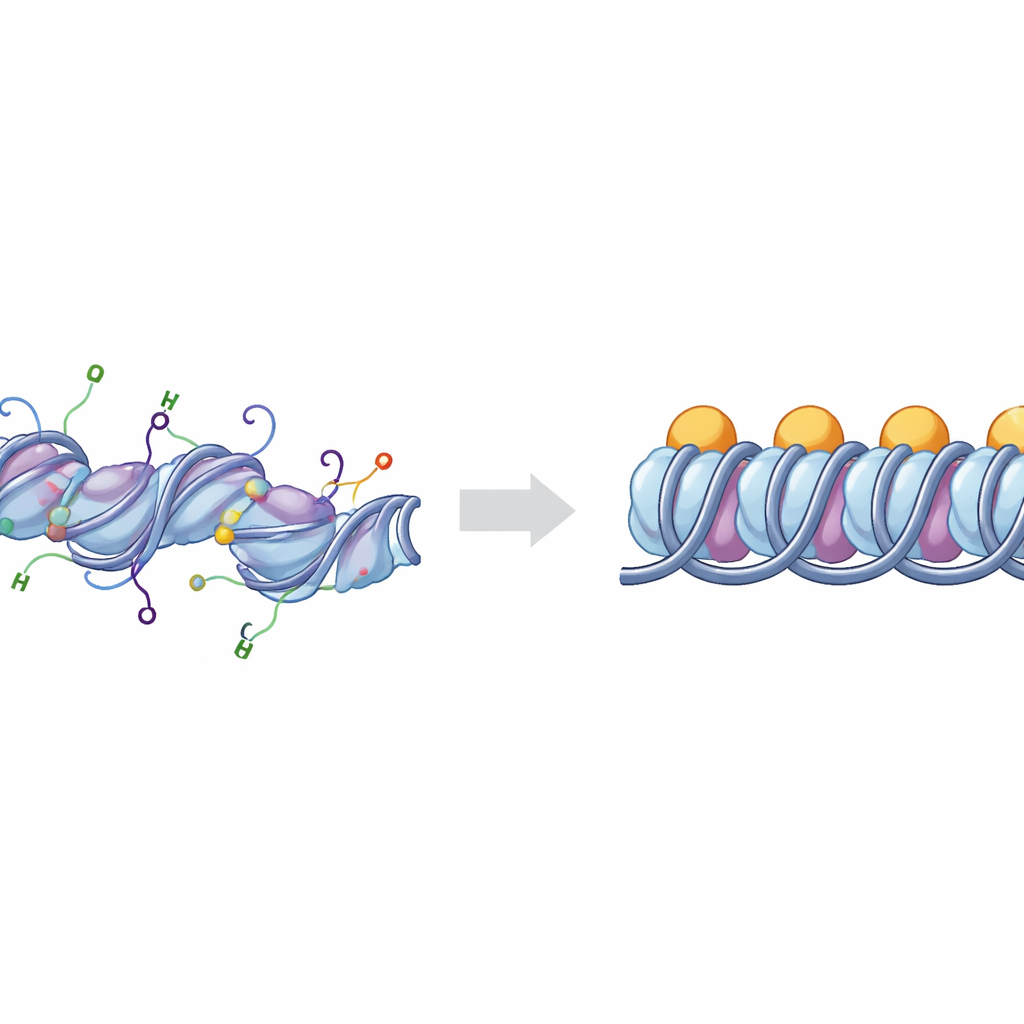
I mattoni fondamentali dell’impacchettamento del DNA
Il DNA nei nostri cromosomi è avvolto attorno a complessi di proteine istoniche per formare unità note come nucleosomi. Quando una proteina aggiuntiva, l’istone linker H1, si lega nei punti in cui il DNA entra ed esce dal nucleosoma, la struttura prende il nome di cromatosoma. Gruppi di cromatosomi possono impilarsi e ripiegarsi per creare regioni di DNA strettamente compattate che sono generalmente meno attive. Le cellule rifiniscono questo impacchettamento con marche chimiche poste su “code” flessibili che si estendono dagli istoni. Due delle code più importanti appartengono agli istoni H3 e H4, i cui cambiamenti chimici sono fortemente legati al fatto che porzioni di DNA si comportino come euchromatina aperta e attiva o come eterocromatina compatta e silente.
Come la modifica di una coda influisce sull’altra
Lavori precedenti avevano mostrato che l’aggiunta di quattro gruppi acetile alla coda di H4—nelle posizioni note collettivamente come H4‑4Kac—tende a rendere più facile anche l’acetilazione della coda di H3 vicina, ma ciò era stato studiato principalmente in assenza dell’istone linker H1. La nuova ricerca si è chiesta cosa accade quando H1 è presente, una situazione più realistica nelle cellule viventi. Tramite criomicroscopia elettronica, gli autori hanno risolto strutture ad alta risoluzione di cromatosomi che portavano la coda di H4 acetilata. Sorprendentemente, la forma complessiva del DNA centrale e delle proteine istoniche è rimasta quasi invariata rispetto ai cromatosomi non modificati. La proteina H1 è risultata ancora nella stessa posizione centrale e il DNA avvolto appariva quasi identico, suggerendo che eventuali effetti importanti derivino dai cambiamenti nel modo in cui le code istoniche flosce si muovono e si rapportano al DNA.
Seguire le parti in movimento con simulazioni e magneti
Per catturare questi moti rapidi e sottili, il gruppo ha combinato simulazioni al computer con spettroscopia di risonanza magnetica nucleare (NMR). Simulazioni di dinamica molecolare a grana grossa hanno modellato come le code di H3 e H4 sfiorino il DNA avvolto e i tratti extra di DNA che collegano i nucleosomi. Nei cromatosomi, la presenza di H1 rende naturalmente le due code di H3 differenti nel comportamento: una tende a contattare principalmente il DNA avvolto nel core, mentre l’altra entra in contatto anche con il DNA linker esposto. Quando H4 è acetilata, la sua stessa coda si stacca dal DNA, diventando più flessibile ed esposta al solvente. Questo rilascio sposta leggermente il modo in cui sia la lunga coda di H1 sia le code di H3 esplorano la superficie del DNA, ma le simulazioni suggerivano solo modesti cambiamenti medi nei pattern di contatto.
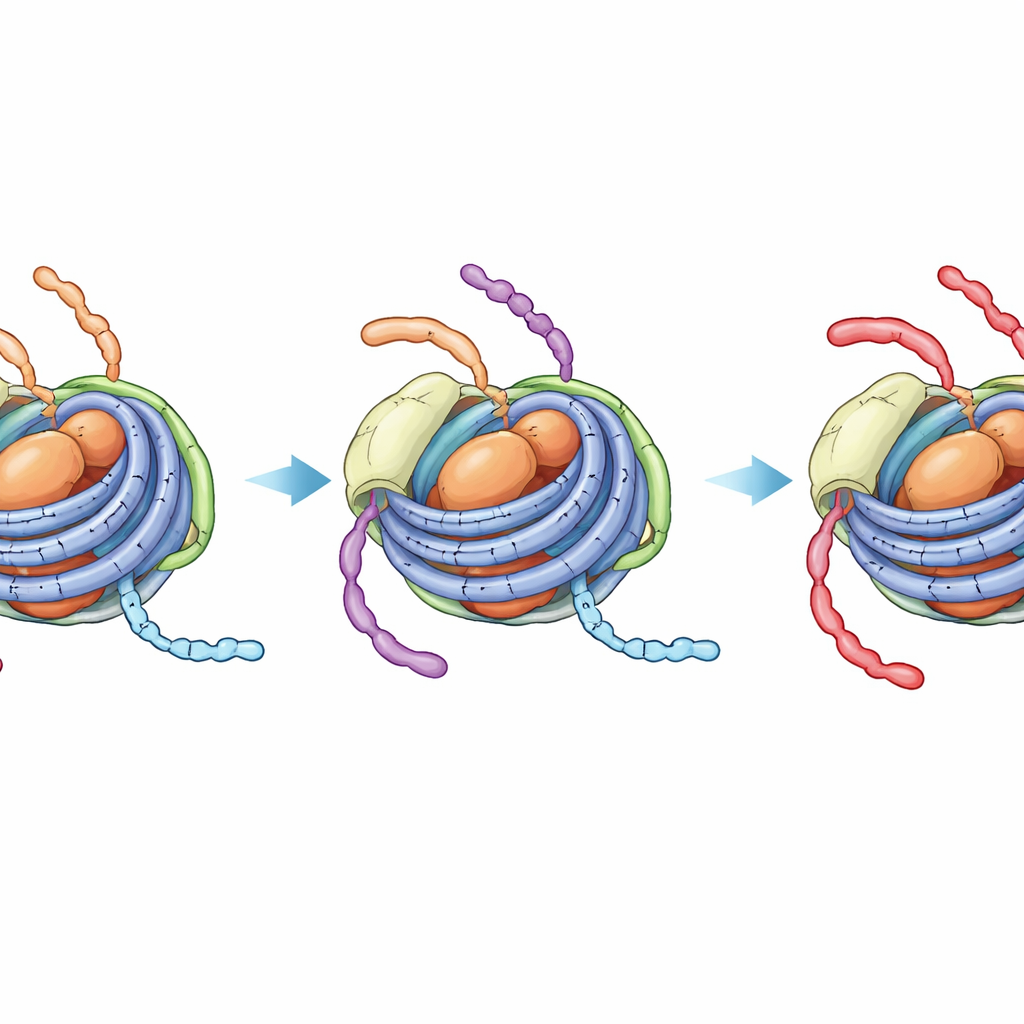
Uno stato nascosto e più compatto che blocca ulteriori modifiche
La spettroscopia NMR, che rileva l’ambiente locale di specifici atomi, ha rivelato un effetto più evidente. Nei cromatosomi non modificati, i segnali provenienti dalla coda di H3 mostrano una miscela di due stati dinamici—uno somigliante al nucleosoma più aperto (con contatto al DNA linker) e uno somigliante alla particella di nucleosoma più compatta limitata al core. Su scale temporali tipiche di una reazione enzimatica, questi stati si scambiano, così l’enzima che acetila la posizione K14 sulla coda di H3 può ancora raggiungere segmenti esposti al linker. Al contrario, quando la coda di H4 porta quattro gruppi acetile e H1 è presente, i segnali di H3 collassano in un unico stato robusto che somiglia alla forma strettamente legata al DNA del core. Il monitoraggio diretto NMR della reazione di acetilazione ha confermato che H3 K14 viene quindi modificata molto più lentamente, a una velocità quasi indistinguibile da quella del nucleosoma chiuso senza alcun DNA linker.
Cosa significa per gli interruttori on/off dei geni
Considerando i risultati nel loro insieme, gli autori suggeriscono che l’acetilazione della coda di H4, in presenza dell’istone linker H1, paradossalmente contribuisce a bloccare le code di H3 vicine contro il DNA del core anziché liberarle per ulteriori modifiche. Promuovendo questo stato stabile e abbracciante il DNA e rallentando fortemente l’acetilazione aggiuntiva di H3, H1 sembra contrastare la diffusione della cromatina aperta e attiva e favorire invece regioni più compatte e silenti. In termini pratici, lo studio mostra che un insieme di marche chimiche e una singola proteina in più possono decidere se tratti contigui di DNA restano aperti e funzionali oppure vengono ripiegati e conservati a lungo termine, aggiungendo un nuovo livello di comprensione su come le cellule preservino la propria identità nel tempo.
Citazione: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Parole chiave: struttura della cromatina, acetilazione degli istoni, istone linker H1, dinamica del nucleosoma, regolazione epigenetica