Clear Sky Science · nl
Linkerhiston H1 onderdrukt H3-staartacetylatie geïnduceerd door H4-staartacetylatie en verandert diens dynamiek
Waarom kleine proteïnestaarten belangrijk zijn voor ons DNA
In elke cel worden bijna twee meter DNA opgeborgen in een microscopische kern. Dit opvouwingskunstje wordt verzorgd door spoelen van eiwitten die histonen heten en die mede bepalen of genen aan of uit staan. De nieuwe studie onderzocht hoe kleine chemische labels op deze histonen, en de aanwezigheid van een ander eiwit genaamd linkerhiston H1, samenwerken om DNA óf toegankelijk te maken voor genactiviteit óf juist dicht te houden. Inzicht in dit evenwicht verklaart hoe cellen langdurig ‘onthouden’ welke genen actief of stil moeten blijven.
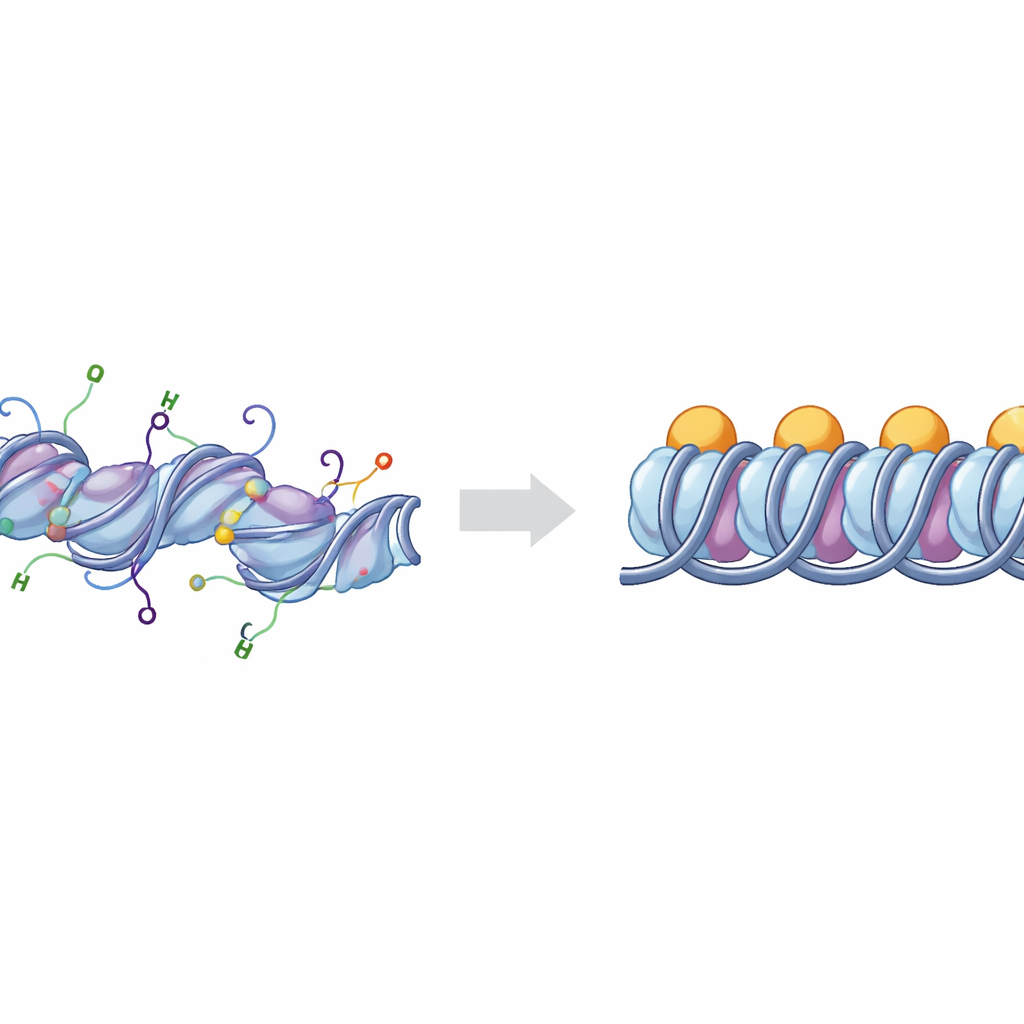
De basiselementen van DNA‑opslag
Het DNA in onze chromosomen is om clusters histoneiwitten gewonden en vormt zodoende eenheidjes die nucleosomen heten. Als een extra eiwit, linkerhiston H1, zich bindt op de plekken waar het DNA het nucleosoom in- en uitgaat, spreekt men van een chromatosoom. Rijen chromatosomen kunnen opstapelen en vouwen tot dicht opeengepakte DNA‑gebieden die doorgaans minder actief zijn. Cellen stemmen deze verpakking fijn af met chemische merktekens die op flexibele “staarten” van de histonen zitten. Twee van de belangrijkste staarten behoren tot histonen H3 en H4, waarvan de chemische veranderingen sterk samenhangen met of DNA‑gebieden fungeren als actief, open euchromatine of stil, compact heterochromatine.
Hoe verandering in de ene staart de andere beïnvloedt
Eerder werk toonde dat het toevoegen van vier acetylgroepen aan de H4‑staart — op posities samengevat als H4‑4Kac — ertoe neigt de naburige H3‑staart ook makkelijker te laten acetylëren, maar dat was vooral bestudeerd zonder linkerhiston H1. De nieuwe studie vroeg wat er gebeurt als H1 aanwezig is, een realistischer situatie in levende cellen. Met cryo‑elektronenmicroscopie bepaalden de auteurs hoge‑resolutie structuren van chromatosomen met de geacetyleerde H4‑staart. Verrassend genoeg bleef de algemene vorm van het kern‑DNA en de core‑histonproteïnen vrijwel ongewijzigd vergeleken met niet‑gemodificeerde chromatosomen. H1 zat nog steeds op dezelfde centrale plaats en het gewikkelde DNA leek bijna identiek, wat suggereert dat belangrijke effecten voortkomen van veranderingen in hoe de losse histonstaarten bewegen en het DNA aanraken.
Bewegingen volgen met simulaties en magneten
Om deze snelle, subtiele bewegingen vast te leggen combineerde het team computersimulaties met nucleaire magnetische resonantie (NMR)‑spectroscopie. Grofmazige moleculaire dynamica‑simulaties modelleerden hoe de H3‑ en H4‑staarten langs het gewikkelde DNA en de extra stukken linker‑DNA tussen nucleosomen schuren. In chromatosomen veroorzaakt de aanwezigheid van H1 dat de twee H3‑staarten zich van nature anders gedragen: de ene raakt vooral het core‑gewikkelde DNA aan, terwijl de andere ook contact maakt met het blootgestelde linker‑DNA. Wanneer H4 geacetyleerd is, laat die staart juist het DNA los en wordt flexibeler en meer aan de oplosmiddelzijde blootgesteld. Deze vrijmaking verschuift lichtjes hoe zowel H1’s lange staart als de H3‑staarten het DNA‑oppervlak verkennen, maar de simulaties suggereerden slechts bescheiden gemiddelde veranderingen in contactpatronen.
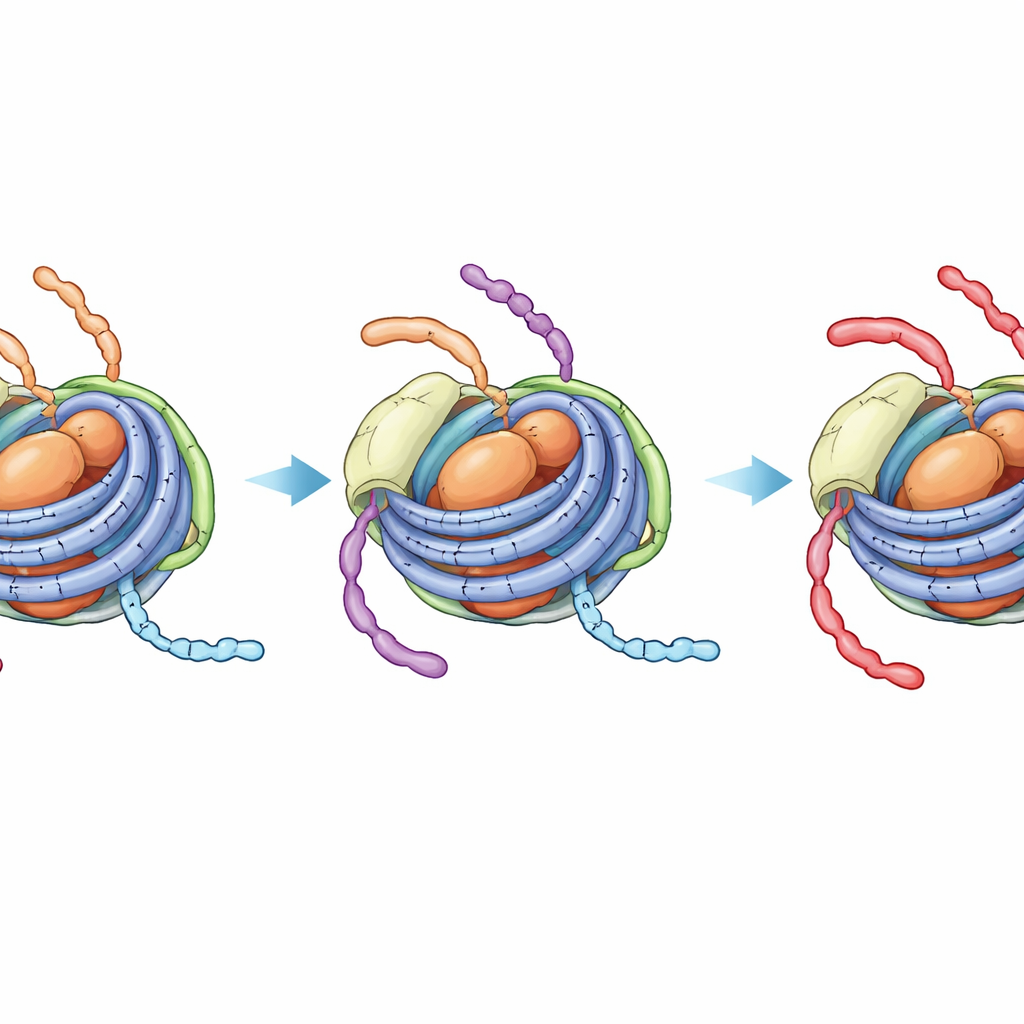
Een verborgen, strakere toestand die verdere verandering blokkeert
NMR‑spectroscopie, die de lokale omgeving van specifieke atomen waarneemt, toonde een opvallender effect. In ongewijzigde chromatosomen laten signalen van de H3‑staart een mengsel van twee dynamische toestanden zien — één die lijkt op het meer open nucleosoom (met contact met linker‑DNA) en één die lijkt op het strakker aan het core‑DNA gebonden nucleosoomdeeltje. Over de tijdschaal van een enzymreactie wisselen deze toestanden onderling, zodat het enzym dat positie K14 op de H3‑staart acetyleert nog steeds toegang heeft tot linker‑blootgestelde segmenten. Daarentegen, wanneer de H4‑staart vier acetylgroepen draagt en H1 aanwezig is, klappen de H3‑staatsignalen in elkaar tot één robuuste toestand die lijkt op de strak gebonden core‑DNA‑vorm. Directe NMR‑monitoring van de acetylatiereactie bevestigde dat H3 K14 dan veel trager wordt gemodificeerd, bijna niet meer te onderscheiden van de gesloten nucleosoomcore zonder enig linker‑DNA.
Wat dit betekent voor gen‑aan/uit‑schakelaars
Gezamenlijk wijzen de resultaten erop dat acetylatie van de H4‑staart, in aanwezigheid van linkerhiston H1, paradoxaal genoeg helpt de naburige H3‑staarten tegen het core‑DNA te vergrendelen in plaats van ze vrijer te maken voor verdere veranderingen. Door deze stabiele, aan‑het‑DNA‑geklemde toestand te bevorderen en aanvullende acetylatie van H3 sterk te vertragen, lijkt H1 de verspreiding van open, actief chromatine tegen te werken en eerder compacte, stille regio’s te bevoordelen. In gewone bewoordingen toont de studie aan dat één set chemische merktekens en één extra eiwit kunnen beslissen of naburige DNA‑stukken open blijven voor gebruik of worden opgevouwen voor langdurige opslag, en daarmee een nieuwe laag van begrip toevoegen aan hoe cellen hun identiteit in de loop van de tijd behouden.
Bronvermelding: Furukawa, A., Echigoya, K., Blazquez, S. et al. Linker histone H1 represses H3 tail acetylation induced by H4 tail acetylation and alters its dynamics. Commun Biol 9, 496 (2026). https://doi.org/10.1038/s42003-026-09926-y
Trefwoorden: chromatine‑structuur, histonacetylatie, linkerhiston H1, nucleosoomdynamiek, epigenetische regulatie