Clear Sky Science · zh
CRISPR-Cas9 筛选鉴定了肝癌中由 ATOX1 驱动的顺铂耐药机制并评估了靶向抑制剂的疗效
为何这项研究重要
肝癌是全球最致命的癌症之一,许多患者接受一种常用的化疗药物——顺铂。然而,随着时间推移,肿瘤常常学会对该药产生耐受,使疾病复发并转移。本研究揭示了这一耐药背后一个令人意外的分子元凶,并介绍了一种设计化合物,可能有助于提高顺铂的疗效并降低毒性。对于读者而言,这项工作展示了现代遗传学、计算模拟与化学如何结合以智取癌症的防御机制。
肝肿瘤如何躲避化疗
顺铂通过损伤 DNA 杀死癌细胞,但肿瘤可以通过多种手段变得耐药:将药物泵出细胞、更快修复 DNA,或重编程生存信号。作者利用一种强大的基因编辑工具——全基因组 CRISPR-Cas9 筛选,系统性敲除两株肝癌细胞系中的几乎所有基因,然后暴露于顺铂。他们提出一个简单的问题:当某个基因被敲除时,细胞对药物是更敏感还是更耐受?在数十个与耐药相关的基因中,有一个脱颖而出——ATOX1,这是一个通常帮助细胞处理必需金属铜的小蛋白。肝癌细胞中 ATOX1 的表达高于健康肝细胞,且肿瘤中 ATOX1 高表达的患者往往预后较差并更易出现顺铂耐药。
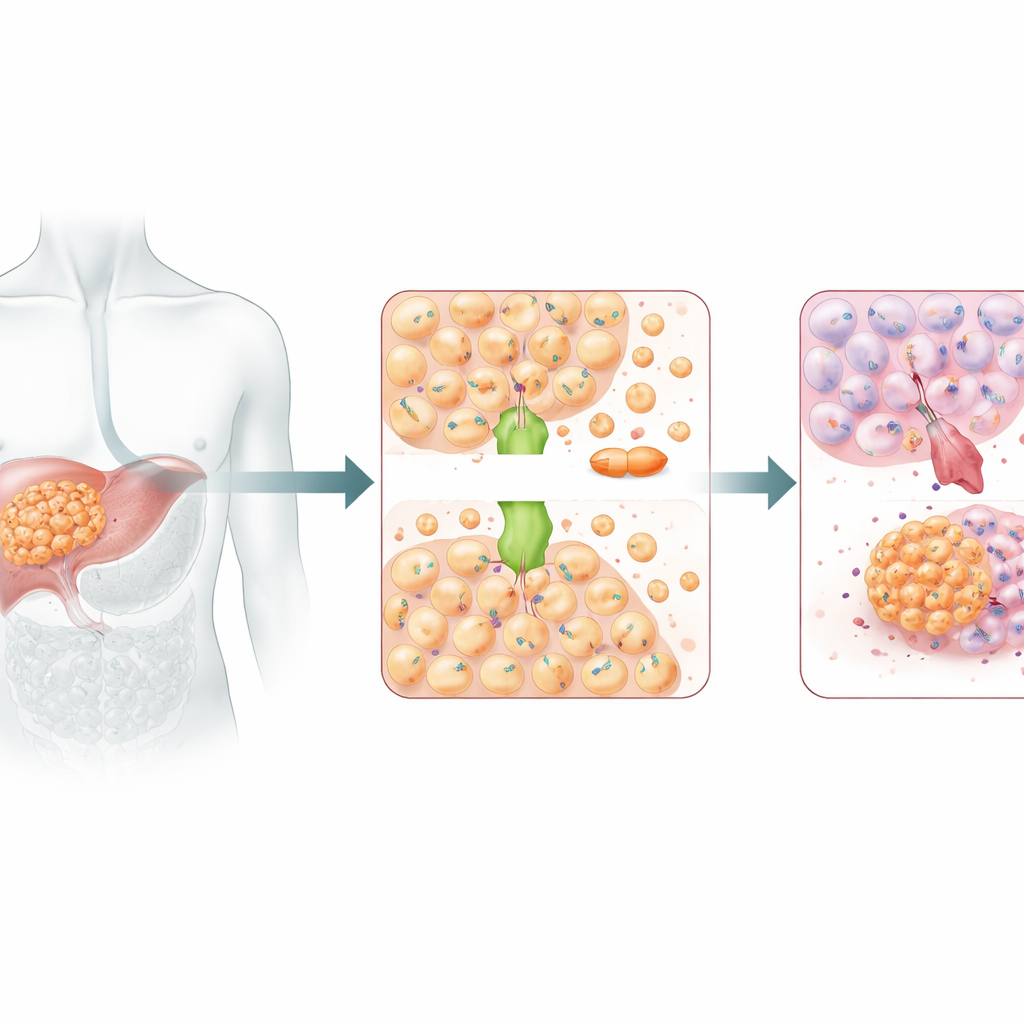
带有黑暗面向的铜运输者
ATOX1 通常充当铜的搬运者,在细胞内运输铜离子以维持铜的稳态。但铜与顺铂在某些方面相似,可能会共享部分运输通路。早期的结构研究提示 ATOX1 能够直接与顺铂结合。在本研究中,沉默 ATOX1 使肝癌细胞对顺铂更加脆弱:它们生长减慢、克隆形成减少、程序性细胞死亡增加。在携带人源肝肿瘤的小鼠模型中,敲低 ATOX1 也使顺铂更有效地缩小肿瘤。综合这些结果,表明 ATOX1 是帮助肝癌细胞抵御铂类化疗的关键因子。
设计精准抑制剂
研究团队没有采用广泛影响铜水平的方式(这可能有毒),而是着眼于直接阻断 ATOX1。他们在计算机上模拟 ATOX1 蛋白的运动,寻找可能结合药物的稳定口袋,然后对 150 万种小分子进行虚拟筛选以评价其契合度。经过多轮筛选和实验验证,出现了一个候选分子——称为化合物 8——作为强而特异的结合物。生物物理学检测显示,化合物 8 与 ATOX1 紧密结合并稳定其构象,同时对一个与之相关且旧抑制剂也会作用的铜蛋白影响甚微。细胞实验表明,与先前的 ATOX1 药物相比,化合物 8 对正常肝细胞的损伤更小,提示其安全窗更好,尽管单药抗癌活性仅为适中。
将铜反过来用于对付肿瘤
最显著的效果出现在化合物 8 与顺铂联用时。在培养皿中生长的肝癌细胞里,两药联合比任何单药都更能抑制生长、减少克隆形成并引发更高的细胞死亡率。在小鼠体内,联合用药产生了最小的肿瘤体积与最低的细胞增殖标志物水平,且未见主要器官的明显损伤。为了解机制,研究者分析了基因活性,发现阻断 ATOX1 导致癌细胞内铜积聚。铜的积累与一个名为 NOTCH1 的基因控制区上化学标记——DNA 甲基化的增加相关。更高的甲基化意味着 NOTCH1 的开关被下调,其下游伙伴基因 HES1 也被抑制。重要的是,使用铜螯合剂可以逆转这些变化,表明铜本身是该效应的关键。
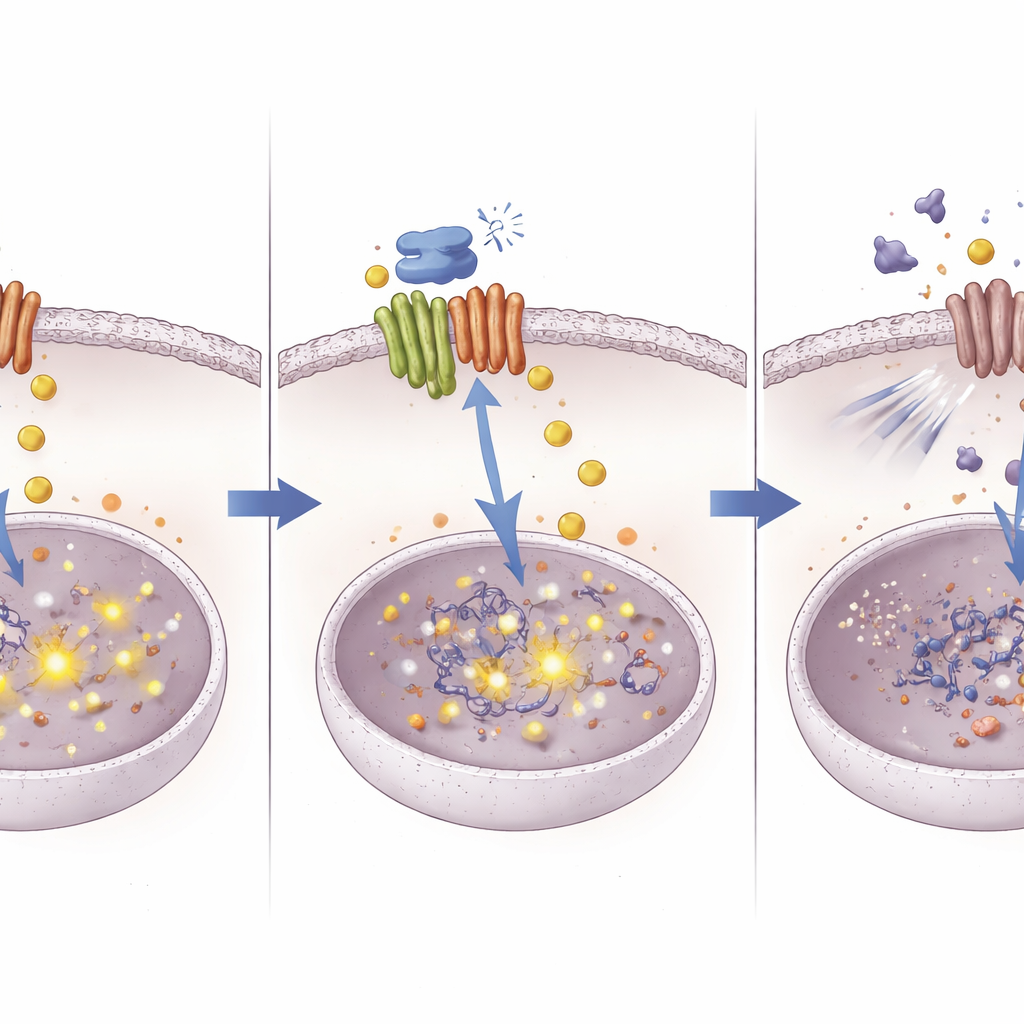
使老药更有效的一条新途径
通过追踪从铜搬运蛋白到生存通路的 DNA 级别变化的路径,这项研究勾勒出一种全新的策略来应对肝癌的化疗耐药。研究表明,ATOX1 使肿瘤能够以一种削弱顺铂效力的方式管理铜与信号传导。用化合物 8 阻断 ATOX1 导致铜积累,进而通过 DNA 甲基化沉默 NOTCH1,去掉了肿瘤对顺铂的重要屏障。尽管化合物 8 仍处于实验性分子阶段,但其体现的概念——精确靶向金属处理蛋白以重编程癌细胞行为——有望帮助恢复现有化疗的疗效并激发新的联用治疗思路。
引用: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
关键词: 肝癌, 顺铂耐药, 铜代谢, ATOX1 抑制剂, Notch 信号通路