Clear Sky Science · fr
Criblage CRISPR-Cas9 identifie des mécanismes de résistance au cisplatine dirigés par ATOX1 dans le cancer du foie et évalue l’efficacité d’un inhibiteur ciblé
Pourquoi cette recherche est importante
Le cancer du foie est l’un des cancers les plus meurtriers au monde, et de nombreux patients reçoivent un médicament de chimiothérapie courant appelé cisplatine. Avec le temps, cependant, les tumeurs apprennent souvent à résister au traitement, permettant à la maladie de réapparaître et de se propager. Cette étude met au jour un coupable moléculaire surprenant derrière cette résistance et présente un composé conçu qui pourrait aider le cisplatine à être plus efficace et plus sûr. Pour les lecteurs, elle offre un aperçu de la manière dont la génétique moderne, la modélisation informatique et la chimie peuvent être combinées pour déjouer les défenses du cancer.
Comment les tumeurs hépatiques échappent à la chimiothérapie
Le cisplatine tue les cellules cancéreuses en endommageant leur ADN, mais les tumeurs peuvent devenir résistantes par de nombreux mécanismes : expulser le médicament, réparer l’ADN plus rapidement ou réorienter les signaux de survie. Les auteurs ont utilisé un outil puissant d’édition génomique, un criblage CRISPR-Cas9 à l’échelle du génome, pour désactiver systématiquement presque tous les gènes dans deux lignées cellulaires de cancer du foie, puis les exposer au cisplatine. Ils se sont posé une question simple : lorsqu’un gène est inactivé, les cellules deviennent-elles plus ou moins sensibles au médicament ? Parmi des dizaines de gènes liés à la résistance, un s’est détaché — ATOX1, une petite protéine qui aide normalement les cellules à gérer le métal essentiel qu’est le cuivre. Les cellules de cancer du foie présentaient plus d’ATOX1 que les cellules hépatiques saines, et les patients dont les tumeurs montraient des niveaux élevés d’ATOX1 avaient tendance à avoir une survie plus mauvaise et davantage de résistance au cisplatine.
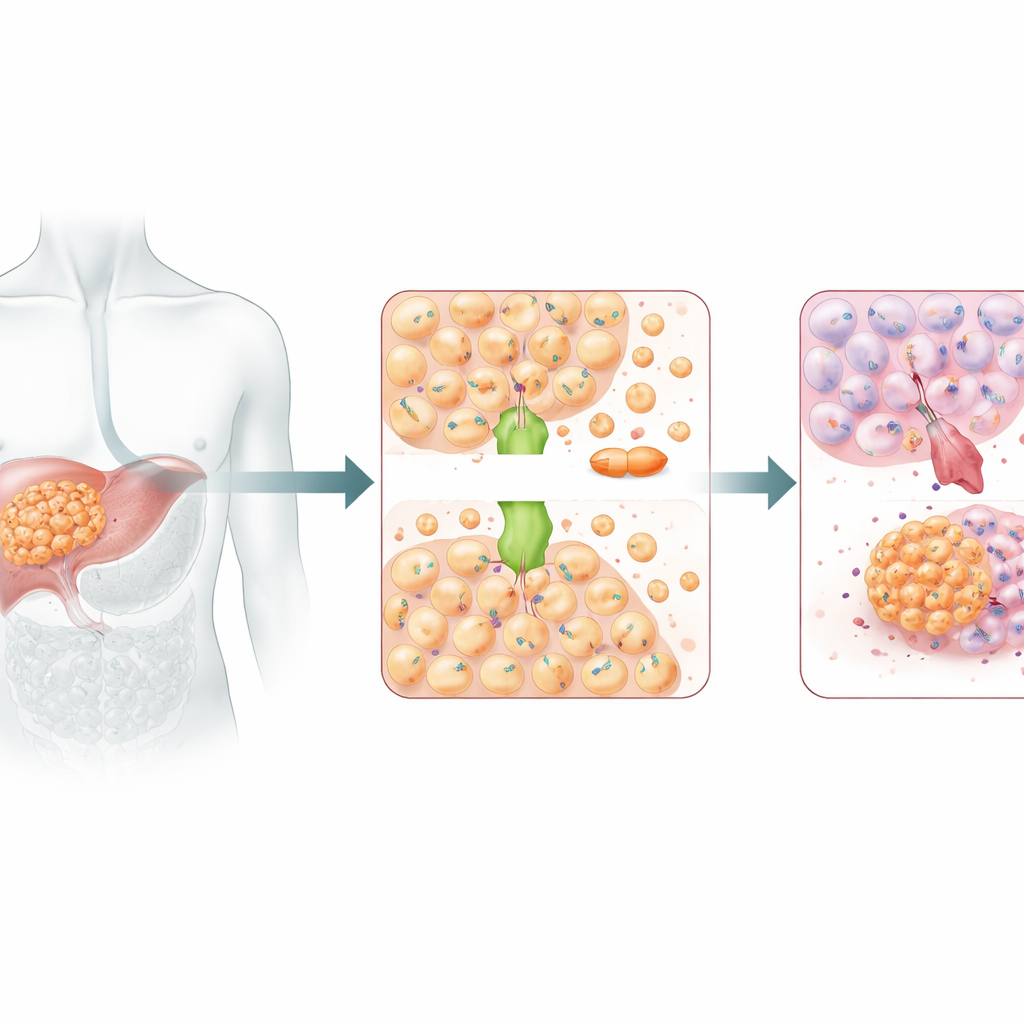
Un transporteur de cuivre au côté obscur
ATOX1 agit habituellement comme un transporteur de cuivre, acheminant des ions cuivre à l’intérieur des cellules pour maintenir l’équilibre de ce métal vital. Mais le cuivre et le cisplatine se ressemblent suffisamment pour emprunter certains des mêmes itinéraires de transport. Des travaux structuraux antérieurs laissaient entendre qu’ATOX1 peut se lier directement au cisplatine. Dans cette étude, l’inhibition d’ATOX1 dans des cellules de cancer du foie les rendait beaucoup plus vulnérables au cisplatine : leur croissance ralentissait, elles formaient moins de colonies et subissaient plus de mort cellulaire programmée. Chez des souris portant des tumeurs hépatiques humaines, l’abaissement d’ATOX1 a également renforcé l’effet réducteur du cisplatine sur les tumeurs. Ensemble, ces résultats désignent ATOX1 comme un auxiliaire clé permettant aux cellules du cancer du foie de résister à la chimiothérapie à base de platine.
Concevoir un bloqueur de précision
Plutôt que de cibler le cuivre de façon large, ce qui peut être toxique, l’équipe a cherché à bloquer ATOX1 lui‑même. Ils ont simulé le mouvement de la protéine ATOX1 sur ordinateur pour trouver des poches stables où une molécule thérapeutique pourrait se lier, puis ont testé virtuellement 1,5 million de petites molécules pour évaluer leur aptitude à s’emboîter. Après plusieurs séries de filtrages et de validations en laboratoire, un candidat — baptisé composé 8 — est apparu comme un ligand fort et spécifique. Des essais biophysiques ont montré que le composé 8 se liait étroitement à ATOX1 et stabilisait sa structure, tout en ayant peu d’effet sur une protéine de cuivre apparentée ciblée par des inhibiteurs plus anciens. Dans des tests cellulaires, le composé 8 était moins nocif pour les cellules hépatiques normales qu’un médicament ATOX1 précédent, suggérant une marge de sécurité améliorée bien que son activité anticancéreuse en monothérapie fût modeste.
Retourner le cuivre contre la tumeur
Les effets les plus marquants sont apparus lorsque le composé 8 était associé au cisplatine. Dans des cellules de cancer du foie cultivées en plaque, la combinaison des deux médicaments réduisait la croissance plus que l’un ou l’autre seul, diminuait la formation de colonies et augmentait les taux de mort cellulaire. Chez la souris, la combinaison a produit les plus petites tumeurs et les niveaux les plus faibles de marqueurs de division cellulaire, sans dommages apparents aux organes majeurs. Pour comprendre pourquoi, les chercheurs ont analysé l’activité génétique et ont constaté que le blocage d’ATOX1 provoquait une accumulation de cuivre à l’intérieur des cellules cancéreuses. Cette accumulation de cuivre était associée à une augmentation des marquages chimiques — la méthylation de l’ADN — sur la région de contrôle d’un gène appelé NOTCH1, partie d’une voie qui aide les cellules tumorales à survivre au stress et à réparer l’ADN. Une méthylation plus importante signifiait que l’interrupteur NOTCH1 était abaissé, et son gène partenaire HES1 était lui aussi calmé. Fait important, l’utilisation d’un chélateur du cuivre inversait ces changements, montrant que le cuivre lui‑même était central dans l’effet.
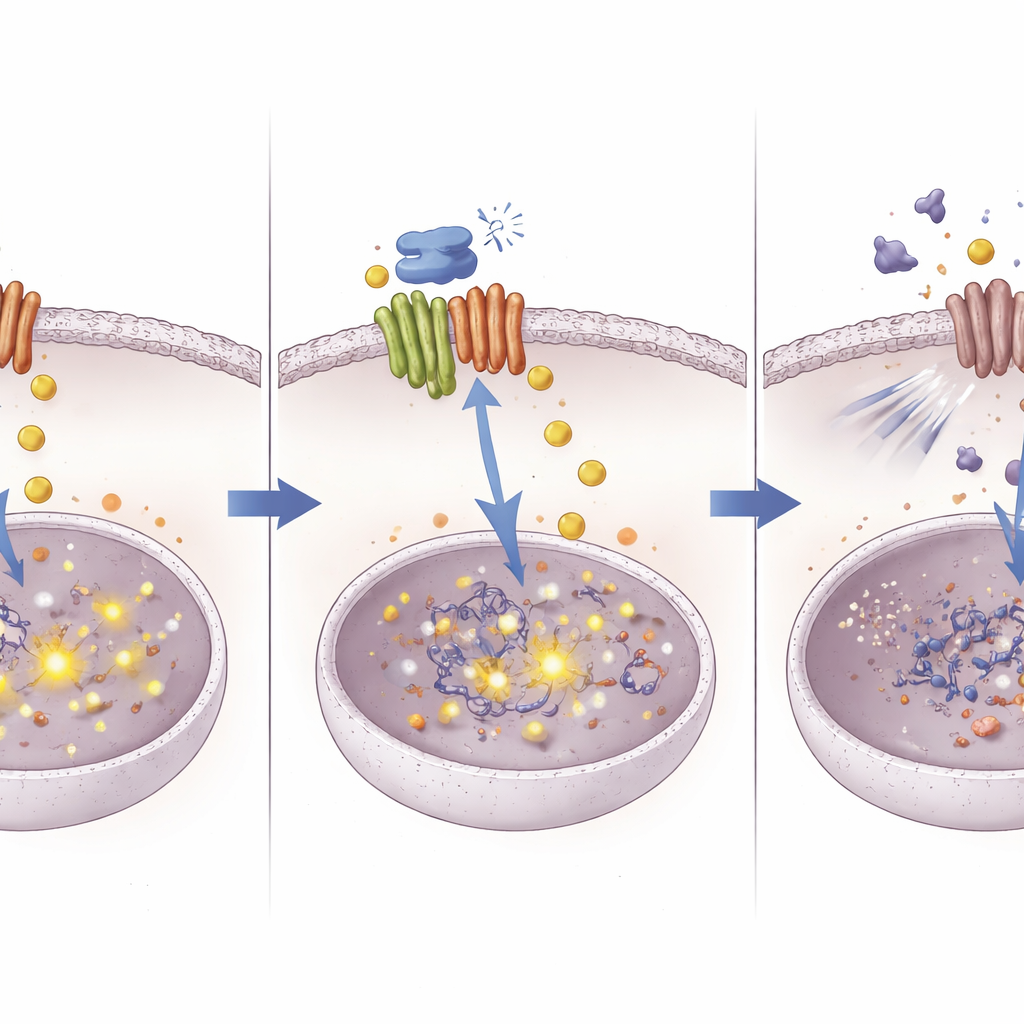
Une nouvelle voie pour améliorer des médicaments anciens
En retraçant le chemin d’un transporteur de cuivre jusqu’à des modifications au niveau de l’ADN dans une voie de survie, cette étude décrit une approche nouvelle pour combattre la résistance à la chimiothérapie dans le cancer du foie. Les travaux suggèrent qu’ATOX1 permet aux tumeurs de gérer le cuivre et la signalisation d’une manière qui atténue l’effet du cisplatine. Bloquer ATOX1 avec le composé 8 provoque l’accumulation de cuivre, qui à son tour silencie NOTCH1 via la méthylation de l’ADN et supprime un bouclier clé contre le cisplatine. Bien que le composé 8 reste une molécule expérimentale, le concept qu’il illustre — cibler précisément les protéines de gestion des métaux pour reprogrammer le comportement des cellules cancéreuses — pourrait contribuer à ranimer l’efficacité de chimiothérapies existantes et inspirer de nouvelles combinaisons thérapeutiques.
Citation: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Mots-clés: cancer du foie, résistance au cisplatine, métabolisme du cuivre, inhibiteur d’ATOX1, signalisation Notch