Clear Sky Science · it
Screening CRISPR-Cas9 identifica meccanismi di resistenza al cisplatino guidati da ATOX1 nel cancro del fegato e valuta l’efficacia di un inibitore mirato
Perché questa ricerca è importante
Il cancro del fegato è uno dei tumori più letali a livello mondiale e molti pazienti ricevono un farmaco chemioterapico comunemente usato, il cisplatino. Col tempo, però, i tumori spesso sviluppano resistenza al farmaco, permettendo alla malattia di ricomparire e diffondersi. Questo studio individua un sorprendente colpevole molecolare alla base di quella resistenza e presenta un composto progettato che potrebbe migliorare l’efficacia e la sicurezza del cisplatino. Per il lettore, offre uno sguardo su come genetica moderna, modellazione al computer e chimica possano essere combinate per superare le difese del cancro.
Come i tumori epatici eludono la chemioterapia
Il cisplatino uccide le cellule tumorali danneggiandone il DNA, ma i tumori possono diventare resistenti con molte strategie: espellendo il farmaco, riparando il DNA più rapidamente o riorganizzando segnali di sopravvivenza. Gli autori hanno usato un potente strumento di editing genetico, uno screening genome-wide con CRISPR-Cas9, per spegnere sistematicamente quasi tutti i geni in due linee cellulari di cancro del fegato e poi esporle al cisplatino. Hanno posto una semplice domanda: quando un gene viene eliminato, le cellule diventano più o meno sensibili al farmaco? Tra dozzine di geni collegati alla resistenza, uno è emerso in modo netto—ATOX1, una piccola proteina che normalmente aiuta le cellule a gestire il metallo essenziale rame. Le cellule di cancro epatico presentavano livelli di ATOX1 maggiori rispetto alle cellule epatiche sane, e i pazienti i cui tumori mostravano alti livelli di ATOX1 tendevano ad avere una sopravvivenza peggiore e maggiore resistenza al cisplatino.
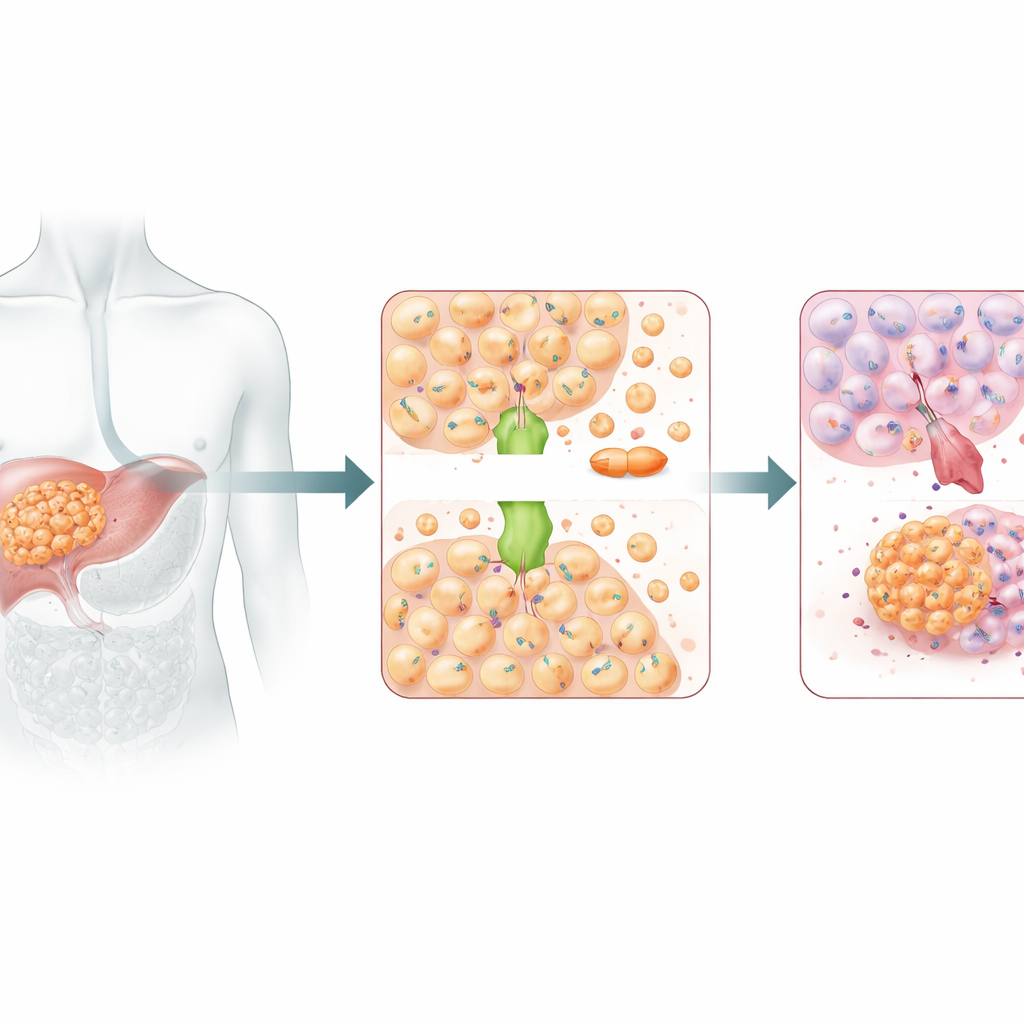
Un corriere del rame dal lato oscuro
ATOX1 normalmente agisce come corriere del rame, trasportando ioni rame all’interno delle cellule per mantenere l’equilibrio di questo metallo vitale. Ma rame e cisplatino sono abbastanza simili da poter usare in parte gli stessi percorsi di trasporto. Lavori strutturali precedenti avevano suggerito che ATOX1 può legare direttamente il cisplatino. In questo studio, silenziare ATOX1 nelle cellule tumorali del fegato le rendeva molto più vulnerabili al cisplatino: la loro crescita rallentava, formavano meno colonie e andavano incontro a più morte cellulare programmata. Anche nei topi portatori di tumori umani al fegato, l’abbattimento di ATOX1 ha reso il cisplatino più efficace nel ridurre le dimensioni dei tumori. Nel complesso, questi risultati indicano ATOX1 come un collaboratore chiave che permette alle cellule tumorali epatiche di resistere alla chemioterapia a base di platino.
Progettare un bloccante di precisione
Piuttosto che colpire il rame in modo ampio, cosa che può essere tossica, il gruppo ha mirato a bloccare ATOX1 stesso. Hanno simulato al computer il movimento della proteina ATOX1 per trovare tasche stabili dove un farmaco potrebbe legarsi, quindi hanno testato virtualmente 1,5 milioni di piccole molecole per valutarne l’idoneità. Dopo diverse fasi di filtraggio e validazione di laboratorio, è emerso un candidato—battezzato composto 8—come legante forte e specifico. Saggi biofisici hanno mostrato che il composto 8 si legava saldamente ad ATOX1 e stabilizzava la sua struttura, pur avendo poco effetto su una proteina del rame correlata che gli inibitori più vecchi colpivano. Nei test cellulari, il composto 8 era meno dannoso per le cellule epatiche normali rispetto a un precedente farmaco contro ATOX1, suggerendo un margine di sicurezza migliore anche se la sua attività anticancro come agente singolo era modesta.
Usare il rame contro il tumore
Gli effetti più evidenti sono comparsi quando il composto 8 è stato associato al cisplatino. Nelle cellule di cancro del fegato coltivate in piastre, la combinazione dei due farmaci riduceva la crescita più di ciascuno da solo, diminuiva la formazione di colonie e induceva tassi maggiori di morte cellulare. Nei topi, la combinazione ha prodotto i tumori più piccoli e i livelli più bassi di marcatori di divisione cellulare, senza danni evidenti agli organi principali. Per capire il motivo, i ricercatori hanno analizzato l’attività genica e hanno scoperto che bloccare ATOX1 causava l’accumulo di rame all’interno delle cellule tumorali. Quel accumulo di rame era associato a un aumento dei segni chimici—metilazione del DNA—nella regione di controllo di un gene chiamato NOTCH1, parte di una via che aiuta le cellule tumorali a sopravvivere allo stress e a riparare il DNA. Una metilazione più intensa significava che l’interruttore di NOTCH1 veniva abbassato, e anche il suo gene partner HES1 si quietava. È importante che l’uso di un composto che chelava il rame invertisse questi cambiamenti, mostrando che è stato il rame stesso a essere centrale nell’effetto.
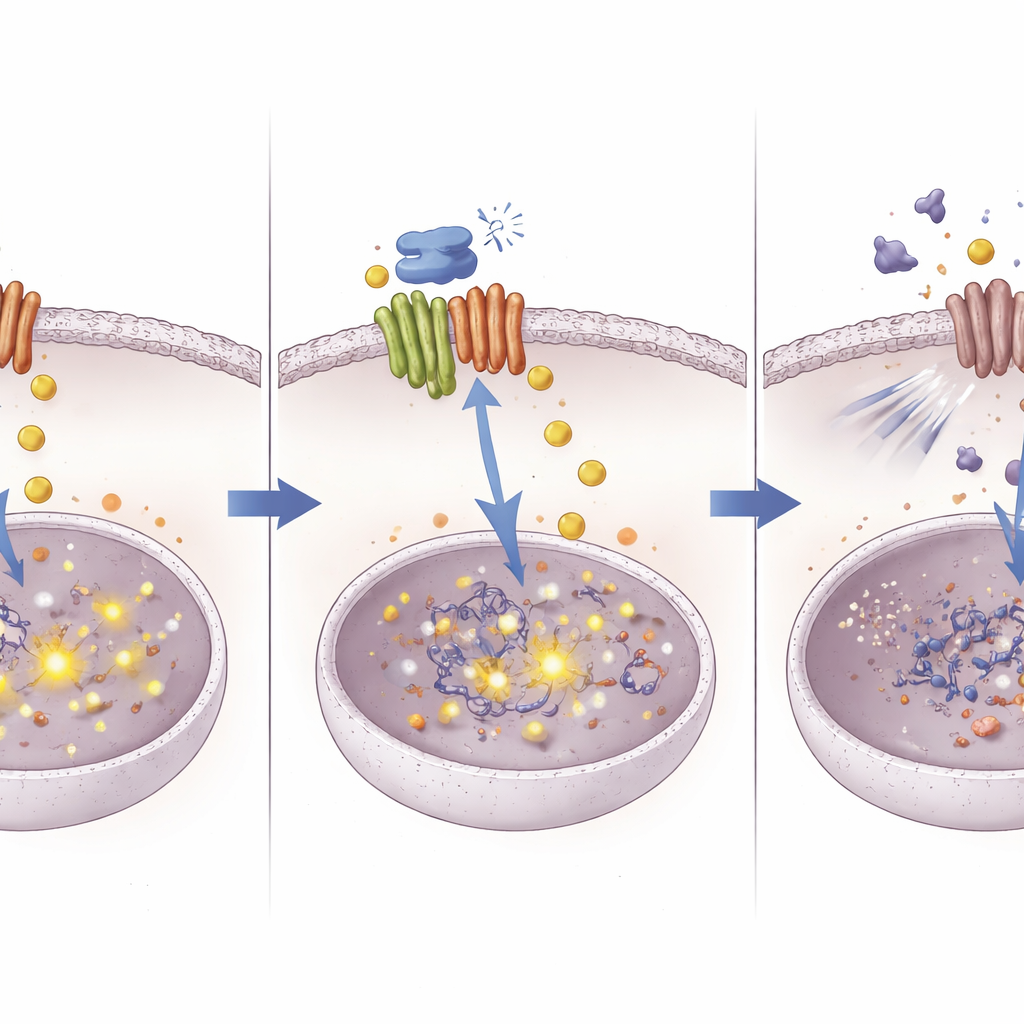
Una nuova via per far funzionare meglio farmaci vecchi
Tracciando il percorso da una proteina corriere del rame fino a cambiamenti a livello del DNA in una via di sopravvivenza, questo studio delinea un approccio nuovo per affrontare la resistenza alla chemioterapia nel cancro del fegato. Il lavoro suggerisce che ATOX1 permette ai tumori di gestire rame e segnali in modo da attenuare l’efficacia del cisplatino. Bloccare ATOX1 con il composto 8 provoca l’accumulo di rame, che a sua volta silenzia NOTCH1 tramite metilazione del DNA e rimuove una protezione chiave contro il cisplatino. Sebbene il composto 8 sia ancora una molecola sperimentale, il concetto che incarna—colpire con precisione le proteine che gestiscono i metalli per rimodellare il comportamento delle cellule tumorali—potrebbe contribuire a ridare efficacia a chemioterapie esistenti e ispirare nuove terapie combinate.
Citazione: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Parole chiave: cancro del fegato, resistenza al cisplatino, metabolismo del rame, inibitore di ATOX1, segnalazione Notch