Clear Sky Science · pt
Triagem CRISPR-Cas9 identifica mecanismos de resistência ao cisplatina dirigidos por ATOX1 no câncer de fígado e avalia a eficácia de um inibidor específico
Por que esta pesquisa é importante
O câncer de fígado é um dos cânceres mais letais no mundo, e muitos pacientes recebem um quimioterápico comum chamado cisplatina. Com o tempo, porém, os tumores frequentemente aprendem a resistir ao fármaco, permitindo que a doença retorne e se espalhe. Este estudo revela um culpado molecular surpreendente por trás dessa resistência e apresenta um composto projetado que pode ajudar a tornar a cisplatina mais eficaz e mais segura. Para os leitores, oferece um vislumbre de como genética moderna, modelagem computacional e química podem ser combinadas para superar as defesas do câncer.
Como tumores hepáticos escapam da quimioterapia
A cisplatina mata células cancerosas danificando seu DNA, mas os tumores podem se tornar resistentes por vários artifícios: bombear o fármaco para fora, reparar o DNA mais rapidamente ou reprogramar sinais de sobrevivência. Os autores usaram uma poderosa ferramenta de edição gênica, uma triagem genômica CRISPR-Cas9, para desligar sistematicamente quase todos os genes em duas linhagens de células de câncer de fígado e então expô-las à cisplatina. Eles fizeram uma pergunta simples: quando um gene é desativado, as células se tornam mais ou menos sensíveis ao fármaco? Entre dezenas de genes ligados à resistência, um se destacou—ATOX1, uma pequena proteína que normalmente ajuda as células a lidar com o metal essencial cobre. Células de câncer de fígado tinham mais ATOX1 do que células hepáticas saudáveis, e pacientes cujos tumores exibiam altos níveis de ATOX1 tendiam a ter pior sobrevida e maior resistência à cisplatina.
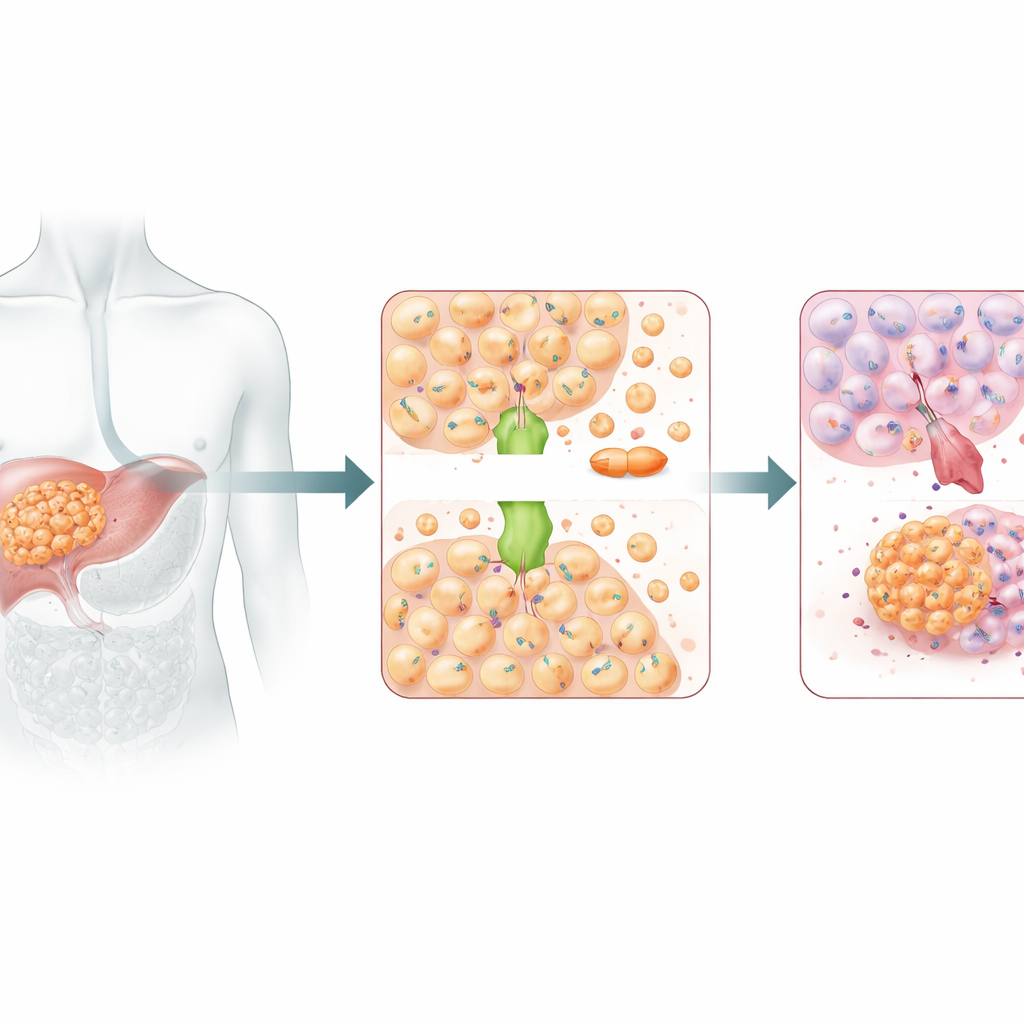
Um mensageiro do cobre com um lado sombrio
ATOX1 geralmente age como um mensageiro do cobre, transportando íons de cobre dentro das células para manter esse metal vital em equilíbrio. Mas cobre e cisplatina são semelhantes o suficiente para possivelmente trafegar por algumas das mesmas rotas de transporte. Trabalhos estruturais anteriores indicaram que ATOX1 pode se ligar diretamente à cisplatina. Neste estudo, silenciar ATOX1 em células de câncer de fígado as tornou muito mais vulneráveis à cisplatina: seu crescimento diminuiu, formaram menos colônias e apresentaram mais morte celular programada. Em camundongos com tumores humanos de fígado, reduzir ATOX1 também fez com que a cisplatina encolhesse os tumores com mais eficácia. Juntos, esses resultados apontaram ATOX1 como um ajudante-chave que permite que células de câncer de fígado resistam à quimioterapia à base de platina.
Desenvolvendo um bloqueador de precisão
Em vez de direcionar o cobre de forma ampla, o que pode ser tóxico, a equipe buscou bloquear o próprio ATOX1. Eles simularam o movimento da proteína ATOX1 em computador para encontrar bolsões estáveis onde um fármaco poderia se ligar, depois testaram virtualmente 1,5 milhão de pequenas moléculas quanto à sua capacidade de se encaixar. Após várias rodadas de filtragem e validação em laboratório, um candidato—apelidado de composto 8—surgiu como um ligante forte e específico. Ensaios biofísicos mostraram que o composto 8 se ligava firmemente ao ATOX1 e estabilizava sua estrutura, tendo pouco efeito sobre uma proteína de cobre relacionada que inibidores mais antigos também atingiam. Em testes celulares, o composto 8 foi menos danoso para células hepáticas normais do que um fármaco anterior para ATOX1, sugerindo uma margem de segurança melhor, embora sua atividade anticâncer isolada tenha sido modesta.
Virando o cobre contra o tumor
Os efeitos mais marcantes apareceram quando o composto 8 foi combinado com a cisplatina. Em células de câncer de fígado cultivadas em placa, a combinação dos dois fármacos reduziu o crescimento mais do que cada um isoladamente, diminuiu a formação de colônias e desencadeou taxas maiores de morte celular. Em camundongos, a combinação produziu os menores tumores e os níveis mais baixos de marcadores de divisão celular, sem danos óbvios aos principais órgãos. Para entender por quê, os pesquisadores analisaram a atividade gênica e descobriram que bloquear o ATOX1 causou acúmulo de cobre dentro das células cancerosas. Esse acúmulo de cobre foi associado a aumento de marcas químicas—metilação do DNA—na região de controle de um gene chamado NOTCH1, parte de uma via que ajuda células tumorais a sobreviver ao estresse e reparar o DNA. Metilação mais intensa significou que o interruptor de NOTCH1 foi reduzido, e seu gene parceiro HES1 também silenciou. Importante, usar um composto quelante de cobre reverteu essas alterações, demonstrando que o próprio cobre era central para o efeito.
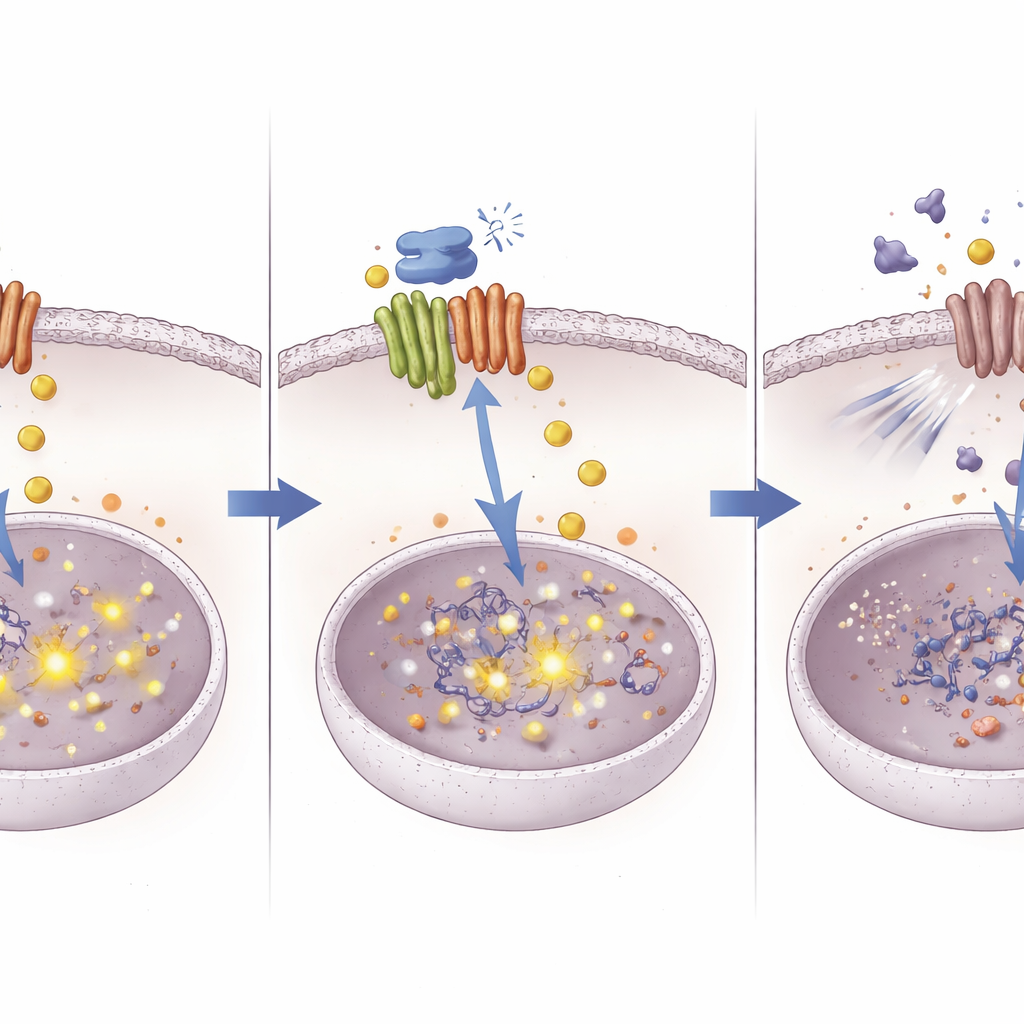
Uma nova rota para melhorar drogas antigas
Ao traçar o caminho de uma proteína mensageira do cobre até mudanças ao nível do DNA em uma via de sobrevivência, este estudo descreve uma abordagem inédita para enfrentar a resistência à quimioterapia no câncer de fígado. O trabalho sugere que ATOX1 permite que os tumores gerenciem cobre e sinalização de maneira que atenua o efeito da cisplatina. Bloquear o ATOX1 com o composto 8 faz o cobre se acumular, o que por sua vez silencia NOTCH1 por meio da metilação do DNA e remove um escudo chave contra a cisplatina. Embora o composto 8 ainda seja uma molécula experimental, o conceito que ele representa—alvo preciso em proteínas que manipulam metais para reprogramar o comportamento das células cancerosas—poderia ajudar a reviver a eficácia de quimioterapias existentes e inspirar novos tratamentos combinados.
Citação: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Palavras-chave: câncer de fígado, resistência ao cisplatina, metabolismo do cobre, inibidor de ATOX1, sinalização Notch