Clear Sky Science · de
CRISPR-Cas9-Screening identifiziert ATOX1-getriebene Cisplatin-Resistenzmechanismen beim Leberkrebs und bewertet die Wirksamkeit eines zielgerichteten Inhibitors
Warum diese Forschung wichtig ist
Leberkrebs gehört zu den tödlichsten Krebsarten weltweit, und viele Patientinnen und Patienten erhalten das häufig eingesetzte Chemotherapeutikum Cisplatin. Im Laufe der Zeit lernen Tumoren jedoch oft, dem Medikament zu widerstehen, wodurch die Krankheit zurückkehren und sich ausbreiten kann. Diese Studie deckt einen überraschenden molekularen Verantwortlichen für diese Resistenz auf und stellt eine synthetisch entwickelte Verbindung vor, die Cisplatin wirksamer und potenziell sicherer machen könnte. Für Leserinnen und Leser bietet sie einen Einblick, wie moderne Genetik, Computermodellierung und Chemie kombiniert werden können, um die Verteidigungsmechanismen des Krebses zu überlisten.
Wie Lebertumoren die Chemotherapie umgehen
Cisplatin tötet Krebszellen, indem es ihre DNA schädigt, doch Tumoren können auf verschiedenen Wegen resistent werden: durch aktiven Austransport des Wirkstoffs, schnellere DNA-Reparatur oder Umprogrammierung von Überlebenssignalen. Die Autorinnen und Autoren nutzten ein leistungsfähiges Geneditierwerkzeug, ein genomweites CRISPR-Cas9-Screening, um systematisch nahezu jedes Gen in zwei Leberkrebszelllinien auszuschalten und die Zellen anschließend Cisplatin auszusetzen. Die Fragestellung war einfach: Führt der Verlust eines Gens dazu, dass Zellen gegenüber dem Medikament empfindlicher oder widerstandsfähiger werden? Unter Dutzenden von Genen, die mit Resistenz assoziiert waren, stach ein Gen besonders hervor—ATOX1, ein kleines Protein, das normalerweise dabei hilft, das essentielle Metall Kupfer in der Zelle zu handhaben. Leberkrebszellen zeigten höhere ATOX1-Spiegel als gesunde Leberzellen, und Patientinnen und Patienten, deren Tumoren erhöhte ATOX1-Werte aufwiesen, hatten tendenziell schlechteres Überleben und stärkere Cisplatin-Resistenz.
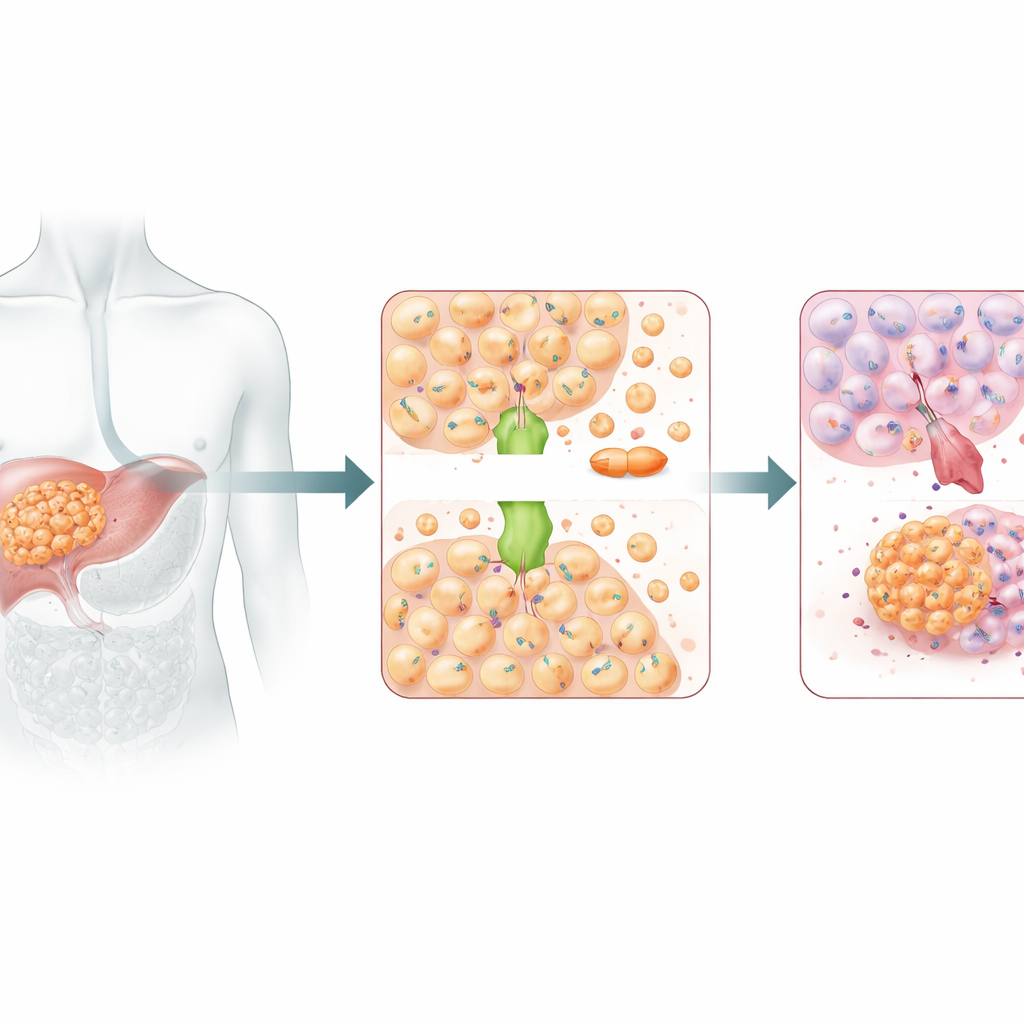
Ein Kupferkurier mit Schattenseiten
ATOX1 fungiert normalerweise als Kupferkurier und transportiert Kupferionen in der Zelle, um dieses wichtige Metall im Gleichgewicht zu halten. Kupfer und Cisplatin ähneln sich jedoch so sehr, dass sie einige derselben Transportwege nutzen könnten. Frühere Strukturarbeiten deuteten bereits an, dass ATOX1 Cisplatin direkt binden kann. In dieser Studie machte die Stilllegung von ATOX1 Leberkrebszellen deutlich anfälliger für Cisplatin: ihr Wachstum verlangsamte sich, sie bildeten weniger Kolonien und zeigten vermehrt programmierte Zellsterblichkeit. Auch in Mäusen mit humanen Lebertumoren führte die Herunterregulierung von ATOX1 dazu, dass Cisplatin Tumoren wirksamer verkleinerte. Zusammengenommen deuteten diese Ergebnisse darauf hin, dass ATOX1 ein entscheidender Helfer ist, der Leberkrebszellen das Überstehen einer platinhaltigen Chemotherapie erleichtert.
Entwicklung eines präzisen Blockers
Anstatt Kupfer breit anzugreifen, was toxisch sein kann, strebte das Team an, ATOX1 direkt zu blockieren. Sie simulierten die Bewegung des ATOX1-Proteins im Computer, um stabile Taschen zu finden, an die ein Wirkstoff binden könnte, und testeten dann virtuell 1,5 Millionen kleine Moleküle auf ihre Passfähigkeit. Nach mehreren Filterrunden und Validierung im Labor kristallisierte sich ein Kandidat—mit der Bezeichnung Verbindung 8—als starker und spezifischer Binder heraus. Biophysikalische Tests zeigten, dass Verbindung 8 fest an ATOX1 anband und dessen Struktur stabilisierte, während sie wenig Einfluss auf ein verwandtes Kupferprotein hatte, das ältere Inhibitoren ebenfalls treffen. In Zelltests war Verbindung 8 weniger schädlich für normale Leberzellen als ein früheres ATOX1-Medikament, was eine bessere Sicherheitsmarge nahelegt, obwohl seine alleinige krebshemmende Wirkung moderat blieb.
Das Kupfer gegen den Tumor wenden
Die eindrücklichsten Effekte traten auf, wenn Verbindung 8 mit Cisplatin kombiniert wurde. In in vitro kultivierten Leberkrebszellen schnitt die Kombination besser ab als jede Einzelsubstanz: stärkeres Wachstumshemmen, reduzierte Koloniebildung und höhere Raten an Zellsterben. In Mäusen führten die beiden zusammen zu den kleinsten Tumoren und den niedrigsten Werten von Teilungsmarkern, ohne offensichtliche Schädigung wichtiger Organe. Um die Ursache zu klären, analysierten die Forschenden die Genaktivität und stellten fest, dass die Blockade von ATOX1 zu einer Kupferanreicherung innerhalb der Krebszellen führte. Diese Kupferakkumulation hing mit erhöhten chemischen Markierungen—DNA-Methylierung—im Kontrollbereich des Gens NOTCH1 zusammen, das zu einem Signalweg gehört, der Tumorzellen beim Umgang mit Stress und DNA-Reparatur unterstützt. Stärkere Methylierung führte zu einer Absenkung des NOTCH1-Schalters, und auch das Partnergen HES1 wurde leiser geschaltet. Wichtig: Der Einsatz einer kupferbindenden (chelatisierenden) Verbindung kehrte diese Veränderungen um und zeigte damit, dass gerade das Kupfer zentral für den beobachteten Effekt war.
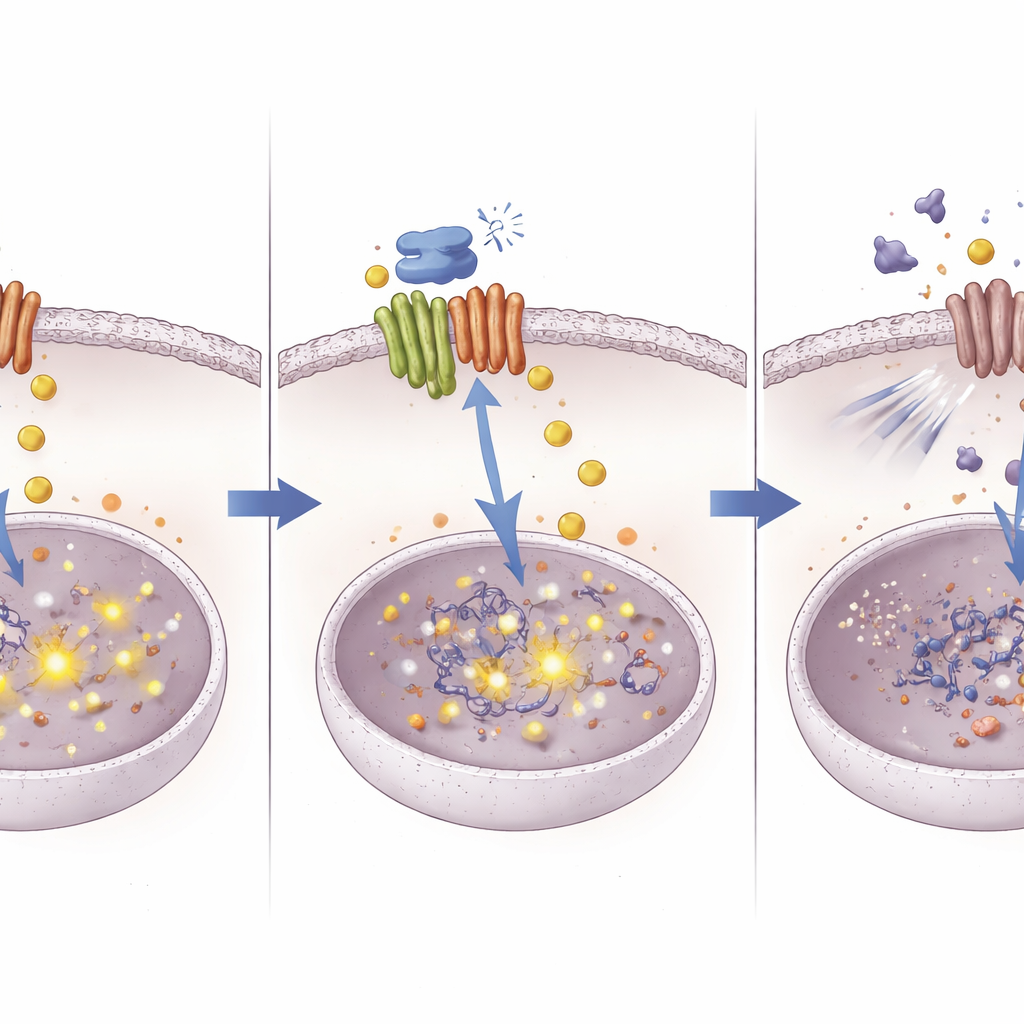
Ein neuer Weg, alte Medikamente wirksamer zu machen
Indem die Studie den Weg von einem Kupferkurierprotein bis hin zu DNA-Ebenen-Veränderungen in einem Überlebensweg nachzeichnet, skizziert sie einen neuen Ansatz, um Chemoresistenz beim Leberkrebs anzugehen. Die Arbeit legt nahe, dass ATOX1 Tumoren dabei hilft, Kupfer und Signalwege so zu regulieren, dass die Wirkung von Cisplatin abgeschwächt wird. Die Blockade von ATOX1 durch Verbindung 8 führt zur Kupferakkumulation, die wiederum NOTCH1 über DNA-Methylierung stilllegt und damit einen wichtigen Schutzschild gegen Cisplatin entfernt. Obwohl Verbindung 8 noch ein experimentelles Molekül ist, könnte das zugrunde liegende Konzept—das präzise Anvisieren von Metall‑Handhabungsproteinen, um das Verhalten von Krebszellen umzuprogrammieren—dazu beitragen, die Wirksamkeit vorhandener Chemotherapien wiederzubeleben und neue Kombinationsbehandlungen anzustoßen.
Zitation: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Schlüsselwörter: Leberkrebs, Cisplatin-Resistenz, Kupferstoffwechsel, ATOX1-Inhibitor, Notch-Signalgebung