Clear Sky Science · tr
CRISPR-Cas9 taraması, karaciğer kanserinde ATOX1 kaynaklı sisplatin direnç mekanizmalarını tanımlıyor ve hedefe yönelik inhibitör etkinliğini değerlendiriyor
Bu araştırma neden önemli
Karaciğer kanseri dünya çapında en ölümcül kanserlerden biridir ve birçok hasta sisplatin adı verilen yaygın bir kemoterapi ilacı alır. Ancak zamanla tümörler sıklıkla ilaca karşı direnç geliştirmeyi öğrenir; bu da hastalığın geri dönmesine ve yayılmasına izin verir. Bu çalışma, bu direncin arkasındaki beklenmedik moleküler bir suçluyu ortaya koyuyor ve sisplatinin daha etkili ve daha güvenli çalışmasına yardımcı olabilecek tasarım bir bileşiği tanıtıyor. Okuyucular için, modern genetik, bilgisayar modelleme ve kimyanın kanserin savunmalarını aşmak için nasıl birleştirilebileceğine dair bir pencere sunuyor.
Karaciğer tümörleri kemoterapiden nasıl kaçıyor
Sisplatin kanser hücrelerini DNA’larını hasara uğratarak öldürür, ancak tümörler ilacı dışarı pompalama, DNA’yı daha hızlı tamir etme veya hayatta kalma sinyallerini yeniden düzenleme gibi birçok hileyle dirençli hale gelebilir. Yazarlar, güçlü bir gen düzenleme aracı olan genom çapında bir CRISPR‑Cas9 taraması kullanarak iki karaciğer kanseri hücre hattındaki neredeyse her geni sistematik olarak kapattı ve ardından hücreleri sisplatine maruz bıraktı. Basit bir soru sordular: bir gen devre dışı bırakıldığında hücreler ilaca karşı daha mı hassaslaşıyor yoksa daha mı dirençli oluyor? Dirençle ilişkili onlarca gen arasından bir gen öne çıktı—ATOX1, normalde hücrelerin temel metal bakırı işlemesine yardımcı olan küçük bir protein. Karaciğer kanseri hücrelerinde, sağlıklı karaciğer hücrelerine göre daha fazla ATOX1 vardı ve tümörlerinde yüksek ATOX1 seviyeleri görülen hastalar genellikle daha kötü sağkalım ve daha fazla sisplatin direnci gösteriyordu.
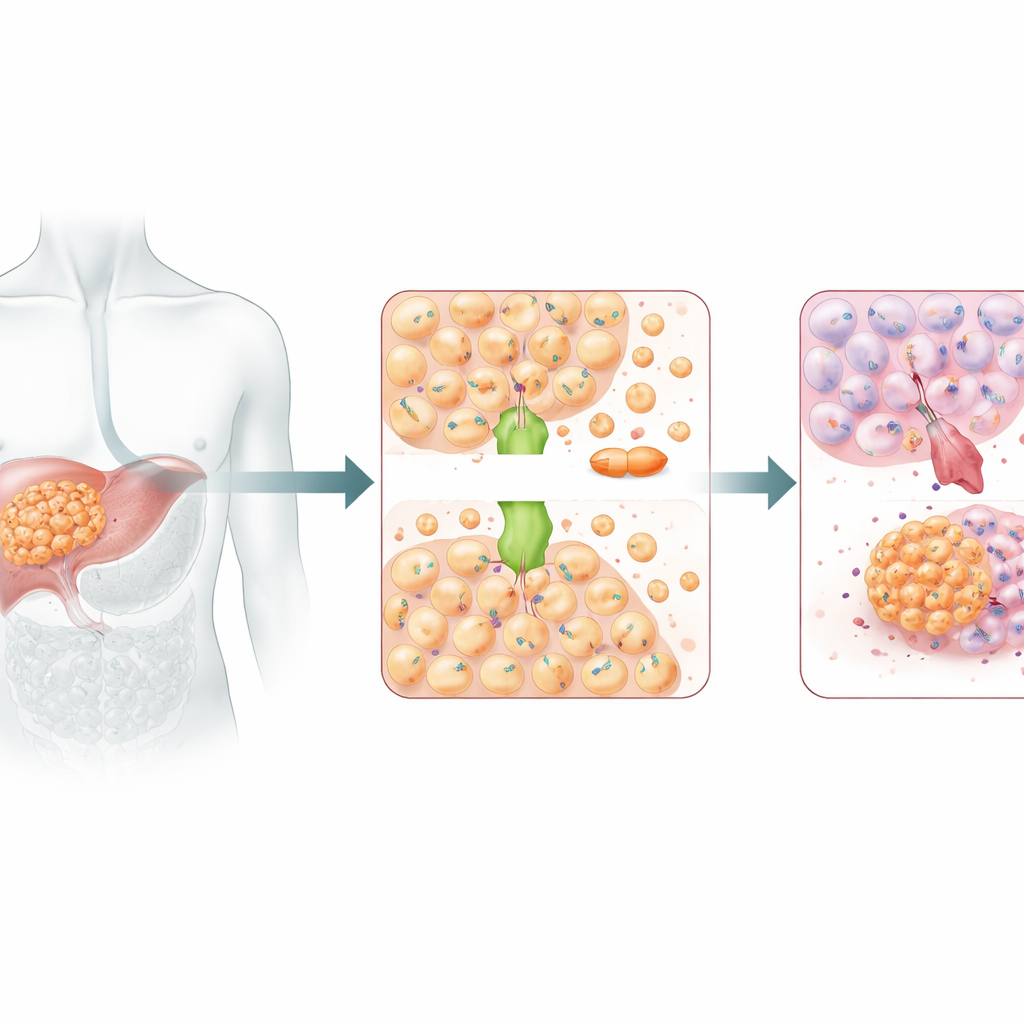
Karanlık tarafı olan bir bakır kuryesi
ATOX1 genellikle hücre içinde bakır iyonlarını taşıyan bir bakır kuryesi olarak görev yapar ve bu hayati metalin dengesini korur. Ancak bakır ile sisplatin birbirine yeterince benzeyebilir ve bazı ortak taşıma yollarını kullanabilirler. Önceki yapısal çalışmalar ATOX1’in sisplatine doğrudan bağlanabileceğine işaret etmişti. Bu çalışmada, karaciğer kanseri hücrelerinde ATOX1 susturulduğunda hücreler sisplatine karşı çok daha savunmasız hale geldi: büyümeleri yavaşladı, daha az kolon oluşturdular ve daha fazla programlı hücre ölümü geçirdiler. İnsan karaciğer tümörleri taşıyan farelerde ATOX1’in baskılanması da sisplatinin tümörleri daha etkili küçültmesini sağladı. Birlikte, bu sonuçlar ATOX1’i karaciğer kanseri hücrelerinin platin bazlı kemoterapiye dayanmasına olanak tanıyan kilit bir yardımcı olarak işaretledi.
Hassas bir engelleyici tasarlamak
Bakırı geniş çapta hedeflemek toksik olabileceğinden ekip doğrudan ATOX1’i engellemeyi amaçladı. Bir bilgisayarda ATOX1 proteininin hareketlerini simüle ederek bir ilacın bağlanabileceği stabil cepleri buldular, ardından 1,5 milyon küçük molekülü sanal olarak bu ceplere uyma yetenekleri açısından test ettiler. Birkaç eleme ve laboratuvar doğrulama turunun ardından bir aday—bileşik 8—güçlü ve spesifik bir bağlayıcı olarak öne çıktı. Biyofiziksel testler, bileşik 8’in ATOX1’e sıkı bağlandığını ve yapısını stabilize ettiğini gösterdi; bununla birlikte daha eski inhibitörlerin etkilediği ilişkili bir bakır protein üzerinde çok az etkisi vardı. Hücre testlerinde, bileşik 8 önceki bir ATOX1 ilacına göre normal karaciğer hücrelerine daha az zarar veriyordu; bu da tek başına anticancer aktivitesi sınırlı olsa da daha iyi bir güvenlik marjı olabileceğini düşündürdü.
Bakırı tümöre karşı çevirmek
En çarpıcı etkiler bileşik 8 ile sisplatinin birlikte kullanıldığı durumlarda ortaya çıktı. Petri kaplarında yetiştirilen karaciğer kanseri hücrelerinde iki ilacın kombinasyonu, tek başına verilenlerden daha fazla büyümeyi kesti, kolon oluşumunu azalttı ve daha yüksek hücre ölümü oranları tetikledi. Farelerde kombinasyon en küçük tümörleri ve en düşük hücre bölünme belirteç seviyelerini üretti; büyük organlarda bariz bir zarar görülmedi. Bunun neden olduğunu anlamak için araştırmacılar gen etkinliğini analiz etti ve ATOX1’in bloke edilmesinin kanser hücreleri içinde bakır birikimine yol açtığını buldu. Bu bakır birikimi, NOTCH1 adlı ve tümör hücrelerinin strese karşı hayatta kalmasına ve DNA’yı onarmasına yardımcı olan yolun kontrol bölgesinde artmış kimyasal işaretler—DNA metilasyonu—ile bağlantılıydı. Artan metilasyon, NOTCH1 anahtarının kapandığı anlamına geliyordu ve onun eşlik eden geni HES1 de sessizleşti. Önemli olarak, bir bakır şelatörünün kullanılması bu değişiklikleri tersine çevirdi ve etkinin merkezinde bakırın olduğunu gösterdi.
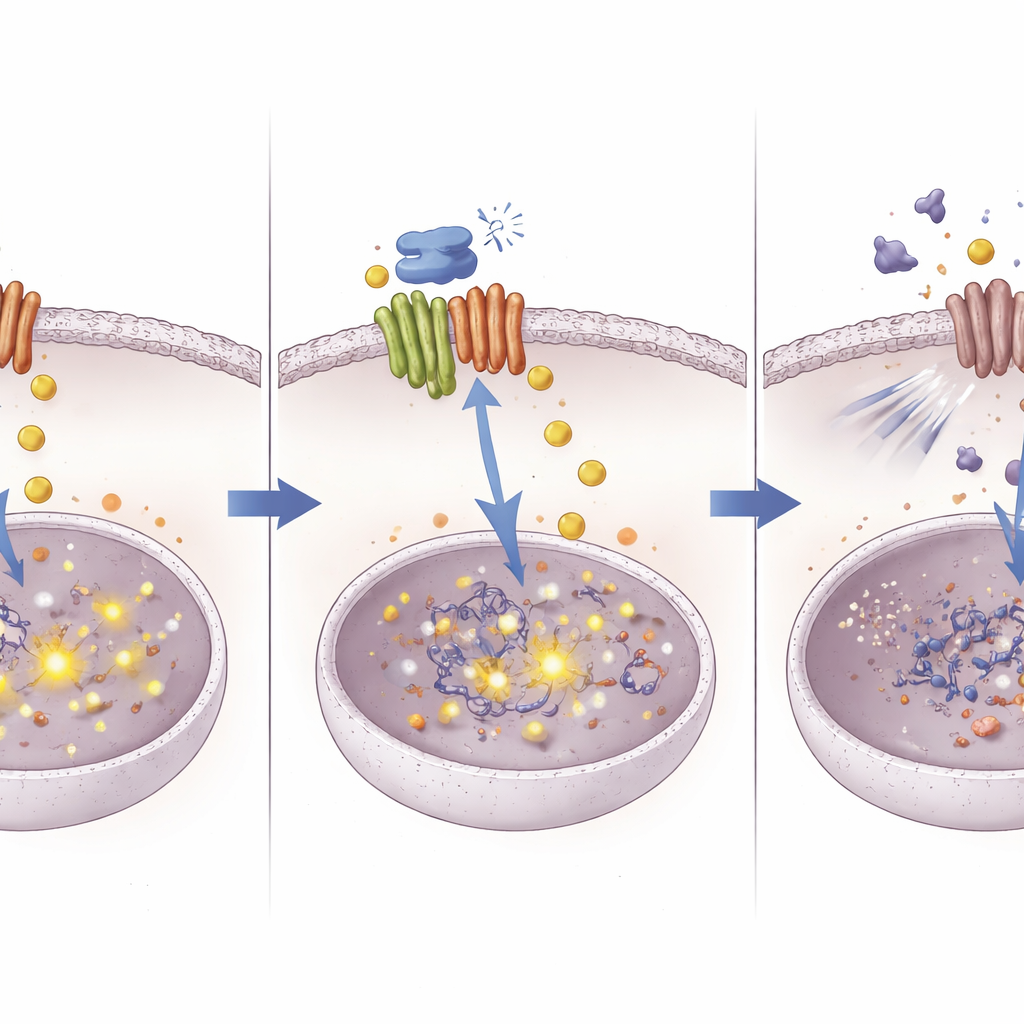
Eski ilaçları daha iyi çalıştırmanın yeni bir yolu
Bir bakır kuryesi proteinden bir hayatta kalma yolundaki DNA düzeyindeki değişikliklere uzanan yolu izleyerek bu çalışma, karaciğer kanserinde kemoterapi direncine karşı taze bir yaklaşım özetliyor. Çalışma, ATOX1’in tümörlerin bakırı ve sinyalleşmeyi yönetmesine izin vererek sisplatinin etkisini zayıflattığını öne sürüyor. ATOX1’i bileşik 8 ile engellemek bakırın birikmesine neden oluyor; bu da NOTCH1’i DNA metilasyonu yoluyla susturarak sisplatine karşı önemli bir kalkanı ortadan kaldırıyor. Bileşik 8 hâlen deneysel bir molekül olsa da, temsil ettiği konsept—metal işleyen proteinleri hassas biçimde hedefleyerek kanser hücresi davranışını yeniden kablolamak—var olan kemoterapilerin etkinliğini canlandırmaya ve yeni kombinasyon tedavilerini teşvik etmeye yardımcı olabilir.
Atıf: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Anahtar kelimeler: karaciğer kanseri, sisplatin direnci, bakır metabolizması, ATOX1 inhibitörü, Notch sinyalleşmesi