Clear Sky Science · he
סקרינינג CRISPR‑Cas9 מזהה מנגנוני עמידות לציספלטין המונעים על‑ידי ATOX1 בסרטן הכבד ומעריך את יעילות מעכבי מטרה
מדוע מחקר זה חשוב
סרטן הכבד הוא אחד מסוגי הסרטן הקטלניים ביותר בעולם, ורבים מהחולים מקבלים טיפול כימותרפי נפוץ בשם ציספלטין. עם הזמן, לעיתים קרובות הגידולים מפתחים עמידות לתרופה, מה שמאפשר לחלה להתחדש ולהתפשט. המחקר הזה חושף אשם מולקולרי מפתיע שמעורב בעמידות ומציג תרכובת מתוכננת שעשויה לעזור להפוך את הציספלטין ליעיל ובטוח יותר. לקוראים, הוא מספק הצצה לאופן שבו גנטיקה מודרנית, דוגמנות ממוחשבת וכימיה יכולים להשתלב כדי להתעלות על מנגנוני ההגנה של הסרטן.
איך גידולי כבד מתחמקים מכימותרפיה
ציספלטין הורג תאים ממאירים על‑ידי פגיעה ב‑DNA שלהם, אך גידולים יכולים לפתח עמידות באמצעות טריקים רבים: הוצאת התרופה החוצה, תיקון DNA מהיר יותר או הטיית אותות הישרדות. החוקרים השתמשו בכלי חיתוך־גנים עוצמתי — סקרינינג גנומי CRISPR‑Cas9 — כדי לנטרל באופן שיטתי כמעט כל גן בשתי שורות תאי סרטן כבד ואז לחשוף אותן לציספלטין. הם שאלו שאלה פשוטה: כאשר גורעים גן מסוים, האם התאים נעשים רגישים יותר או פחות לתרופה? בין עשרות הגנים המקושרים לעמידות, אחד בלט — ATOX1, חלבון קטן שבאופן רגיל מסייע לתאים להתמודד עם המתכת החיונית נחושת. בתאי סרטן כבד נמצא ריכוז גבוה יותר של ATOX1 מאשר בתאים כבדיים בריאים, ובחולים שבהם הגידולים הראו רמות גבוהות של ATOX1 נצפתה הישרדות גרועה יותר ועמידות מוגברת לציספלטין.
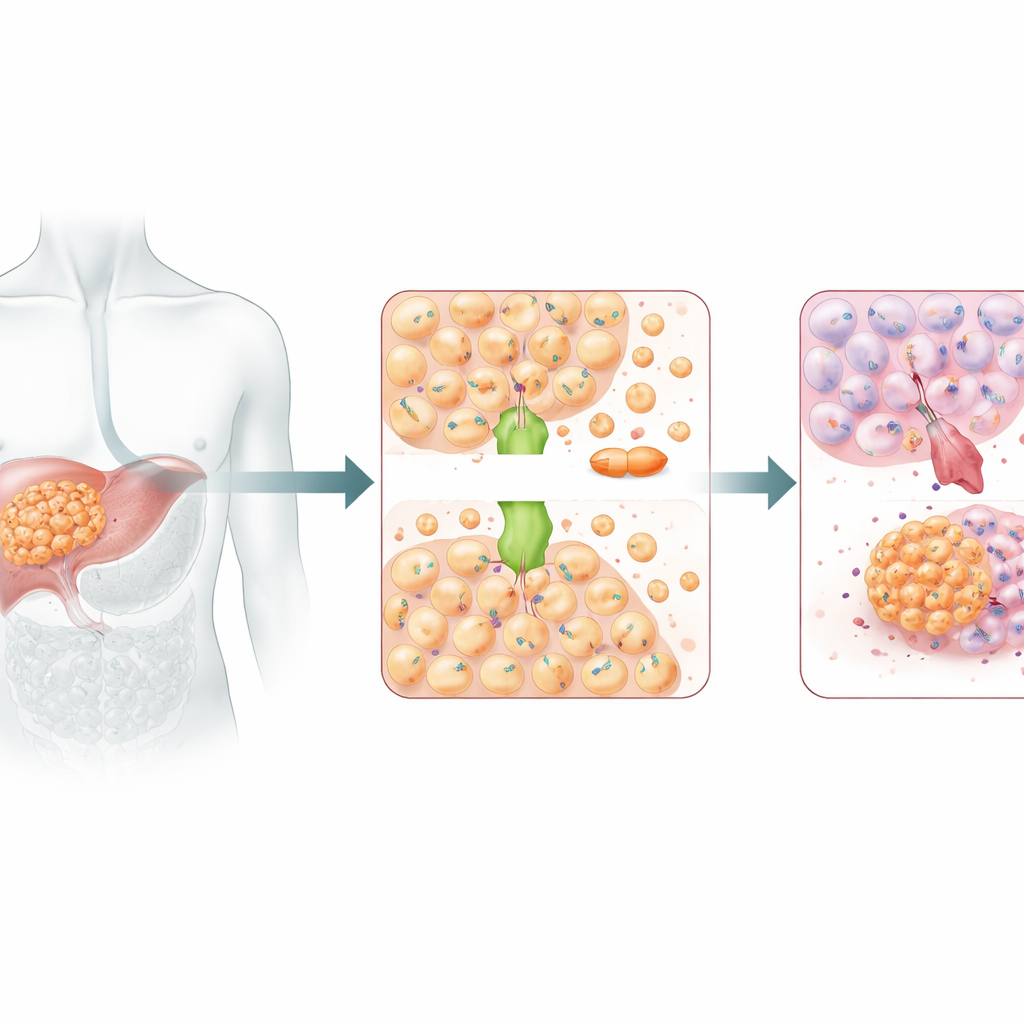
שליח נחושת עם צד אפל
ATOX1 בדרך כלל משמש כשליח נחושת, מועבר יוני נחושת בתוך התאים כדי לשמור על איזון של מתכת חיונית זו. אך נחושת וציספלטין דומים מספיק כך שהם עשויים להשתמש במסלולי הובלה חלקיים זהים. עבודות מבנה קודמות רמזו ש‑ATOX1 יכול לקשור ציספלטין ישירות. במחקר זה, השתקה של ATOX1 בתאי סרטן כבד הפכה אותם לפגיעים יותר לציספלטין: קצב גדילתם האט, הם יצרו פחות מושבות והלאה חלו שיעורי מוות תאי מתוכנן גבוהים יותר. בעכברים נשאי גידולים אנושיים בכבד, הדיכוי של ATOX1 גם גרם לציספלטין לכווץ את הגידולים באופן יעיל יותר. יחד, התוצאות הללו מצביעות על ATOX1 כעל מסייע מפתח שמאפשר לתאי סרטן כבד לעמוד בפני כימותרפיה על בסיס פלאטינה.
עיצוב חסם ממוקד
במקום לגעת בנחושת באופן כללי, מה שעשוי להיות רעיל, הצוות שאף לחסום את ATOX1 עצמו. הם סימלו את תנועת חלבון ATOX1 במחשב כדי למצוא כיסים יציבים שבהם תרופה עשויה להיקשר, ואז בחרו באופן וירטואלי 1.5 מיליון מולקולות קטנות לפי התאמתן. לאחר מספר סבבי סינון ואימות במעבדה, עלה מועמד אחד — שכונה תרכובת 8 — כקושר חזק וספציפי. ניסויים ביופיזיקליים הראו שתרכובת 8 נקשרת בחוזקה ל‑ATOX1 ומייצבת את מבנהו, בעוד שאין לה השפעה משמעותית על חלבון נחושת קשור אחר שאליו פוגעות גם מעכבים ישנים. בבדיקות תאים, תרכובת 8 הייתה פחות מזיקה לתאי כבד רגילים מאשר תרופה קודמת ל‑ATOX1, מה שמרמז על מרווח בטיחות משופר אף על פי שפעילותה כנגד סרטן כתרופה יחידה היתה צנועה.
לכופף את הנחושת נגד הגידול
ההשפעות הבולטות ביותר נראו כאשר תרכובת 8 שולבה עם ציספלטין. בתאי סרטן כבד שגדלו במעבדה, השילוב קיצץ את הגדילה יותר מכל אחת מהתרופות בנפרד, הקטין היווצרות מושבות וגרם לשיעורי מוות תאי גבוהים יותר. בעכברים, השילוב הניב את הגידולים הקטנים ביותר ואת הרמות הנמוכות ביותר של סמנים לחלוקת תאים, ללא נזק ברור לאיברים מרכזיים. כדי להבין מדוע, החוקרים ניתחו פעילות גנים ומצאו שהחסימה של ATOX1 גרמה להצטברות נחושת בתוך תאי הגידול. הצטברות הנחושת הזו נקשרה לתוספת תגיות כימיות — מתילציה של DNA — באזור הבקרה של גן בשם NOTCH1, חלק מנתיב שעוזר לתאי גידול לשרוד מתח ולתקן DNA. מתילציה כבדה יותר פירושה שהמפתח של NOTCH1 הושתק, וגֵן השותף שלו HES1 גם שקט. חשוב: שימוש במחמצי נחושת (קושר נחושת) הפך את השינויים האלה, מה שמראה שנחושת עצמה היא מרכזית להשפעה.
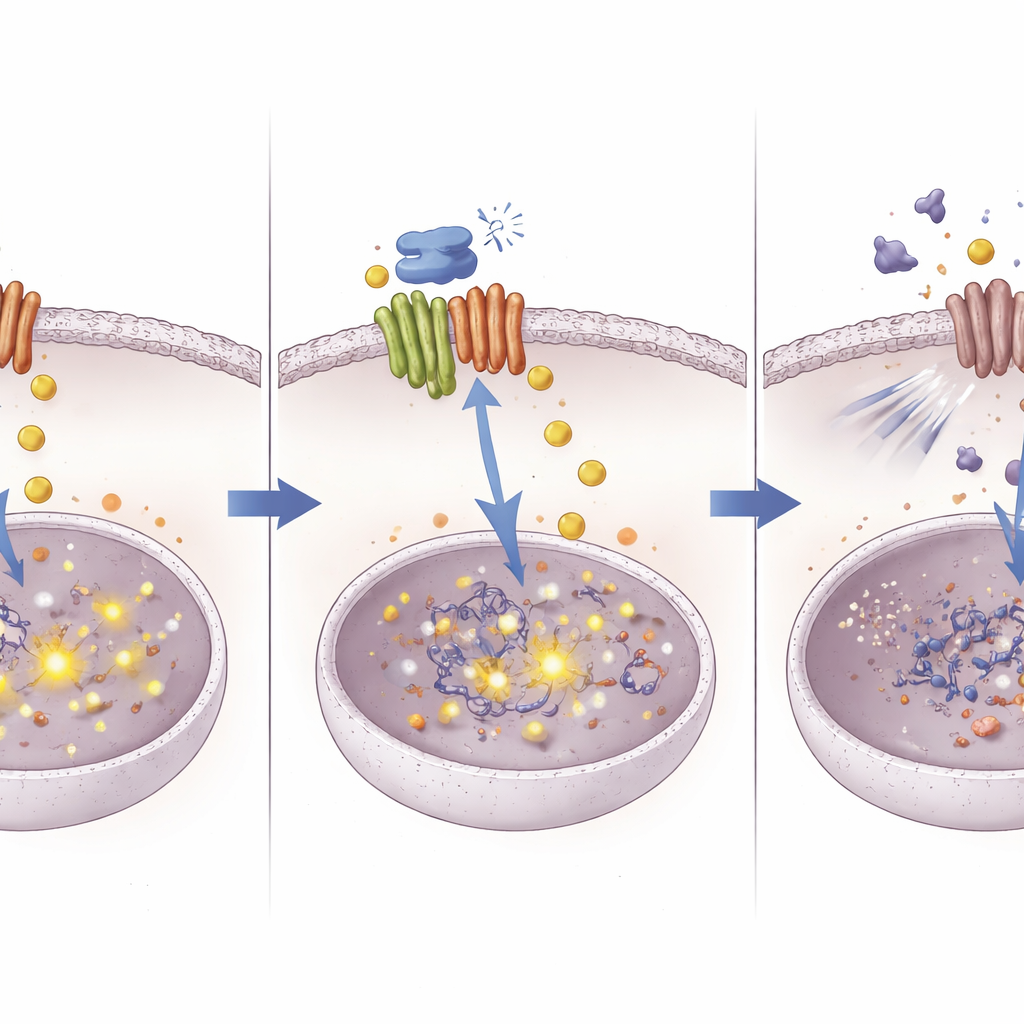
נתיב חדש לשפר תרופות ישנות
באמצעות מיפוי המסלול מחלבון שליח נחושת לשינויים ברמת ה‑DNA בנבי הישרדות, המחקר מציג דרך חדשה להתמודד עם עמידות לכימותרפיה בסרטן הכבד. העבודה מציעה ש‑ATOX1 מאפשר לגידולים לנהל נחושת וסיגנלים כך שלא ייפגעו חזק על‑ידי ציספלטין. חסימת ATOX1 בעזרת תרכובת 8 גורמת להצטברות נחושת, שמצידה משתקת את NOTCH1 באמצעות מתילציית DNA ומסירה מגננה חשובה נגד ציספלטין. אף שתרכובת 8 עדיין מולקולה ניסיונית, הקונספט שהיא מגלמת — פגיעה מדויקת בחלבונים המטפלים במתכות כדי לשנות את התנהגות תאי הסרטן — יכול לסייע להחיות את היעילות של כימותרפיות קיימות ולהוות השראה לשילובי טיפולים חדשים.
ציטוט: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
מילות מפתח: סרטן הכבד, עמידות לציספלטין, מטבוליזם הנחושת, מעכב ATOX1, סיגנלינג Notch