Clear Sky Science · es
Detección CRISPR-Cas9 identifica mecanismos de resistencia al cisplatino impulsados por ATOX1 en cáncer de hígado y evalúa la eficacia de un inhibidor dirigido
Por qué importa esta investigación
El cáncer de hígado es uno de los más letales a nivel mundial, y muchos pacientes reciben un fármaco quimioterápico habitual llamado cisplatino. Con el tiempo, sin embargo, los tumores a menudo aprenden a ignorar el medicamento, lo que permite que la enfermedad reaparezca y se disemine. Este estudio revela un culpable molecular inesperado detrás de esa resistencia e introduce un compuesto diseñado que podría ayudar a que el cisplatino funcione mejor y con mayor seguridad. Para el lector, ofrece una visión de cómo la genética moderna, la modelización por ordenador y la química pueden combinarse para burlar las defensas del cáncer.
Cómo los tumores hepáticos eluden la quimioterapia
El cisplatino mata a las células cancerosas dañando su ADN, pero los tumores pueden volverse resistentes mediante múltiples trucos: expulsando el fármaco, reparando el ADN más rápido o reconfigurando señales de supervivencia. Los autores emplearon una potente herramienta de edición génica, una pantalla genómica CRISPR-Cas9, para desactivar sistemáticamente casi todos los genes en dos líneas celulares de cáncer de hígado y luego exponerlas al cisplatino. Plantearon una pregunta simple: cuando se elimina un gen, ¿las células se vuelven más o menos sensibles al medicamento? Entre docenas de genes vinculados a la resistencia destacó uno: ATOX1, una pequeña proteína que normalmente ayuda a las células a manejar el metal esencial cobre. Las células de cáncer hepático presentaban más ATOX1 que las células hepáticas sanas, y los pacientes cuyos tumores mostraban niveles altos de ATOX1 tendían a tener peor supervivencia y más resistencia al cisplatino.
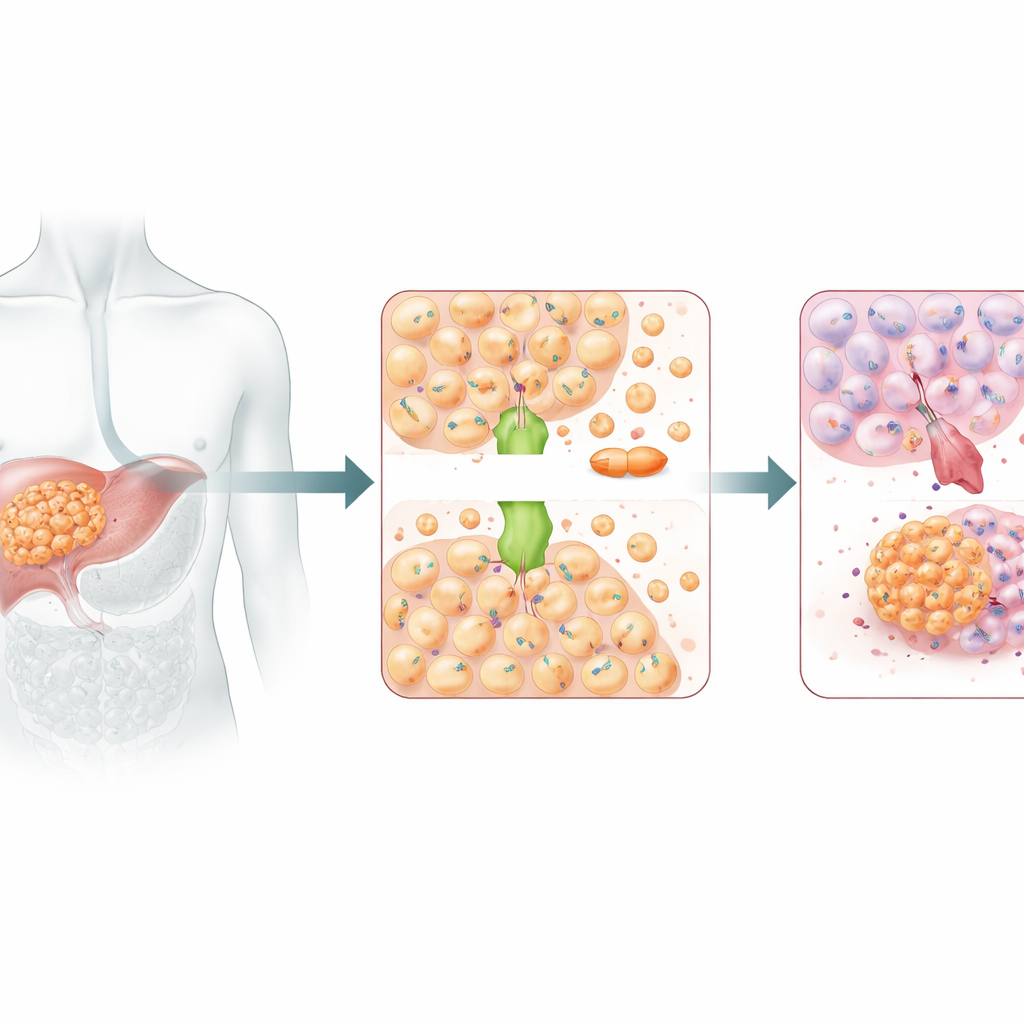
Un mensajero del cobre con un lado oscuro
ATOX1 suele actuar como un mensajero del cobre, transportando iones de cobre dentro de las células para mantener este metal vital en equilibrio. Pero el cobre y el cisplatino son lo suficientemente parecidos como para poder usar algunas de las mismas rutas de transporte. Trabajos estructurales previos habían insinuado que ATOX1 puede unirse directamente al cisplatino. En este estudio, silenciar ATOX1 en células de cáncer hepático las hizo mucho más vulnerables al cisplatino: su crecimiento se ralentizó, formaron menos colonias y experimentaron más muerte celular programada. En ratones con tumores hepáticos humanos, reducir la expresión de ATOX1 también permitió que el cisplatino redujera los tumores con mayor eficacia. En conjunto, estos resultados señalaron a ATOX1 como un colaborador clave que permite a las células de cáncer hepático resistir la quimioterapia basada en platino.
Diseñando un bloqueador de precisión
En lugar de atacar el cobre de forma general, lo que puede ser tóxico, el equipo se propuso bloquear el propio ATOX1. Simularon el movimiento de la proteína ATOX1 en ordenador para encontrar bolsillos estables donde un fármaco pudiera unirse, y luego evaluaron virtualmente 1,5 millones de pequeñas moléculas por su capacidad de encajar. Tras varias rondas de filtrado y validación en laboratorio, surgió un candidato—denominado compuesto 8—como un ligando fuerte y específico. Ensayos biofísicos mostraron que el compuesto 8 se unía firmemente a ATOX1 y estabilizaba su estructura, mientras que tenía poco efecto sobre una proteína de cobre relacionada que los inhibidores anteriores también atacaban. En pruebas celulares, el compuesto 8 resultó menos dañino para las células hepáticas normales que un fármaco previo contra ATOX1, lo que sugiere un mejor margen de seguridad aunque su actividad anticancerígena como agente único fuera modesta.
Volviendo el cobre contra el tumor
Los efectos más llamativos aparecieron cuando el compuesto 8 se combinó con cisplatino. En células de cáncer hepático cultivadas en placas, la combinación de ambos fármacos redujo el crecimiento más que cualquiera de los dos por separado, disminuyó la formación de colonias y provocó tasas más altas de muerte celular. En ratones, la combinación produjo los tumores más pequeños y los niveles más bajos de marcadores de división celular, sin daños evidentes en órganos principales. Para entender por qué, los investigadores analizaron la actividad génica y hallaron que bloquear ATOX1 provocó acumulación de cobre dentro de las células cancerosas. Esa acumulación de cobre se asoció con un aumento de marcas químicas—metilación del ADN—en la región de control de un gen llamado NOTCH1, parte de una vía que ayuda a las células tumorales a sobrevivir al estrés y reparar el ADN. Una mayor metilación implicó que el interruptor de NOTCH1 se apagaba, y su gen asociado HES1 también se silenció. De forma importante, el uso de un compuesto quelante de cobre revirtió estos cambios, demostrando que el cobre en sí era central para el efecto.
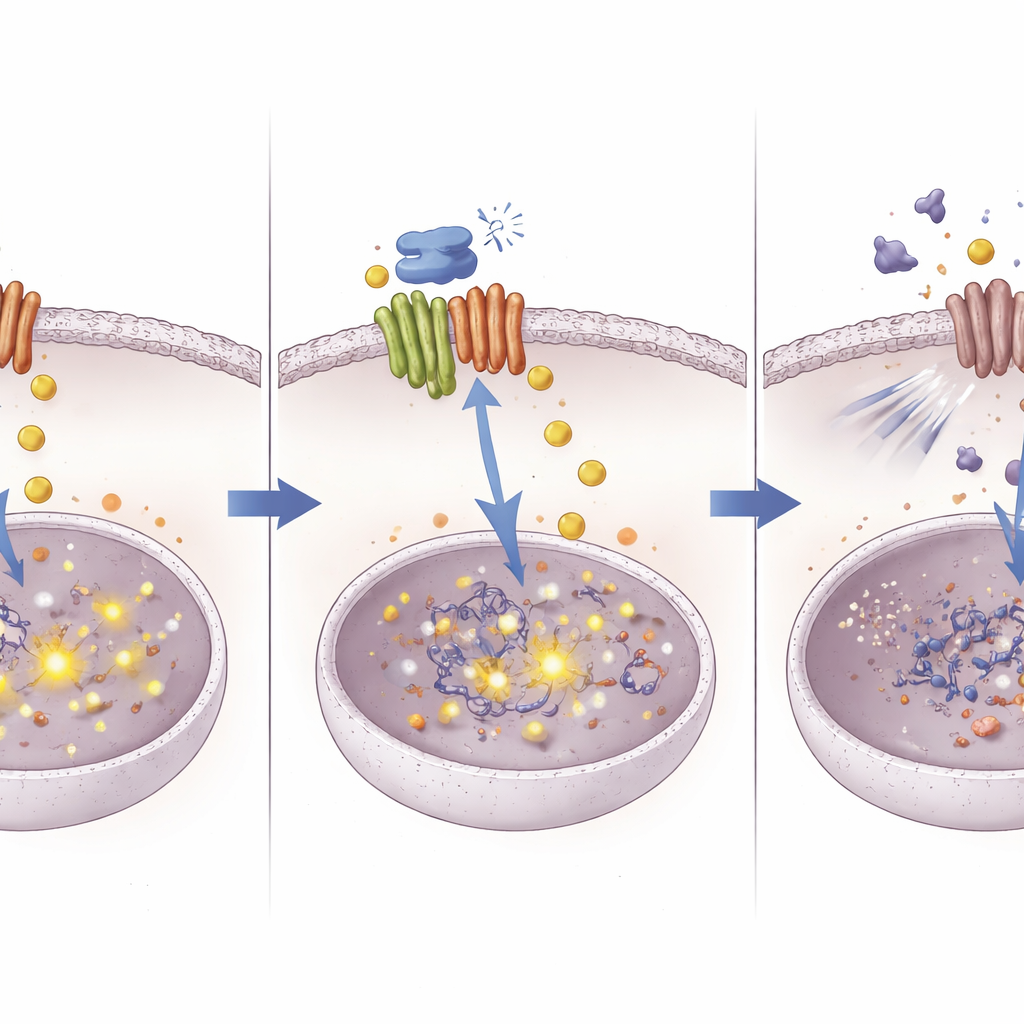
Una nueva vía para hacer que fármacos antiguos funcionen mejor
Al trazar la ruta desde una proteína mensajera de cobre hasta cambios a nivel del ADN en una vía de supervivencia, este estudio describe una forma novedosa de abordar la resistencia a la quimioterapia en el cáncer de hígado. El trabajo sugiere que ATOX1 permite a los tumores manejar el cobre y la señalización de un modo que amortigua el efecto del cisplatino. Bloquear ATOX1 con el compuesto 8 provoca la acumulación de cobre, que a su vez silencia NOTCH1 mediante metilación del ADN y elimina un escudo clave frente al cisplatino. Aunque el compuesto 8 sigue siendo una molécula experimental, el concepto que encarna—apuntar de forma precisa a proteínas manejadoras de metales para reconfigurar el comportamiento de las células cancerosas—podría ayudar a resucitar la eficacia de quimioterapias existentes e inspirar nuevos tratamientos combinados.
Cita: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Palabras clave: cáncer de hígado, resistencia al cisplatino, metabolismo del cobre, inhibidor de ATOX1, señalización Notch