Clear Sky Science · ar
مسح CRISPR-Cas9 يحدد آليات مقاومة السيسبلاتين المدفوعة بـ ATOX1 في سرطان الكبد ويقيّم فعالية مثبط مستهدف
لماذا يهم هذا البحث
يُعد سرطان الكبد من أكثر أنواع السرطان فتكا في العالم، ويتلقى العديد من المرضى دواءً كيميائياً شائعاً يُدعى السيسبلاتين. مع مرور الوقت، تتعلم الأورام في كثير من الأحيان تفادي تأثير الدواء، مما يسمح للمرض بالعودة والانتشار. يكشف هذا البحث عن سبب جزيئي مفاجئ لتلك المقاومة ويعرض مركباً مصمماً قد يساعد على جعل السيسبلاتين أكثر فعالية وأماناً. للقارئ، يقدم لمحة عن كيفية دمج علم الوراثة الحديث والمحاكاة الحاسوبية والكيمياء للتغلب على دفاعات السرطان.
كيف تهرب أورام الكبد من العلاج الكيميائي
يقتل السيسبلاتين الخلايا السرطانية عن طريق إلحاق ضرر بالحمض النووي، لكن الأورام يمكن أن تصبح مقاومة عبر حيل متعددة: ضخ الدواء خارج الخلية، إصلاح الحمض النووي بسرعة أكبر، أو إعادة توصيل إشارات البقاء. استخدم المؤلفون أداة قوية لتحرير الجينات، وهي مسح جينومي واسع النطاق باستخدام CRISPR-Cas9، لإطفاء ما يقرب من كل جينين في خطي خلايا سرطان الكبد ثم تعريضها للسيسبلاتين. طرحوا سؤالاً بسيطاً: عند تعطيل جينٍ ما، هل تصبح الخلايا أكثر أو أقل حساسية تجاه الدواء؟ من بين عشرات الجينات المرتبطة بالمقاومة، برز جين واحد—ATOX1، وهو بروتين صغير يساعد الخلايا عادة على التعامل مع المعدن الضروري النحاس. كانت خلايا سرطان الكبد تحتوي على مستويات أعلى من ATOX1 مقارنة بالخلايا الكبدية السليمة، ويميل المرضى الذين تظهر أورامهم مستويات عالية من ATOX1 إلى البقاء لفترات أقصر وإلى مقاومة أكبر للسيسبلاتين.
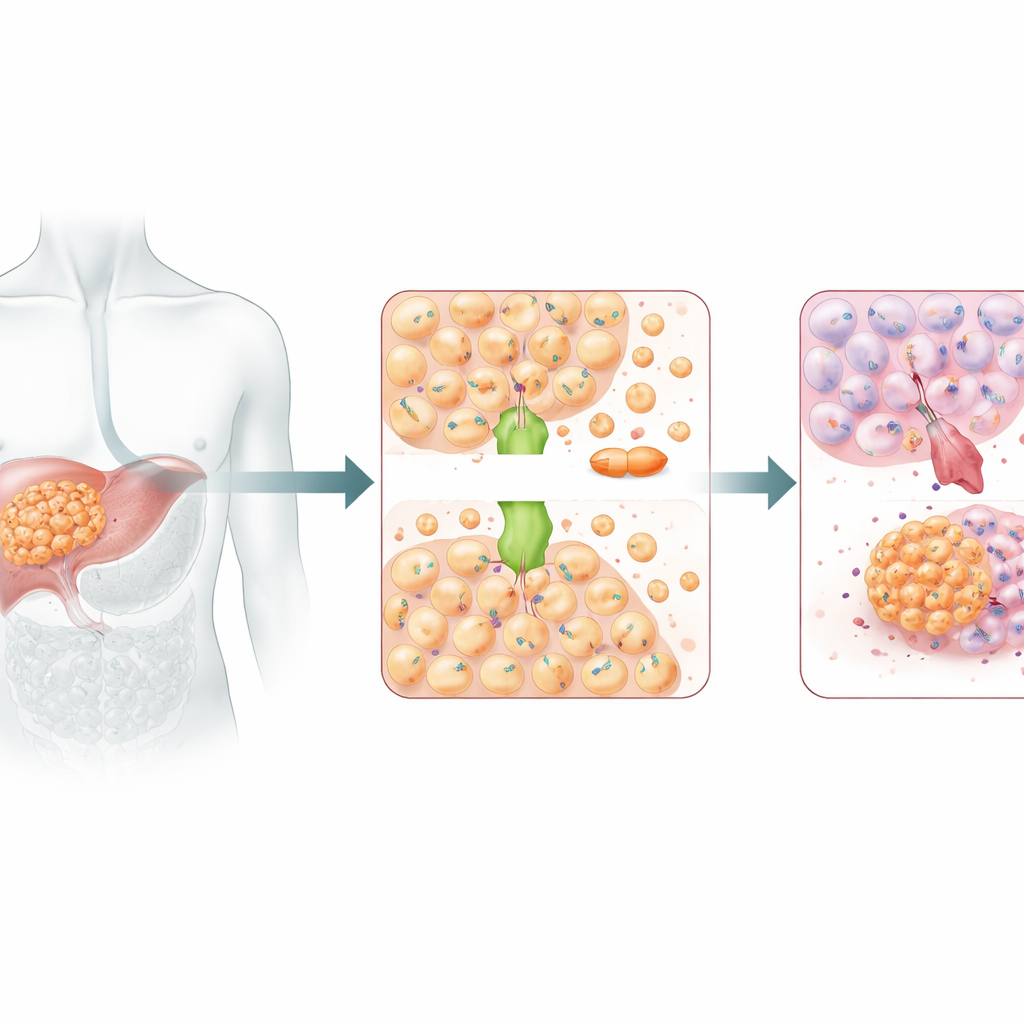
ناقل نحاس ذو جانب مظلم
يعمل ATOX1 عادة كناقل للنحاس، ينقل أيونات النحاس داخل الخلايا للحفاظ على توازن هذا المعدن الحيوي. لكن النحاس والسيسبلاتين متشابهان بما يكفي ليشتركا في بعض مسارات النقل نفسها. أشارت أعمال بنيوية سابقة إلى أن ATOX1 يمكن أن يربط السيسبلاتين مباشرة. في هذه الدراسة، جعل إسكات ATOX1 خلايا سرطان الكبد أكثر عُرضة للسيسبلاتين بشكل كبير: تباطأ نموها، شكلت مستعمرات أقل، وخضعت لمعدلات أعلى من الموت المبرمج. في نماذج فأرية تحمل أورامًا بشرية في الكبد، أدى خفض تعبير ATOX1 أيضاً إلى زيادة فعالية السيسبلاتين في تقليص الأورام. مجتمعة، أشارت هذه النتائج إلى أن ATOX1 يعمل كمساعد أساسي يمكّن خلايا سرطان الكبد من تحمل العلاج الكيميائي القائم على البلاتين.
تصميم حاجز دقيق
بدلاً من استهداف النحاس بصورة عريضة، والتي قد تكون سامة، انطلق الفريق لاستهداف ATOX1 نفسه. قاموا بمحاكاة حركة بروتين ATOX1 على الحاسوب للعثور على جيوب ثابتة قد يربطها دواء، ثم اختبروا افتراضياً 1.5 مليون جزيء صغير لإمكانية التوافق. بعد عدة جولات من التصفية والتحقق المخبري، برز مرشح واحد—أُطلق عليه المركب 8—كدابِّت قوي ومحدد. أظهرت اختبارات حيوية فيزيائية أن المركب 8 يرتبط بقوة بـ ATOX1 ويثبت بنيته، مع تأثير ضئيل على بروتين نحاس ذي صلة تصيبه مثبطات قديمة. في اختبارات الخلايا، كان المركب 8 أقل إيلاماً لخلايا الكبد السليمة من دواء ATOX1 سابق، ما يشير إلى هامش سلامة أفضل رغم أن نشاطه المضاد للسرطان كعاملٍ منفرد كان متواضعاً.
تحويل النحاس ضد الورم
ظهرت التأثيرات الأكثر لفتاً عندما تم إقران المركب 8 مع السيسبلاتين. في خلايا سرطان الكبد المزروعة في أطباق، أدى الجمع بين الدوائين إلى خفض النمو أكثر من أيٍ منهما بمفرده، وتقليل تكوين المستعمرات، وتحفيز معدلات أعلى من موت الخلايا. في الفئران، أنتج الجمع أصغر الأورام وأدنى مستويات علامات انقسام الخلايا، من دون أضرار واضحة للأعضاء الرئيسية. لفهم السبب، حلل الباحثون نشاط الجينات ووجدوا أن حجب ATOX1 تسبب في تراكم النحاس داخل خلايا السرطان. ارتبط هذا التجمع بزيادة الوسوم الكيميائية—مثيلة الحمض النووي—في منطقة التحكم لجين يُدعى NOTCH1، وهو جزء من مسار يساعد خلايا الورم على الصمود تحت الضغوط وإصلاح الحمض النووي. أدت المثيلة الأثقل إلى خفض نشاط مفاتيح تشغيل NOTCH1، وهدأت أيضاً جين الشريك HES1. والأهم أن استخدام مركب مخلّب للنحاس عكس هذه التغيرات، مما أظهر أن النحاس نفسه كان المحور المركزي للتأثير.
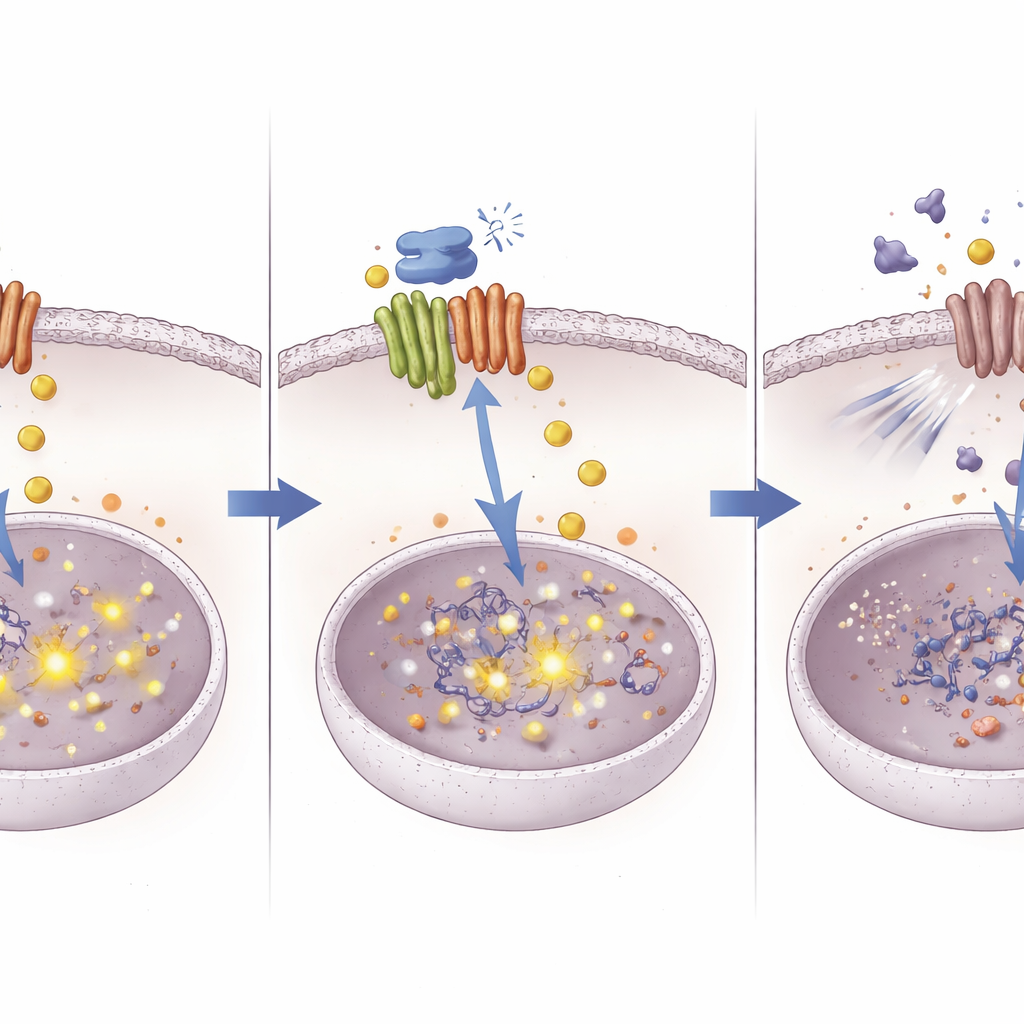
مسار جديد لجعل الأدوية القديمة تعمل بشكل أفضل
من خلال تتبع المسار من بروتين ناقل للنحاس إلى تغيرات على مستوى الحمض النووي في مسار البقاء، تعرض هذه الدراسة نهجاً جديداً للتصدي لمقاومة العلاج الكيميائي في سرطان الكبد. تشير النتائج إلى أن ATOX1 يمكّن الأورام من إدارة النحاس والإشارات بطريقة تقلل من تأثير السيسبلاتين. يؤدي حجب ATOX1 بالمركب 8 إلى تراكم النحاس، الذي يؤدي بدوره إلى إسكات NOTCH1 عبر مثيلة الحمض النووي وإزالة درعٍ رئيسي ضد السيسبلاتين. وعلى الرغم من أن المركب 8 لا يزال جزيئاً تجريبياً، فإن الفكرة التي يجسدها—استهداف بروتينات التعامل مع المعادن بدقة لإعادة برمجة سلوك الخلايا السرطانية—قد تساعد في إحياء فعالية المعالجات الكيميائية الحالية وتلهم تركيبات علاجية جديدة.
الاستشهاد: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
الكلمات المفتاحية: سرطان الكبد, مقاومة السيسبلاتين, تمثّل النحاس, مثبط ATOX1, إشارة نوتش