Clear Sky Science · nl
CRISPR-Cas9-screening identificeert ATOX1-gedreven cisplatine-resistentiemechanismen bij leverkanker en evalueert de doeltreffendheid van gerichte remmers
Waarom dit onderzoek ertoe doet
Leverkanker behoort tot de dodelijkste vormen van kanker wereldwijd, en veel patiënten krijgen de veelgebruikte chemotherapie cisplatine. Na verloop van tijd leren tumoren echter vaak zich te onttrekken aan het middel, waardoor de ziekte kan terugkeren en uitzaaien. Deze studie onthult een verrassende moleculaire oorzaak van die resistentie en introduceert een ontworpen verbinding die cisplatine mogelijk effectiever en veiliger kan maken. Voor lezers biedt het een inkijkje in hoe moderne genetica, computermodellering en chemie gecombineerd kunnen worden om de verdedigingsmechanismen van kanker te slim af te zijn.
Hoe levertumoren chemotherapie ontwijken
Cisplatine doodt kankercellen door hun DNA te beschadigen, maar tumoren kunnen resistent worden via uiteenlopende trucs: het uitpompen van het middel, snellere DNA-reparatie of het herschakelen van overlevingssignalen. De auteurs gebruikten een krachtig genbewerkingstool, een genoombrede CRISPR-Cas9-screen, om vrijwel elk gen uit te schakelen in twee leverkankercellijnen en deze vervolgens aan cisplatine bloot te stellen. Ze stelden een eenvoudige vraag: wanneer een gen wordt uitgeschakeld, worden cellen dan gevoeliger of juist ongevoeliger voor het middel? Onder tientallen genen die met resistentie samenhingen, stak er één bovenuit — ATOX1, een klein eiwit dat normaal helpt bij het omgaan met het essentiële metaal koper. Leverkankercellen bevatten meer ATOX1 dan gezonde levercellen, en patiënten van wie de tumoren hoge ATOX1-niveaus toonden, hadden doorgaans een slechtere overleving en meer cisplatine-resistentie.
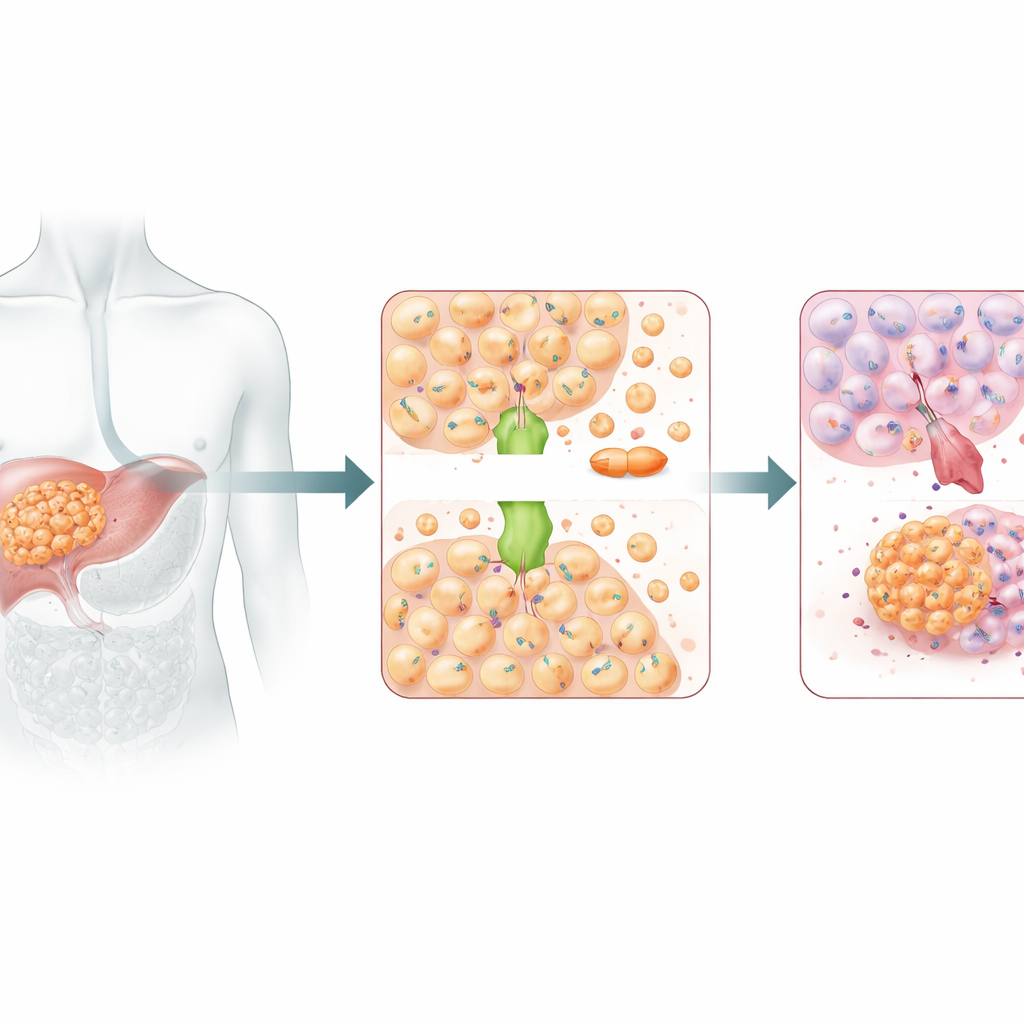
Een koperkoerier met een donkere kant
ATOX1 fungeert doorgaans als een koperkoerier, die koperionen binnen cellen transporteert om dit vitale metaal in balans te houden. Maar koper en cisplatine lijken voldoende op elkaar om sommige transportroutes te delen. Eerder structureel werk had al gesuggereerd dat ATOX1 direct aan cisplatine kan binden. In deze studie maakte het uitschakelen van ATOX1 in leverkankercellen hen veel gevoeliger voor cisplatine: hun groei nam af, ze vormden minder kolonies en ze ondergingen meer geprogrammeerde celdood. In muismodellen met menselijke levertumoren zorgde ATOX1-downregulatie er ook voor dat cisplatine tumoren effectiever deed krimpen. Samen wezen deze resultaten op ATOX1 als een belangrijke helper die leverkankercellen in staat stelt platinumgebaseerde chemotherapie te weerstaan.
Ontwerpen van een precisieblokker
In plaats van koper op een brede manier te targeten, wat toxisch kan zijn, richtte het team zich op het blokkeren van ATOX1 zelf. Ze simuleerden de beweging van het ATOX1-eiwit in een computer om stabiele pockets te vinden waar een geneesmiddel zou kunnen binden, en testten vervolgens virtueel 1,5 miljoen kleine moleculen op hun vermogen om te passen. Na meerdere selectierondes en laboratoriumvalidatie kwam één kandidaat naar voren — gedoopt tot verbinding 8 — als een sterke en specifieke binder. Biofysische assays toonden aan dat verbinding 8 stevig aan ATOX1 bond en diens structuur stabiliseerde, terwijl het weinig effect had op een verwant kopereiwit dat oudere remmers ook aantasten. In cellulaire tests was verbinding 8 minder schadelijk voor normale levercellen dan een eerdere ATOX1-drug, wat wijst op een beter veiligheidsprofiel, ook al was de enkelvoudige antikankeractiviteit bescheiden.
Koper tegen de tumor keren
De meest opvallende effecten traden op wanneer verbinding 8 werd gecombineerd met cisplatine. In in-vitro gekweekte leverkankercellen verminderde de combinatie de groei meer dan elk middel afzonderlijk, verminderde kolonievorming en activeerde hogere percentages celdood. In muizen resulteerde de combinatietherapie in de kleinste tumoren en de laagste niveaus van markers voor celdeling, zonder duidelijke schade aan belangrijke organen. Om te begrijpen waarom analyseerden de onderzoekers genactiviteit en vonden dat het blokkeren van ATOX1 leidde tot koperophoping binnen kankercellen. Die koperophoping hing samen met toegenomen chemische tags — DNA-methylatie — op het regelgebied van een gen genaamd NOTCH1, onderdeel van een pathway die tumorcellen helpt om stress te overleven en DNA te repareren. Zwaardere methylatie betekende dat de NOTCH1-schakelaar werd gedimd, en het partnergen HES1 werd eveneens stilgelegd. Belangrijk was dat het gebruik van een koperchelator deze veranderingen ongedaan maakte, wat aantoonde dat koper zelf centraal stond in het effect.
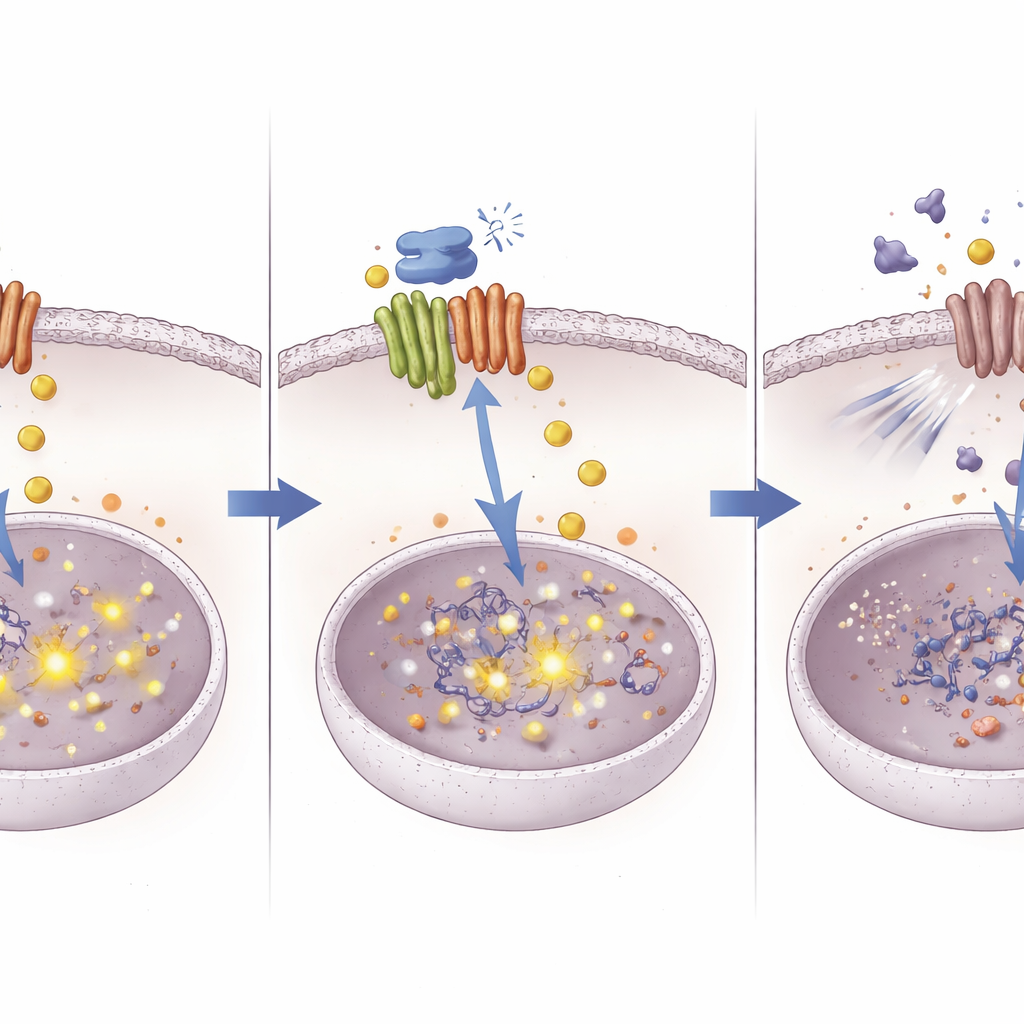
Een nieuwe route om oude middelen effectiever te maken
Door het pad te volgen van een koperkoerier-eiwit naar DNA-niveauveranderingen in een overlevingspathway, schetst deze studie een nieuwe manier om chemotherapie-resistentie bij leverkanker aan te pakken. Het werk suggereert dat ATOX1 tumoren in staat stelt koper en signaalvoering zo te beheren dat de werking van cisplatine wordt verzwakt. Het blokkeren van ATOX1 met verbinding 8 veroorzaakt koperophoping, wat op zijn beurt NOTCH1 via DNA-methylatie stilzet en een belangrijke bescherming tegen cisplatine wegneemt. Hoewel verbinding 8 nog een experimenteel molecuul is, kan het idee dat metalen afhandelende eiwitten nauwkeurig worden getarget om het gedrag van kankercellen te herschakelen, helpen de effectiviteit van bestaande chemotherapieën te herstellen en nieuwe combinatiebehandelingen inspireren.
Bronvermelding: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Trefwoorden: leverkanker, cisplatine-resistentie, koperstofwisseling, ATOX1-remmer, Notch-signaaloverdracht