Clear Sky Science · pl
Badanie CRISPR-Cas9 identyfikuje mechanizmy oporności na cisplatynę napędzane przez ATOX1 w raku wątroby i ocenia skuteczność celowanego inhibitora
Dlaczego to badanie ma znaczenie
Rak wątroby jest jednym z najbardziej śmiertelnych nowotworów na świecie, a wielu pacjentów otrzymuje powszechny chemioterapeutyk, cisplatynę. Z czasem jednak guzy często nabierają odporności na lek, co pozwala chorobie powrócić i się rozprzestrzenić. To badanie odkrywa zaskakujący molekularny sprawca tej oporności i przedstawia zaprojektowany związek, który może pomóc cisplatynie działać lepiej i bezpieczniej. Dla czytelników to wgląd w to, jak nowoczesna genetyka, modelowanie komputerowe i chemia mogą zostać połączone, by przechytrzyć mechanizmy obronne raka.
Jak guzy wątroby unikają chemioterapii
Cisplatyna zabija komórki nowotworowe, uszkadzając ich DNA, ale guzy mogą zdobyć odporność na wiele sposobów: wypompowywać lek, szybciej naprawiać DNA lub przełączać sygnały przetrwania. Autorzy użyli potężnego narzędzia do edycji genów — przesiewu CRISPR-Cas9 obejmującego cały genom — aby systematycznie wyłączać prawie każdy gen w dwóch liniach komórek raka wątroby, a następnie eksponować je na cisplatynę. Zadali proste pytanie: gdy dany gen jest wyłączony, czy komórki stają się bardziej czy mniej wrażliwe na lek? Spośród dziesiątek genów powiązanych z opornością wyróżnił się jeden — ATOX1, mały białkowy nośnik, który normalnie pomaga komórkom gospodarować niezbędnym metalem, miedzią. Komórki raka wątroby wykazywały wyższy poziom ATOX1 niż zdrowe komórki wątroby, a pacjenci z guzami o wysokiej ekspresji ATOX1 mieli skłonność do gorszego przeżycia i większej oporności na cisplatynę.
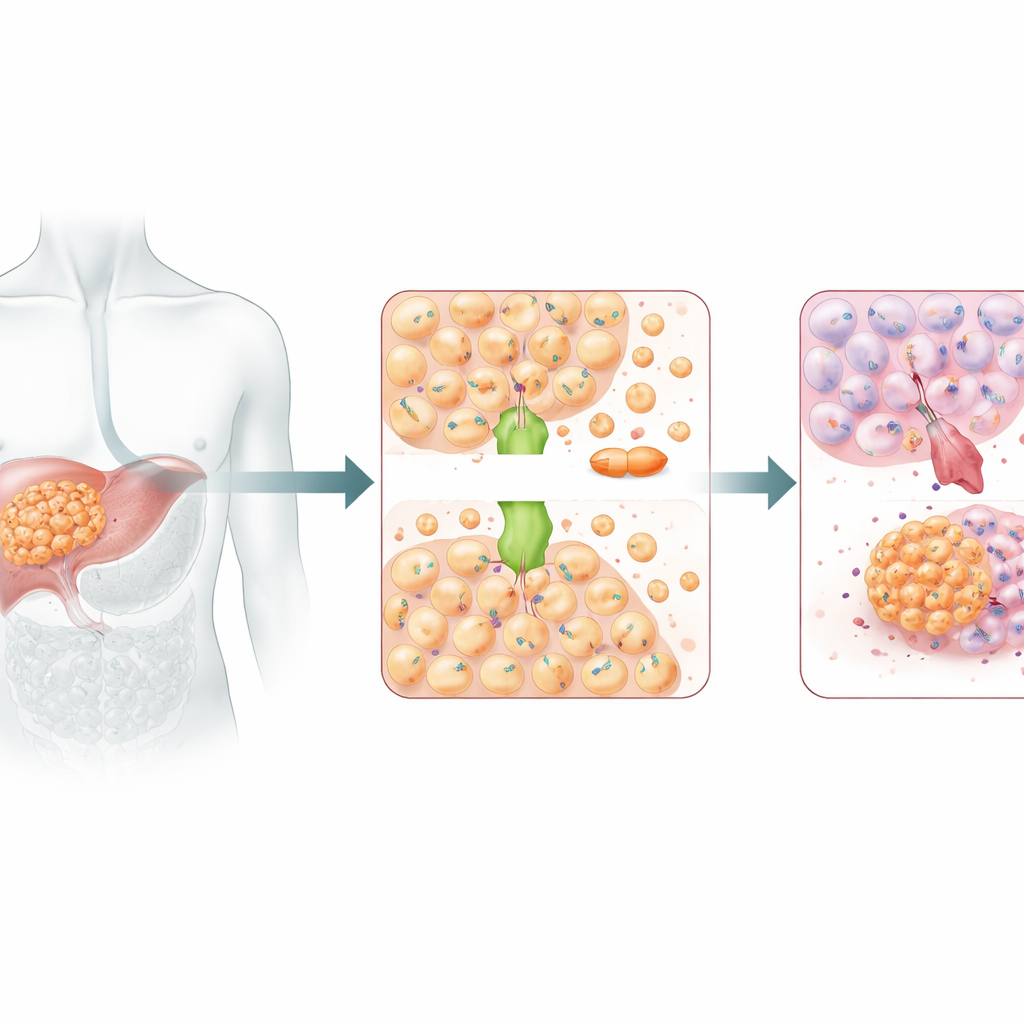
Kurier miedzi z mroczną stroną
ATOX1 zwykle działa jako kurier miedzi, transportując jony miedzi wewnątrz komórek, by utrzymać równowagę tego ważnego metalu. Jednak miedź i cisplatyna są dość podobne, więc mogą korzystać z tych samych szlaków transportowych. Wcześniejsze badania strukturalne sugerowały, że ATOX1 może wiązać cisplatynę bezpośrednio. W tym badaniu wyciszenie ATOX1 w komórkach raka wątroby uczyniło je znacznie bardziej wrażliwymi na cisplatynę: ich wzrost spowolnił, tworzyły mniej kolonii i częściej przechodziły zaprogramowaną śmierć komórkową. U myszy z przeniesionymi ludzkimi guzami wątroby, wyciszenie ATOX1 również sprawiło, że cisplatyna skuteczniej zmniejszała guzy. Razem wyniki te wskazują na ATOX1 jako kluczowego pomocnika, który pozwala komórkom raka wątroby przeciwstawiać się chemioterapii na bazie platyny.
Projektowanie precyzyjnego blokeru
Zamiast szeroko celować w miedź, co może być toksyczne, zespół postanowił zablokować samo ATOX1. Zesymulowali ruch białka ATOX1 na komputerze, aby znaleźć stabilne kieszenie, w które mógłby związać się lek, a następnie wirtualnie przetestowali 1,5 miliona małych cząsteczek pod kątem dopasowania. Po kilku rundach filtracji i walidacji laboratoryjnej wyłonił się kandydat — nazwany związek 8 — jako silny i specyficzny ligand. Badania biofizyczne wykazały, że związek 8 wiązał się silnie z ATOX1 i stabilizował jego strukturę, przy niewielkim wpływie na spokrewnione białko miedziowe, na które oddziaływały starsze inhibitory. W testach komórkowych związek 8 był mniej szkodliwy dla normalnych komórek wątroby niż wcześniejszy lek na ATOX1, sugerując lepszy margines bezpieczeństwa, choć jego aktywność przeciwnowotworowa jako pojedynczego środka była umiarkowana.
Wykorzystanie miedzi przeciwko nowotworowi
Najbardziej uderzające efekty pojawiły się, gdy związek 8 połączono z cisplatyną. W komórkach raka wątroby hodowanych in vitro połączenie obu leków hamowało wzrost bardziej niż którykolwiek z nich osobno, zmniejszało tworzenie kolonii i wywoływało wyższe wskaźniki śmierci komórek. U myszy kombinacja dała najmniejsze guzy i najniższe poziomy markerów podziału komórkowego, bez widocznych uszkodzeń głównych narządów. Aby to wyjaśnić, badacze przeanalizowali aktywność genów i stwierdzili, że blokada ATOX1 powodowała gromadzenie się miedzi w komórkach nowotworowych. To nagromadzenie miedzi wiązało się ze wzrostem chemicznych znaków — metylacji DNA — w regionie regulatorowym genu NOTCH1, należącego do szlaku, który pomaga komórkom nowotworowym przetrwać stres i naprawiać DNA. Silniejsza metylacja oznaczała przyciszenie przełącznika NOTCH1, a jego partner HES1 również się uciszył. Co ważne, zastosowanie związku chelatującego miedź odwracało te zmiany, pokazując, że to właśnie miedź była kluczowa dla efektu.
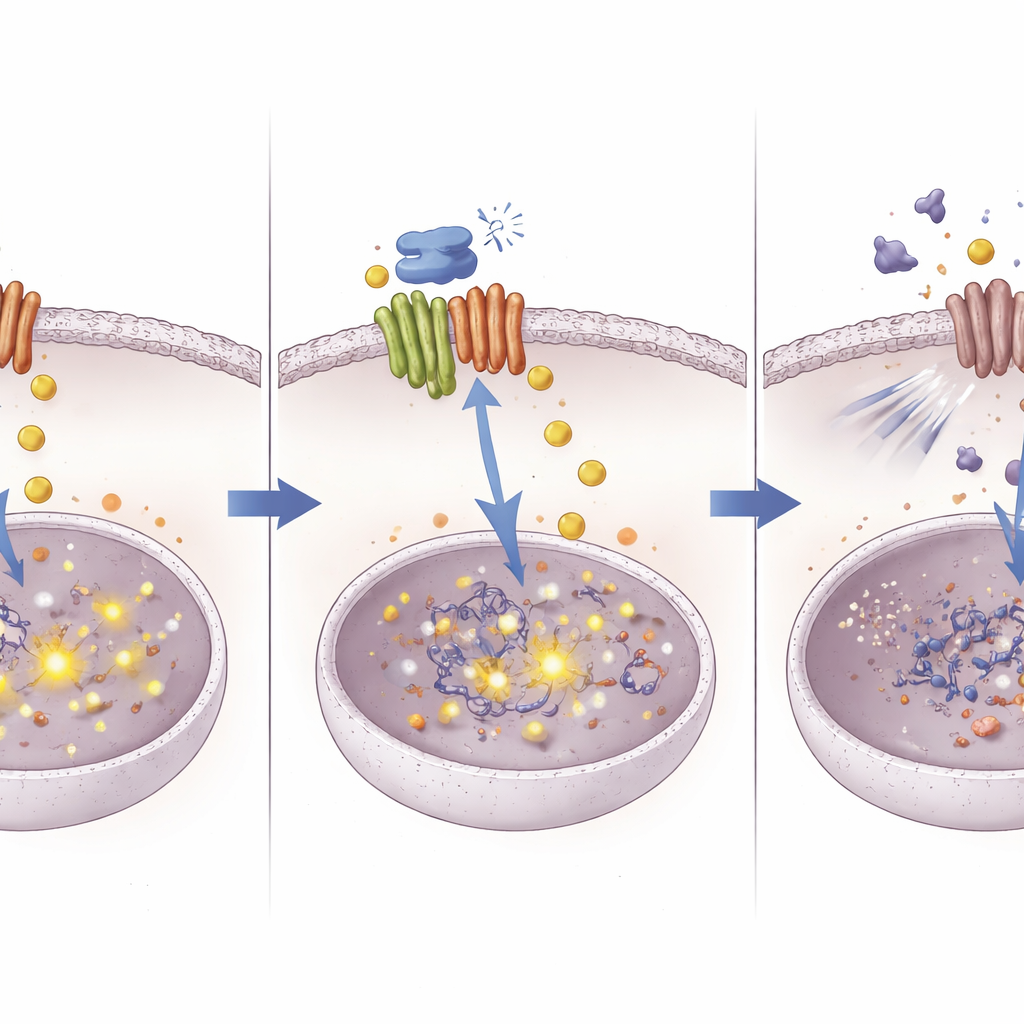
Nowa droga, by stare leki działały lepiej
Śledząc ścieżkę od białka-kuriera miedzi do zmian na poziomie DNA w szlaku przetrwania, to badanie przedstawia świeże podejście do zwalczania oporności na chemioterapię w raku wątroby. Praca sugeruje, że ATOX1 pozwala guzom zarządzać miedzią i sygnalizacją w sposób osłabiający działanie cisplatyny. Zablokowanie ATOX1 związkiem 8 powoduje akumulację miedzi, co z kolei ucisza NOTCH1 przez metylację DNA i usuwa istotną ochronę przed cisplatyną. Chociaż związek 8 jest wciąż molekułą eksperymentalną, koncepcja, którą reprezentuje — precyzyjne celowanie w białka zajmujące się metalami, aby przestawić zachowanie komórek nowotworowych — może pomóc przywrócić skuteczność istniejących chemioterapii i zainspirować nowe terapie skojarzone.
Cytowanie: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Słowa kluczowe: rak wątroby, oporność na cisplatynę, metabolizm miedzi, inhibitor ATOX1, sygnalizacja Notch