Clear Sky Science · sv
CRISPR-Cas9-screening identifierar ATOX1-drivna cisplatinresistensmekanismer i levercancer och utvärderar målinriktad inhibitorseffektivitet
Varför denna forskning är viktig
Levertumörer är en av de dödligaste cancerformerna globalt, och många patienter behandlas med en vanlig cytostatika kallad cisplatin. Med tiden lär sig dock ofta tumörerna att stå emot läkemedlet, vilket gör att sjukdomen kommer tillbaka och sprider sig. Denna studie avslöjar en överraskande molekylär bov bakom den resistensen och presenterar en designad förening som kan få cisplatin att fungera bättre och säkrare. För läsaren ger den en bild av hur modern genetik, datorbaserad modellering och kemi kan kombineras för att överlista cancerförsvar.
Hur levertumörer undviker kemoterapi
Cisplatin dödar cancerceller genom att skada deras DNA, men tumörer kan bli resistenta genom många knep: pumpa ut läkemedlet, reparera DNA snabbare eller omskola överlevnadssignaler. Författarna använde ett kraftfullt genredigeringsverktyg, ett genomsökande CRISPR-Cas9-screen, för systematiskt stänga av nästan varje gen i två levercancercellinjer och därefter utsätta dem för cisplatin. De ställde en enkel fråga: när en gen slås ut, blir cellerna mer eller mindre känsliga för läkemedlet? Bland dussintals gener kopplade till resistens stack en ut—ATOX1, ett litet protein som normalt hjälper celler hantera det essentiella metallen koppar. Levercancerceller hade högre ATOX1-nivåer än friska leverceller, och patienter med tumörer som visade höga ATOX1-nivåer tenderade att ha sämre överlevnad och större cisplatinresistens.
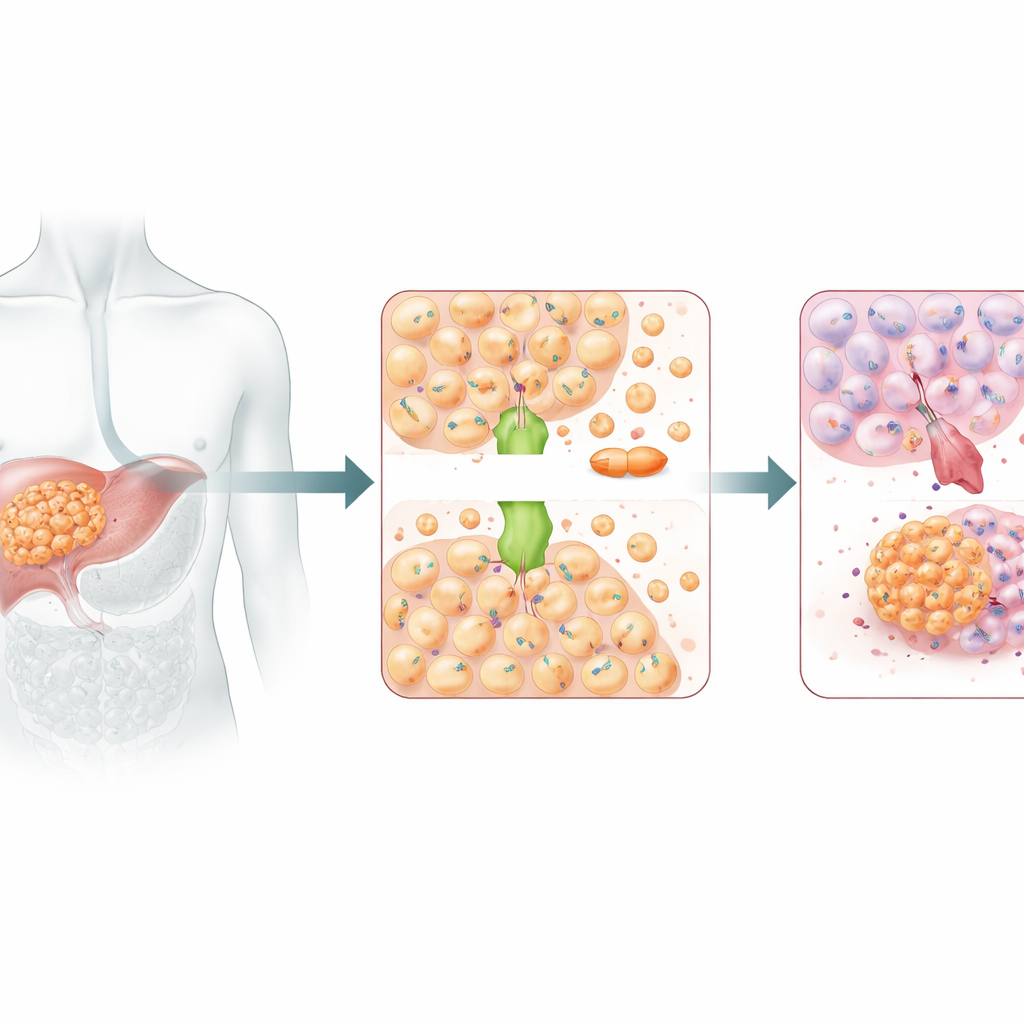
En kopparkurir med en mörk sida
ATOX1 fungerar vanligen som en kopparkurir och för över kopparjoner inuti celler för att hålla detta viktiga metall i balans. Men koppar och cisplatin liknar varandra tillräckligt för att de kan använda vissa av samma transportvägar. Tidigare strukturarbete hade antytt att ATOX1 kan binda cisplatin direkt. I denna studie gjorde tystande av ATOX1 i levercancerceller dem betydligt mer sårbara för cisplatin: deras tillväxt avstannade, de bildade färre kolonier och de genomgick mer programmerad celldöd. I möss med mänskliga levertumörer gjorde nedreglering av ATOX1 också att cisplatin krympte tumörer mer effektivt. Tillsammans pekade dessa resultat på ATOX1 som en nyckelmedhjälpare som tillåter levercancerceller att stå emot platina-baserad kemoterapi.
Design av en precis blockerare
I stället för att rikta in sig på koppar på ett brett sätt, vilket kan vara toxiskt, försökte teamet blockera ATOX1 självt. De simulerade ATOX1-proteinets rörelser i datorn för att hitta stabila fickor där ett läkemedel skulle kunna binda, och testade sedan virtuellt 1,5 miljoner småmolekyler för hur väl de passade. Efter flera filtreringsrundor och laboratorieverifiering framträdde en kandidat—döpt till förening 8—som en stark och specifik bindare. Biofysiska tester visade att förening 8 fäste tätt vid ATOX1 och stabiliserade dess struktur, samtidigt som den hade liten effekt på ett närbesläktat kopparprotein som äldre hämmare också träffade. I celltester var förening 8 mindre skadlig för normala leverceller än ett tidigare ATOX1-läkemedel, vilket tyder på en bättre säkerhetsmarginal även om dess anticanceraktivitet som ensam behandling var måttlig.
Att vända koppar mot tumören
De mest slående effekterna framkom när förening 8 kombinerades med cisplatin. I levercancerceller odlade i petriskålar gav kombinationen större tillväxtsänkning än någon av ämnena ensamt, minskad kolonibildning och högre frekvens av celldöd. I möss gav kombinationen de minsta tumörerna och de lägsta nivåerna av markörer för celldelning, utan uppenbar skada på stora organ. För att förstå varför analyserade forskarna genaktivitet och fann att blockad av ATOX1 orsakade att koppar samlades upp inne i cancercellerna. Denna kopparuppbyggnad kopplades till ökade kemiska markörer—DNA-metylering—på kontrollregionen av en gen kallad NOTCH1, del av en bana som hjälper tumörceller att överleva stress och reparera DNA. Tyngre metylering innebar att NOTCH1-omkopplaren slog ned, och dess parpartnergen HES1 tystnade också. Viktigt var att användning av en kopparbindande förening återställde dessa förändringar, vilket visar att koppar i sig var central i effekten.
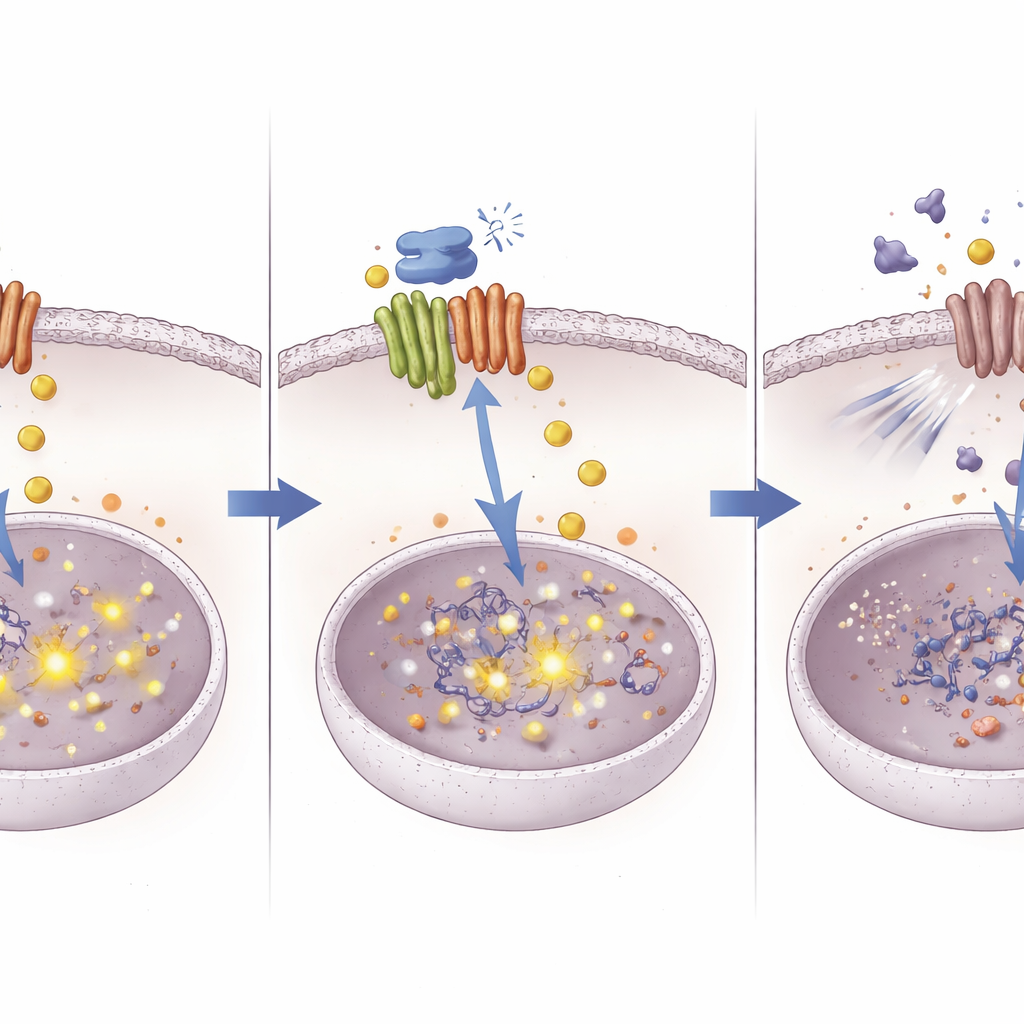
En ny väg för att få gamla läkemedel att fungera bättre
Genom att spåra vägen från ett kopparkurerprotein till DNA-nivåförändringar i en överlevnadsbana beskriver denna studie ett nytt sätt att angripa kemoterapiresistens i levercancer. Arbetet antyder att ATOX1 tillåter tumörer att hantera koppar och signalering på ett sätt som dämpar cisplatins effekt. Att blockera ATOX1 med förening 8 leder till kopparansamling, vilket i sin tur tystar NOTCH1 via DNA-metylering och tar bort ett viktigt skydd mot cisplatin. Även om förening 8 fortfarande är en experimentell molekyl, kan konceptet—att precist rikta in sig på metallhanterande proteiner för att omprogrammera cancercellers beteende—hjälpa till att återuppliva effektiviteten hos befintliga cytostatika och inspirera nya kombinationsbehandlingar.
Citering: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Nyckelord: levercancer, cisplatinresistens, kopparmetabolism, ATOX1-hämmare, Notch-signalering