Clear Sky Science · ja
CRISPR-Cas9スクリーニングが肝臓がんにおけるATOX1駆動のシスプラチン耐性機構を同定し、標的阻害剤の有効性を評価する
この研究が重要な理由
肝臓がんは世界で最も致死性の高いがんの一つであり、多くの患者はシスプラチンという一般的な化学療法薬を投与されます。しかし時間とともに腫瘍はしばしば薬剤に対する耐性を獲得し、病気が再発・進展します。本研究は、その耐性の背後にある意外な分子ドライバーを明らかにし、シスプラチンの効果を高め安全性を改善する可能性のある設計化合物を提示します。読者にとっては、現代の遺伝学、計算モデリング、化学がどのように組み合わさってがんの防御を攻略するかの一端を示す内容です。
肝腫瘍はどうやって化学療法を回避するか
シスプラチンはDNAを損傷させることでがん細胞を死に至らせますが、腫瘍は薬の排出、DNA修復の促進、あるいは生存シグナルの再配線など多様なトリックで耐性を獲得します。著者らはゲノム全体を対象とする強力な遺伝子編集ツール、CRISPR-Cas9スクリーニングを用い、2つの肝がん細胞株でほぼすべての遺伝子を系統的にノックアウトし、その後シスプラチンに曝露しました。問いは単純です:ある遺伝子が失われると、細胞は薬に対してより敏感になるか、それとも耐性を示すか。耐性に関連する数十の遺伝子の中で際立っていたのがATOX1でした。ATOX1は通常、必須金属である銅の取り扱いを助ける小さなタンパク質です。肝がん細胞は正常肝細胞よりもATOX1を多く発現しており、腫瘍でATOX1レベルが高い患者は生存率が低くシスプラチン耐性が強い傾向がありました。
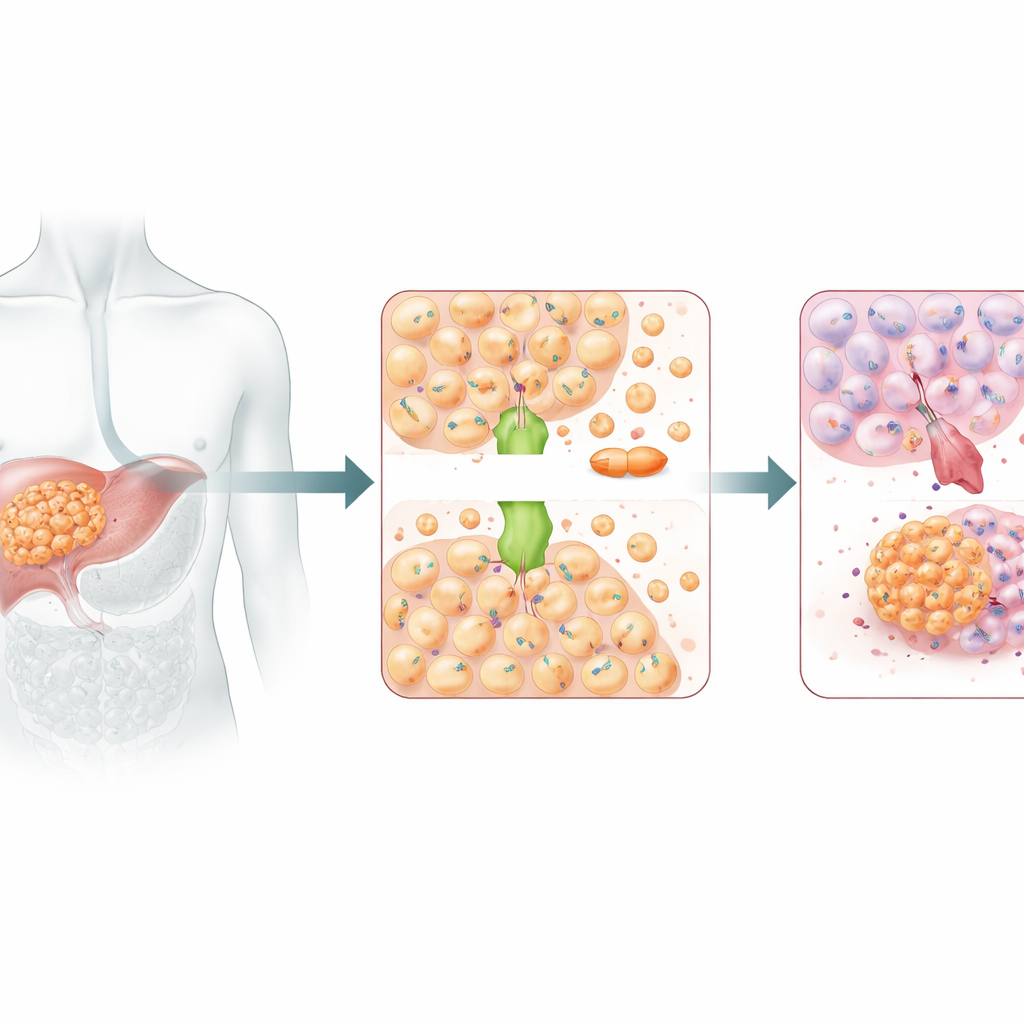
裏のある銅の運搬役
ATOX1は通常、銅イオンを細胞内で運ぶ輸送役として働き、この必須金属のバランスを保ちます。しかし銅とシスプラチンは化学的に十分に類似しているため、いくつかの同じ輸送経路を共有する可能性があります。以前の構造解析はATOX1がシスプラチンと直接結合し得ることを示唆していました。本研究では、肝がん細胞でATOX1をサイレンシングするとシスプラチンに対してはるかに脆弱になり:増殖が遅くなり、コロニー形成が減り、アポトーシスが増加しました。人体由来の肝腫瘍を移植したマウスでも、ATOX1をノックダウンするとシスプラチンで腫瘍がより効果的に縮小しました。これらの結果は総じて、ATOX1が白金系化学療法に対して肝がん細胞を耐えさせる重要な補助因子であることを示しています。
精密阻害剤の設計
銅を広く標的にするのは毒性を伴う可能性があるため、研究チームはATOX1自体を狙うことにしました。彼らはコンピュータ上でATOX1タンパク質の動きをシミュレートし、薬剤が結合し得る安定したポケットを探索し、150万件の小分子を仮想スクリーニングで試しました。数回のフィルタリングと実験室での検証を経て、候補化合物の一つ──化合物8と名付けられたもの──が強力かつ選択的な結合剤として浮上しました。生物物理学的アッセイは、化合物8がATOX1に強く結合してその構造を安定化し、従来の阻害剤が作用する関連する銅結合タンパク質にはほとんど影響を及ぼさないことを示しました。細胞実験では、化合物8は既存のATOX1薬より正常肝細胞へのダメージが少なく、単剤での抗がん活性は控えめであったものの安全域が改善されていることが示唆されました。
腫瘍に対して銅を逆手に取る
最も顕著な効果は化合物8とシスプラチンを組み合わせたときに現れました。培養皿内の肝がん細胞では、両剤併用により単剤よりも成長抑制が大きく、コロニー形成が減少し、細胞死率が上昇しました。マウスでは、併用群が最も小さい腫瘍と最も低い細胞分裂マーカーを示し、主要臓器に明らかな有害影響は見られませんでした。理由を探るために遺伝子発現を解析したところ、ATOX1を阻害するとがん細胞内に銅が蓄積することが分かりました。その銅蓄積は、NOTCH1という遺伝子の制御領域における化学的タグであるDNAメチル化の増加と関連していました。NOTCH1は腫瘍細胞がストレスに対処しDNAを修復するのを助ける経路の一部です。メチル化が増えるとNOTCH1のスイッチは抑えられ、その下流のパートナー遺伝子HES1も沈静化しました。重要な点として、銅をキレートする化合物を用いるとこれらの変化は逆転し、効果の中心に銅そのものがいることが示されました。
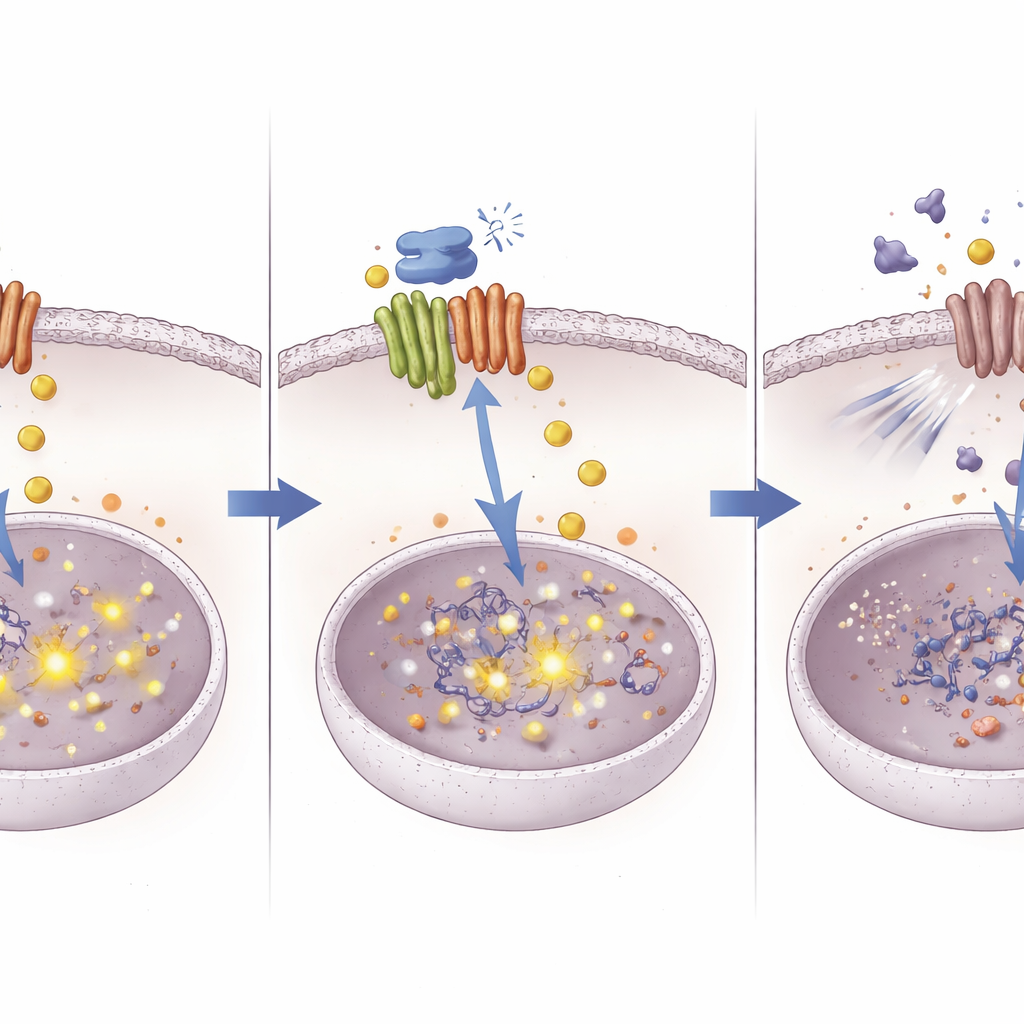
既存薬の効果を高める新たな道筋
銅の運搬タンパク質から生存経路のDNAレベルでの変化へとつながる経路をたどることで、本研究は肝臓がんの化学療法耐性に対処する新しい方法を示しています。結果は、ATOX1が腫瘍における銅とシグナル伝達を管理し、シスプラチンの効力を弱めていることを示唆します。ATOX1を化合物8で阻害すると銅が蓄積し、それがDNAメチル化を介してNOTCH1を沈黙させ、シスプラチンに対する主要な防御を取り除きます。化合物8はまだ実験段階の分子ですが、金属処理タンパク質を精密に標的化してがん細胞の挙動を書き換えるという発想は、既存の化学療法の有効性を取り戻し、新たな併用療法の開発を促す可能性があります。
引用: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
キーワード: 肝臓がん, シスプラチン耐性, 銅代謝, ATOX1阻害剤, Notchシグナル伝達