Clear Sky Science · ru
CRISPR-Cas9-скрининг выявляет механизмы резистентности к цисплатину, управляемые ATOX1, при раке печени и оценивает эффективность целевого ингибитора
Почему это исследование важно
Рак печени — один из самых смертоносных видов рака в мире, и многие пациенты получают широко применяемый химиотерапевтический препарат цисплатин. Со временем опухоли нередко вырабатывают устойчивость к нему, что позволяет болезни возвращаться и распространяться. В этом исследовании обнаружен неожиданный молекулярный виновник такой резистентности и предложено синтетическое соединение, которое может помочь цисплатину работать эффективнее и безопаснее. Для читателя это демонстрирует, как современные генетические методы, компьютерное моделирование и химия можно объединить, чтобы перехитрить защитные механизмы рака.
Как опухоли печени уворачиваются от химиотерапии
Цисплатин убивает раковые клетки, повреждая их ДНК, но опухоли могут становиться устойчивыми различными путями: выкачивая препарат, ускоренно ремонтируя ДНК или перенастраивая сигналы выживания. Авторы использовали мощный инструмент редактирования генома — геномный CRISPR-Cas9-скрининг — чтобы систематически выключить почти каждый ген в двух линиях клеток рака печени и затем подвергнуть их воздействию цисплатина. Они задали простой вопрос: при выключении какого гена клетки становятся более или менее чувствительны к препарату? Среди десятков генов, связанных с резистентностью, выделился один — ATOX1, небольшая белковая молекула, которая обычно помогает клеткам обращаться с жизненно важным металлом меди. В клетках рака печени уровень ATOX1 был выше, чем в здоровой печени, а у пациентов с опухолями, демонстрировавшими высокий уровень ATOX1, как правило, наблюдалась худшая выживаемость и большая устойчивость к цисплатину.
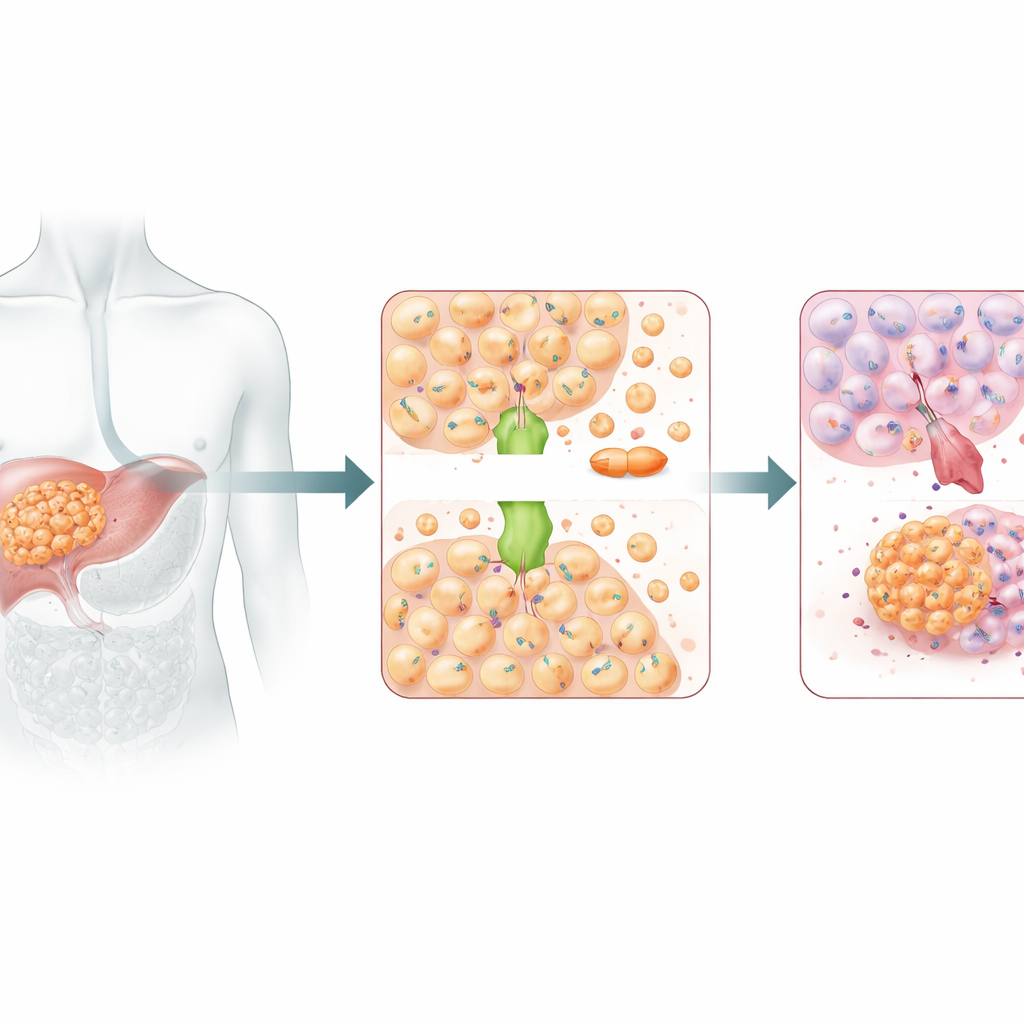
Курьер меди с темной стороной
ATOX1 обычно действует как курьер меди, перенося ионы меди внутри клетки, чтобы поддерживать баланс этого важного металла. Но медь и цисплатин достаточно похожи, чтобы использовать некоторые общие пути транспорта. Ранее структурные исследования указывали на то, что ATOX1 может связывать цисплатин напрямую. В этом исследовании подавление ATOX1 в клетках рака печени сделало их значительно более уязвимыми к цисплатину: замедлялся рост, уменьшалось образование колоний и увеличивался уровень запрограммированной гибели клеток. У мышей с гуманизированными опухолями печени снижение уровня ATOX1 также усиливало эффект цисплатина, приводя к более заметному уменьшению опухолей. В совокупности эти результаты указывали на ATOX1 как на ключевого помощника, который позволяет клеткам рака печени противостоять химиотерапии на основе платины.
Проектирование точечного блокиратора
Вместо того чтобы понижать уровень меди в целом, что может быть токсичным, команда решила блокировать сам ATOX1. Они смоделировали движение белка ATOX1 на компьютере, чтобы найти стабильные карманы для связывания лекарства, затем виртуально проверили 1,5 миллиона малых молекул на способность поместиться в эти участки. После нескольких раундов фильтрации и лабораторной валидации выделился один кандидат — названный соединением 8 — как сильный и специфичный лигант. Биофизические тесты показали, что соединение 8 прочно связывается с ATOX1 и стабилизирует его структуру, при этом оказывая мало влияния на родственный медесвязывающий белок, на который действовали старые ингибиторы. В клеточных экспериментах соединение 8 оказывало меньшее вредное воздействие на нормальные клетки печени по сравнению с предыдущими препаратами против ATOX1, указывая на более широкий запас безопасности, хотя его собственная противоопухолевая активность как монотерапии была умеренной.
Обращая медь против опухоли
Наиболее впечатляющие эффекты проявились при сочетании соединения 8 с цисплатином. В культурах клеток рака печени комбинированное применение двух препаратов сильнее тормозило рост, уменьшало образование колоний и вызывало более высокие уровни гибели клеток, чем каждый препарат по отдельности. У мышей комбинация давала наименьшие опухоли и самые низкие уровни маркеров деления клеток, без очевидного вреда основным органам. Чтобы понять механизмы, исследователи проанализировали активность генов и обнаружили, что блокада ATOX1 приводит к накоплению меди внутри раковых клеток. Это накопление меди связывали с повышением химических меток — метилирования ДНК — в регуляторной области гена NOTCH1, части пути, который помогает опухолевым клеткам выживать под стрессом и ремонтировать ДНК. Более высокое метилирование означало подавление переключателя NOTCH1, и его партнерский ген HES1 также замолчал. Важно, что применение хелатора меди обращало эти изменения, что подтверждает центральную роль самой меди в этом эффекте.
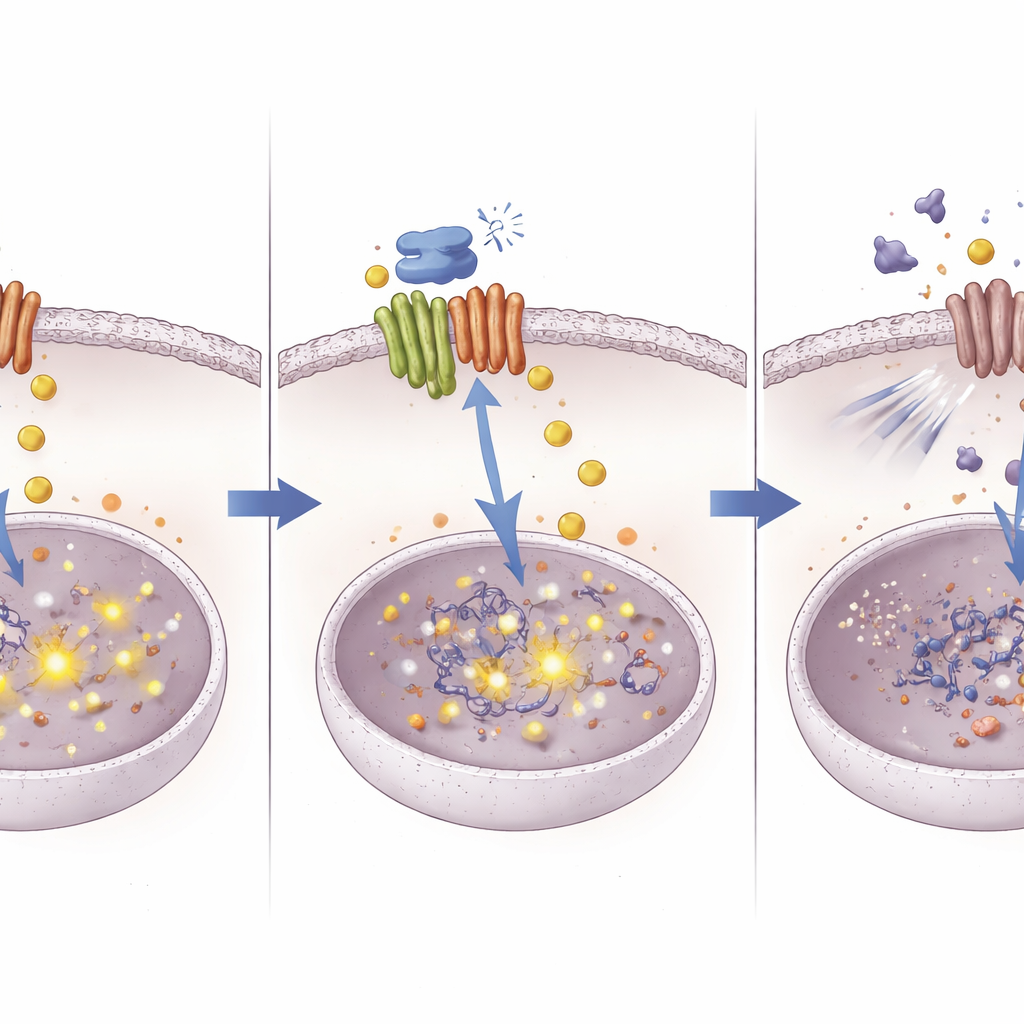
Новый путь сделать старые лекарства эффективнее
Проследив путь от белка-курьера меди до изменений на уровне ДНК в пути выживания, это исследование описывает свежий подход к преодолению резистентности к химиотерапии при раке печени. Работа указывает, что ATOX1 позволяет опухолям управлять медью и сигнальными путями таким образом, что ослабляет действие цисплатина. Блокада ATOX1 соединением 8 вызывает накопление меди, что в свою очередь выключает NOTCH1 через метилирование ДНК и устраняет важный щит против цисплатина. Хотя соединение 8 все еще остается экспериментальной молекулой, заложенная в нем идея — прицельное вмешательство в белки, обращающиеся с металлами, чтобы перенастроить поведение раковых клеток — может помочь возродить эффективность существующих химиотерапий и вдохновить новые комбинационные подходы.
Цитирование: Hu, C., Tai, H., Zhu, R. et al. CRISPR-Cas9 screening identifies ATOX1-driven cisplatin resistance mechanisms in liver cancer and evaluates targeted inhibitor efficacy. Commun Biol 9, 439 (2026). https://doi.org/10.1038/s42003-026-09722-8
Ключевые слова: рак печени, резистентность к цисплатину, метаболизм меди, ингибитор ATOX1, сигнальный путь Notch