Clear Sky Science · zh
与铜死亡相关的 PDHA1 通过 E2F1–PD-L1 轴促进肉瘤进展和免疫治疗反应:一项多组学与临床验证研究
这项研究为何重要
肉瘤虽少见但侵袭性强,常常对现代免疫疗法耐受性高。许多晚期患者在手术、化疗和放疗等标准治疗耗尽后仍面临较差的生存预后。本研究探讨了肉瘤细胞内一个隐秘的代谢开关,该开关似乎既驱动肿瘤生长,又塑造免疫系统的应答。理解这一开关可能为预测哪些患者能从免疫治疗中获益,并为更聪明的联合用药设计提供新思路。
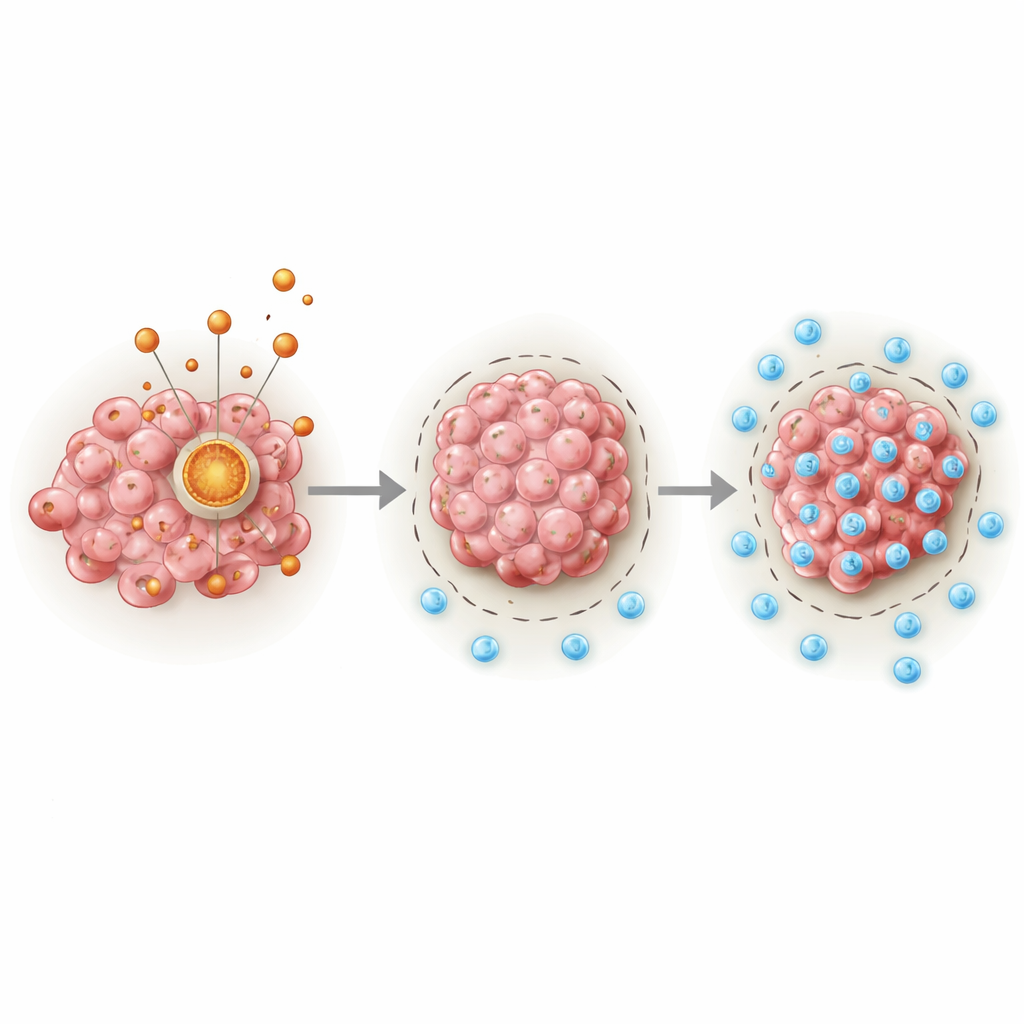
癌细胞内的隐秘发动机
研究的核心是 PDHA1,这是一种蛋白,作为糖类分解与线粒体主要能量循环之间的关键关口。作者分析了大型癌症数据库与临床样本,发现肉瘤组织中 PDHA1 水平持续高于正常组织。肿瘤中 PDHA1 较高的患者,无论年龄、性别或其他多种临床因素,生存期往往更短。研究团队将 PDHA1 水平与常规临床信息结合,构建了一个预测工具,其对一年、三年和五年生存的预测准确性优于传统指标。
代谢如何重塑肿瘤邻域
除了直接驱动增殖,PDHA1 还重塑了肿瘤的“邻域”——即围绕肿瘤的免疫与基质细胞混合体。使用从整体肿瘤 RNA 推断免疫细胞类型的计算方法,以及对单个免疫细胞的单细胞测序,作者显示 PDHA1 不仅在肿瘤细胞中活跃,在许多免疫细胞群体中亦然,尤其是 T 细胞与髓系细胞。PDHA1 高表达的肉瘤倾向于呈现“免疫被排斥”状态的特征:深处肿瘤内的有效杀伤性 T 细胞减少,硬化、纤维化的基质信号增多,以及免疫细胞被限制在肿瘤边缘而无法有效攻击的模式。
阻断免疫攻击的分子链
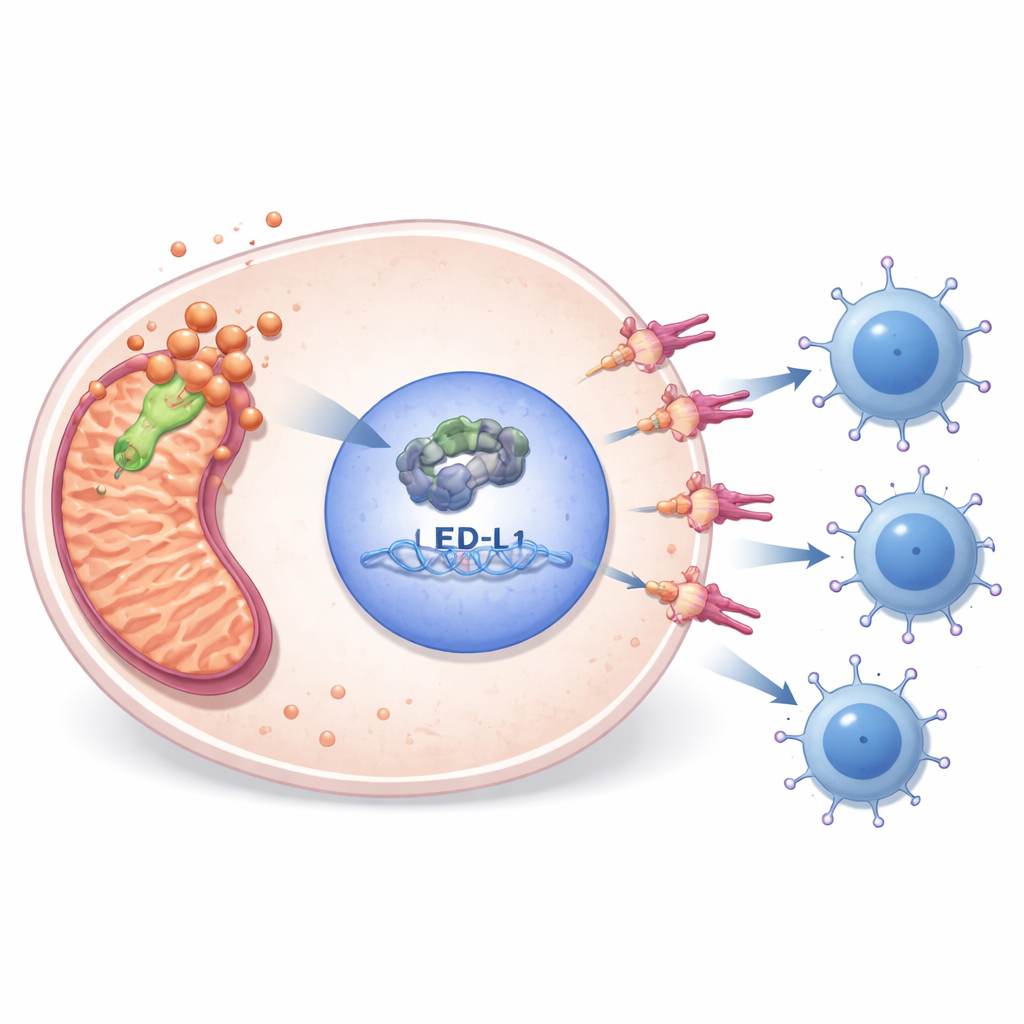
体外实验揭示了 PDHA1 如何将代谢与免疫逃逸连接起来。当研究者在肉瘤细胞系中下调 PDHA1 时,细胞增殖减少、迁移能力下降、克隆形成减少且程序性细胞死亡增加。与此同时,作为细胞分裂相关基因核内调控因子的 E2F1 和肿瘤细胞表面的免疫“刹车”分子 PD-L1 水平均下降。通过查阅公共的 DNA 结合数据并进行靶向实验,团队证明 E2F1 能直接结合 PD-L1 基因的调控区并激活其转录。在 PDHA1 缺失的细胞中恢复 E2F1 会使 PD-L1 水平回升并部分挽救细胞存活,表明 PDHA1 位于一个 E2F1–PD-L1 分子链的上游,该链帮助肿瘤逃避免疫 T 细胞的攻击。
与铜相关的细胞死亡及药物机会
PDHA1 还与一种最近描述的由铜触发的细胞死亡形式——铜致死(cuproptosis)相关。研究显示,通过药物阻断铜的可用性可降低与该通路相关的一个脂酰化线粒体蛋白,并抑制 PDHA1–E2F1–PD-L1 链条,尤其是在联合 PDHA1 下调时效应更明显。基因组与表观遗传分析提示,高 PDHA1 常与特定 DNA 变化、PDHA1 基因低甲基化以及与更具侵袭性的肿瘤相关的 RNA 修饰模式共现。药物筛选数据库和细胞实验指向了若干药物——例如代谢药物 phenformin 与 E2F1 通路抑制剂——这些药物在 PDHA1 活跃的肉瘤中可能特别有效,提示可与免疫检查点抑制剂进行合理组合。
将不良信号转化为治疗指南
在动物模型与患者活检中,PDHA1 高表达的肿瘤体积更大、增殖更强、PD-L1 含量更高且 CD8⁺ 杀伤性 T 细胞浸润更少。然而,这些 PDHA1 高肿瘤同时也表现出一些常与更好免疫检查点抑制反应相关的特征——如更高的突变负荷和更强的检查点信号。在一组接受此类免疫治疗的晚期肉瘤患者小队列中,PDHA1 高表达者更有可能获益。对普通读者而言,结论是 PDHA1 既是肉瘤生长的油门,也是免疫防御的盾牌,但恰恰这种行为可能在正确的抑制措施下使肿瘤更脆弱。测量并靶向 PDHA1 因此有望帮助识别高风险患者、指导免疫疗法的应用,并为难治性肉瘤提供新的代谢—免疫联合用药策略的灵感。
引用: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
关键词: 肉瘤 免疫治疗, 癌症 代谢, PDHA1, 免疫检查点 阻断, 肿瘤 微环境