Clear Sky Science · it
PDHA1 associato alla cuproptosi promuove la progressione del sarcoma e la risposta all’immunoterapia attraverso l’asse E2F1–PD-L1: uno studio di convalida multi-omica e clinica
Perché questa ricerca è importante
I sarcomi sono tumori rari ma aggressivi che spesso resistono ai trattamenti immunitari moderni. Molti pazienti con malattia avanzata esauriscono le opzioni standard come chirurgia, chemioterapia e radioterapia, ma continuano a registrare una sopravvivenza scarsa. Questo studio esplora un interruttore metabolico nascosto all’interno delle cellule di sarcoma che sembra sia alimentare la crescita tumorale sia modellare la risposta del sistema immunitario. Comprendere questo interruttore potrebbe aprire nuove vie per prevedere quali pazienti traggono beneficio dall’immunoterapia e per progettare combinazioni terapeutiche più intelligenti.
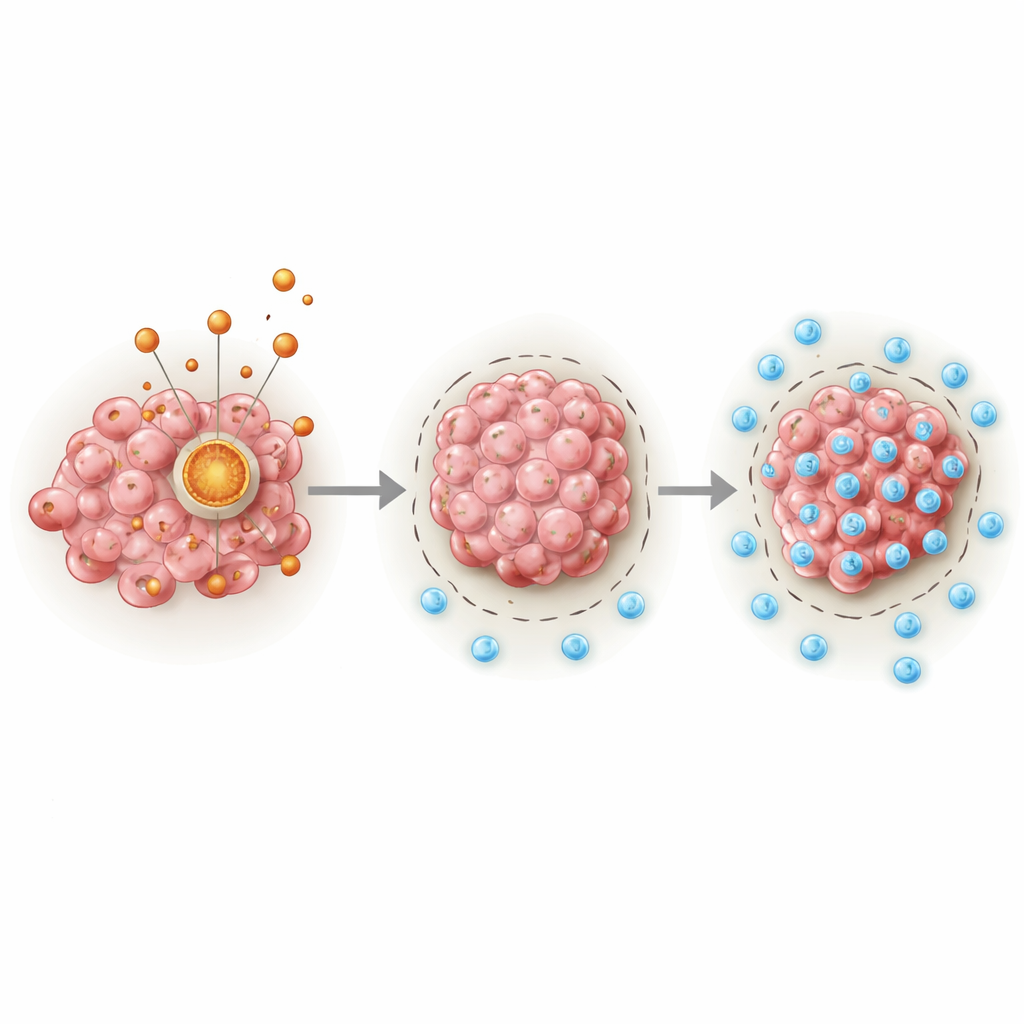
Un motore nascosto dentro le cellule tumorali
Al centro della storia c’è PDHA1, una proteina che funge da portale chiave tra la degradazione degli zuccheri e il principale ciclo energetico della cellula nei mitocondri. Gli autori hanno analizzato ampi database sul cancro e campioni clinici e hanno scoperto che i sarcomi presentano costantemente livelli più alti di PDHA1 rispetto ai tessuti normali. I pazienti i cui tumori avevano più PDHA1 tendevano a vivere meno a lungo, indipendentemente da età, sesso o altri fattori clinici. Combinando i livelli di PDHA1 con le informazioni cliniche standard, il gruppo ha costruito uno strumento predittivo che stima la sopravvivenza a uno, tre e cinque anni con maggiore accuratezza rispetto alle misure tradizionali da sole.
Come il metabolismo modella il quartiere tumorale
Oltre a promuovere la crescita, PDHA1 sembra rimodellare il “quartiere” tumorale — il mix di cellule immunitarie e di supporto che circonda il cancro. Utilizzando metodi computazionali che inferiscono i tipi cellulari immunitari dall’RNA totale tumorale, insieme al sequenziamento a singola cellula di cellule immunitarie individuali, gli autori hanno mostrato che PDHA1 è attivo non solo nelle cellule tumorali ma anche in molte popolazioni immunitarie, in particolare nelle cellule T e nelle cellule mieloidi. I sarcomi con alto PDHA1 tendevano a presentare segni di uno stato di “esclusione immunitaria”: meno cellule T citotossiche utili all’interno profondo del tumore, più segnali di stroma fibroso e rigido, e schemi che suggeriscono che le cellule immunitarie venivano tenute ai margini anziché poter attaccare.
Una catena molecolare che blocca l’attacco immunitario
Esperimenti di laboratorio hanno svelato come PDHA1 colleghi il metabolismo all’evasione immunitaria. Quando i ricercatori riducevano i livelli di PDHA1 in linee cellulari di sarcoma, le cellule si dividevano meno, si muovevano meno, formavano meno colonie e andavano incontro a maggiore morte cellulare programmata. Allo stesso tempo, calavano i livelli di E2F1 — un regolatore nucleare di geni coinvolti nella divisione cellulare — e di PD-L1 — un “freno” immunitario sulla superficie delle cellule tumorali. Esaminando dati pubblici di legame al DNA e effettuando esperimenti mirati, il gruppo ha mostrato che E2F1 si lega direttamente alla regione di controllo del gene PD-L1 e ne attiva l’espressione. Ripristinare E2F1 in cellule carenti di PDHA1 riportava i livelli di PD-L1 e parzialmente salvaguardava la sopravvivenza cellulare, collocando PDHA1 a monte di una catena E2F1–PD-L1 che aiuta i tumori a nascondersi dalle cellule T.
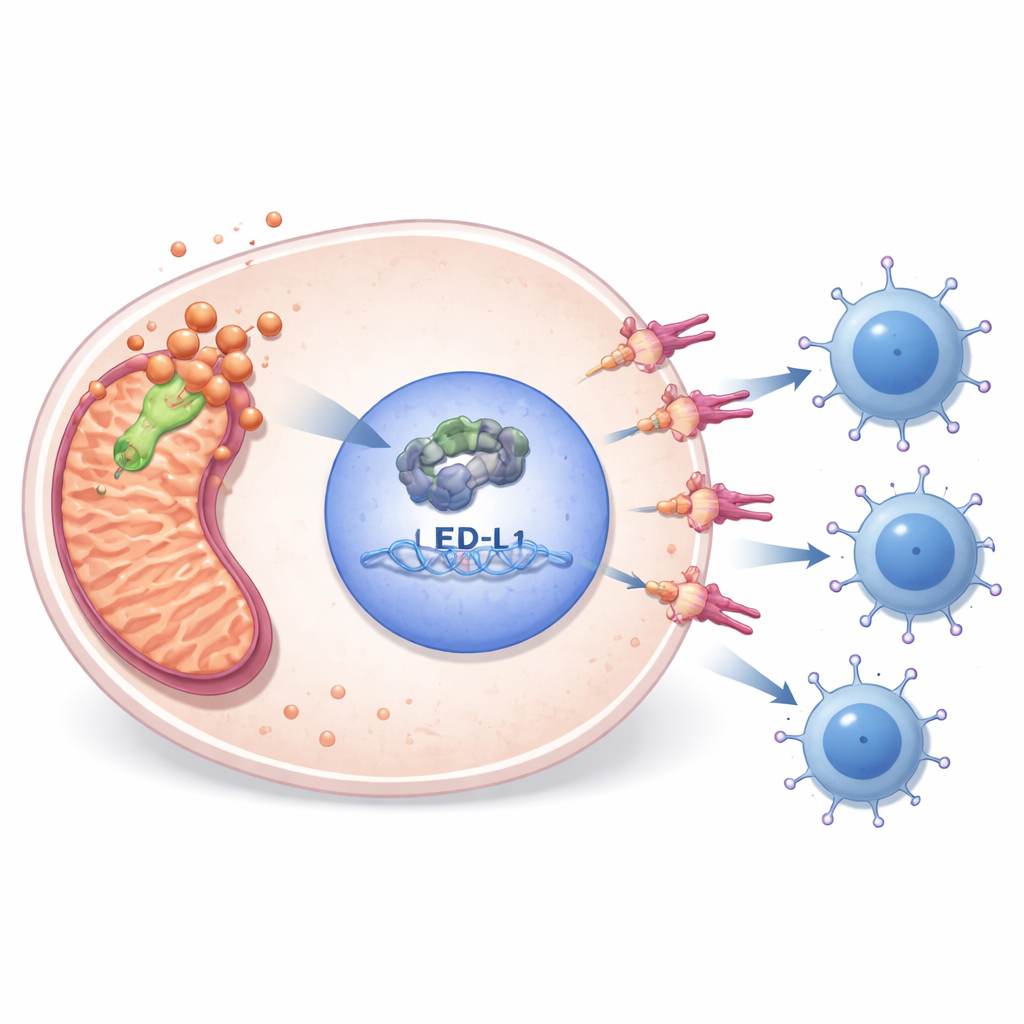
Morte cellulare legata al rame e opportunità farmacologiche
PDHA1 è inoltre collegato a una forma di morte cellulare recentemente descritta e indotta dal rame, chiamata cuproptosi. Lo studio ha mostrato che bloccare la disponibilità di rame con un farmaco riduceva una proteina mitocondriale lipoilata associata a questa via e attenuava la catena PDHA1–E2F1–PD-L1, soprattutto se combinato con il silenziamento di PDHA1. Analisi genomiche ed epigenetiche suggerivano che alti livelli di PDHA1 spesso coincidono con alterazioni del DNA, bassa metilazione del gene PDHA1 e schemi di modificazione dell’RNA associati a tumori più aggressivi. Banche dati di screening farmacologico e saggi cellulari indicavano diversi farmaci — come l’agente metabolico phenformin e un inibitore della via E2F1 — a cui i sarcomi con PDHA1 attivo potrebbero essere particolarmente sensibili, facendo intravedere combinazioni razionali con inibitori dei checkpoint immunitari.
Trasformare un cattivo segno in una guida terapeutica
In modelli animali e in biopsie di pazienti, i tumori con alto PDHA1 erano più grandi, più proliferativi, più ricchi di PD-L1 e meno infiltrati da cellule T CD8⁺ citotossiche. Eppure questi stessi tumori ad alto PDHA1 mostravano anche caratteristiche — come maggiore burden mutazionale e segnali di checkpoint più forti — che spesso si associano a risposte migliori ai farmaci che bloccano PD-1 o PD-L1. In una piccola coorte clinica di pazienti con sarcoma avanzato trattati con tale immunoterapia, chi presentava alti livelli di PDHA1 aveva maggiori probabilità di beneficiare. Per il lettore non specialista, la conclusione è che PDHA1 agisce sia come acceleratore della crescita del sarcoma sia come scudo contro l’attacco immunitario, ma questo stesso comportamento può rendere questi tumori più vulnerabili una volta applicati i freni appropriati. Misurare e mirare PDHA1 potrebbe quindi aiutare a identificare pazienti ad alto rischio, guidare l’uso dell’immunoterapia e ispirare nuove combinazioni metabolico-immunitarie per sarcomi resistenti.
Citazione: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Parole chiave: immunoterapia del sarcoma, metabolismo del cancro, PDHA1, blocco dei checkpoint immunitari, microambiente tumorale