Clear Sky Science · sv
Cuproptos-associerad PDHA1 främjar sarkomtillväxt och immunoterapikänslighet via E2F1–PD-L1-axeln: en multi-omisk och klinisk valideringsstudie
Varför denna forskning är viktig
Sarkom är sällsynta men aggressiva tumörer som ofta står emot moderna immunbaserade behandlingar. Många patienter med avancerad sjukdom har uttömt standardalternativ som operation, cytostatika och strålning, men har ändå dålig överlevnad. Denna studie undersöker en dold metabolisk omskopplare i sarkomceller som tycks både driva tumörtillväxt och forma hur immunsystemet reagerar. Att förstå denna omskopplare kan öppna nya möjligheter att förutsäga vilka patienter som gynnas av immunoterapi och att utforma smartare kombinationsbehandlingar.
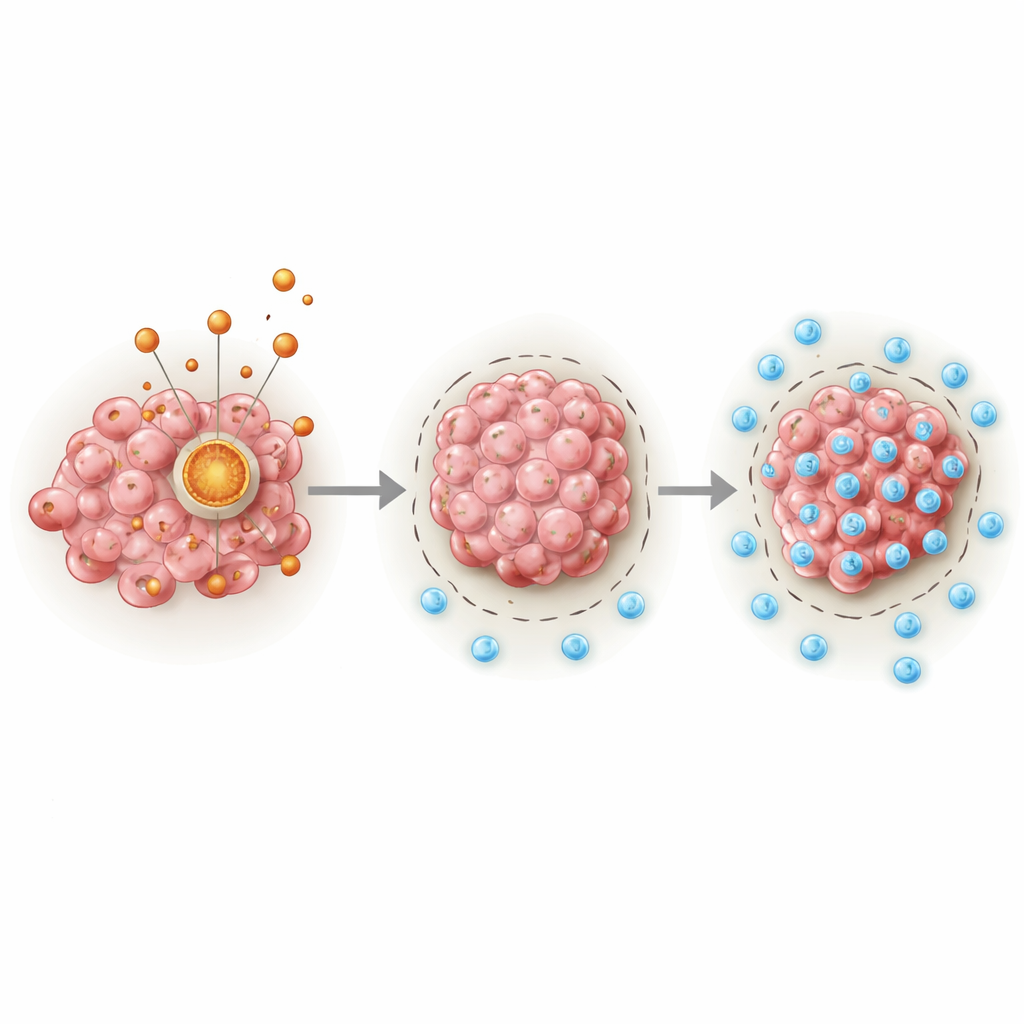
En dold motor inne i cancercellerna
I centrum för berättelsen står PDHA1, ett protein som fungerar som en nyckelport mellan glukosnedbrytning och cellens huvudenergicykel i mitokondrierna. Författarna analyserade stora cancerregister och kliniska prover och fann att sarkom konsekvent uppvisar högre nivåer av PDHA1 än normalt vävnad. Patienter vars tumörer hade mer PDHA1 tenderade att leva kortare tid, oberoende av ålder, kön eller flera andra kliniska faktorer. Genom att kombinera PDHA1-nivåer med standardklinisk information byggde teamet ett prediktionsverktyg som uppskattade ett-, tre- och femårsöverlevnad mer exakt än traditionella mått ensamma.
Hur metabolismen formar tumörnärmiljön
Utöver att driva tillväxt verkade PDHA1 omforma tumörens omgivning — blandningen av immunceller och stödjeceller som omger cancern. Med hjälp av beräkningsmetoder som härleder immuncellstyper från bulk tumör-RNA, samt enkelcellssekvensering av individuella immunceller, visade författarna att PDHA1 är aktiv inte bara i tumörceller utan även över många immuncellpopulationer, särskilt T-celler och myeloida celler. Sarkom med hög PDHA1 visade ofta tecken på ett ”immun-exkluderat” tillstånd: färre hjälpsamma cytotoxiska T-celler djupt inne i tumören, fler signaler om stel, fibrös stroma och mönster som tyder på att immunceller hålls i periferin istället för att tillåtas attackera.
En molekylär kedja som blockerar immunistöt
Laboratorieexperiment visade hur PDHA1 kopplar metabolism till immunflykt. När forskarna minskade PDHA1-nivåerna i sarkomcellinjer delade cellerna sig mindre, rörde sig mindre, bildade färre kolonier och genomgick mer programmerad celldöd. Samtidigt sjönk nivåerna av E2F1 — en nukleär regulator av gener involverade i celldelning — och PD-L1 — en immunologisk ”broms” på tumörcellernas yta. Genom att granska offentliga DNA-bindningsdata och utföra riktade experiment visade teamet att E2F1 direkt binder till regleringsregionen för PD-L1-genen och aktiverar den. Återställande av E2F1 i PDHA1-defekta celler återställde PD-L1 och räddade delvis cellsurvival, vilket placerar PDHA1 uppströms i en E2F1–PD-L1-kedja som hjälper tumörer att gömma sig från T-celler.
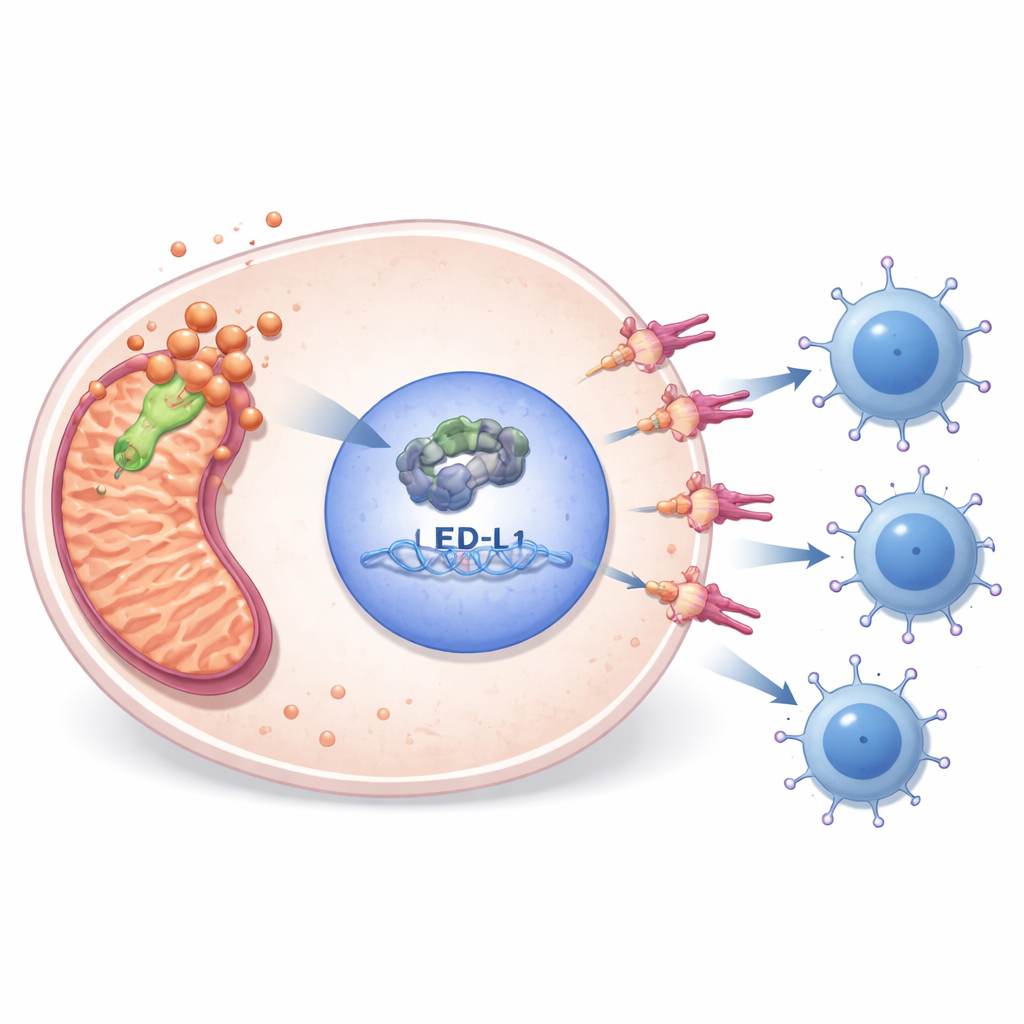
Koppling till kopparutlösta celldöd och läkemedelsmöjligheter
PDHA1 är också kopplat till en nyligen beskriven form av celldöd utlösts av koppar, kallad cuproptos. Studien visade att blockering av koppartillgänglighet med ett läkemedel minskade ett lipoylerat mitokondriellt protein kopplat till denna bana och dämpade PDHA1–E2F1–PD-L1-kedjan, särskilt i kombination med PDHA1-nedsättning. Genom genomiska och epigenetiska analyser antyddes att hög PDHA1 ofta sammanfaller med DNA-förändringar, låg metylering av PDHA1-genen och RNA-modifieringsmönster associerade med mer aggressiva tumörer. Läkemedels-skärningsdatabaser och cellbaserade tester pekade på flera läkemedel — såsom den metabola agenten phenformin och en E2F1-vägsinhibitor — som sarkom med aktiv PDHA1 kan vara särskilt känsliga för, vilket antyder rationella kombinationer med immunkontrollpunktshämmare.
Att vända en dålig markör till en behandlingsguide
I djurmodeller och patientbiopsier var tumörer med hög PDHA1 större, mer proliferativa, rikare på PD-L1 och fattigare på CD8⁺ cytotoxiska T-cellsinfiltrat. Ändå visade dessa hög-PDHA1-tumörer också egenskaper — som högre mutationsbörda och starkare checkpoint-signaler — som ofta förknippas med bättre svar på läkemedel som blockerar PD-1 eller PD-L1. I en liten klinisk kohort av avancerade sarkompatienter som fick sådan immunoterapi var de med hög PDHA1 mer benägna att dra nytta av behandlingen. För en lekmannaläsare blir slutsatsen att PDHA1 fungerar både som en gaspedal för sarkomtillväxt och som en sköld mot immunsvar, men just detta beteende kan göra dessa tumörer mer sårbara när rätt bromsar tillämpas. Att mäta och rikta PDHA1 skulle därför kunna hjälpa identifiera högriskpatienter, vägleda användningen av immunoterapi och inspirera till nya metabolisk–immunologiska läkemedelskombinationer för svårbehandlade sarkom.
Citering: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Nyckelord: sarkomimmunoterapi, cancermetabolism, PDHA1, hämning av immunkontrollpunkter, tumörmikromiljö