Clear Sky Science · tr
Cuproptosis ile ilişkili PDHA1, E2F1–PD-L1 ekseni aracılığıyla sarkom ilerlemesini ve immünoterapi yanıtını artırır: çoklu -omik ve klinik doğrulama çalışması
Bu araştırma neden önemli
Sarkomlar nadir fakat agresif kanserlerdir ve sıklıkla modern immün temelli tedavilere direnç gösterirler. İleri evre birçok hasta cerrahi, kemoterapi ve radyasyon gibi standart seçenekleri tükettikten sonra bile kötü sağkalımla karşılaşır. Bu çalışma, hem tümör büyümesini destekleyen hem de bağışıklık sisteminin yanıtını şekillendiren hücre içi gizli bir metabolik anahtarı araştırıyor. Bu anahtarın anlaşılması, hangi hastaların immünoterapiden yararlanacağını öngörmede ve daha akıllı kombinasyon tedavileri tasarlamada yeni yollar açabilir.
Kanser hücreleri içinde gizli bir motor
Hikayenin merkezinde, şeker yıkımı ile mitokondrideki başlıca enerji döngüsü arasında ana bir geçit görevi gören PDHA1 proteini var. Yazarlar büyük kanser veri tabanlarını ve klinik örnekleri analiz ederek sarkomların normal dokulara kıyasla tutarlı şekilde daha yüksek PDHA1 düzeyleri taşıdığını buldular. Tümörü daha yüksek PDHA1 içeren hastaların, yaş, cinsiyet veya diğer birkaç klinik faktörden bağımsız olarak daha kısa yaşam sürelerine sahip olma eğiliminde olduğu görüldü. PDHA1 düzeylerini standart klinik bilgilerle birleştirerek ekip, bir-, üç- ve beş yıllık sağkalımı geleneksel ölçütlerden daha doğru tahmin eden bir araç geliştirdi.
Metabolizmanın tümör çevresini nasıl şekillendirdiği
Sadece büyümeyi tetiklemekle kalmayıp, PDHA1 tümörün çevresindeki hücre karışımını—kanseri çevreleyen immün ve destek hücrelerini—yeniden şekillendiriyor gibi göründü. Toplu tümör RNA’sından immün hücre tiplerini çıkaran hesaplamalı yöntemlerin yanı sıra tek hücre dizilemesi kullanarak yazarlar, PDHA1’in yalnızca tümör hücrelerinde değil, özellikle T hücreleri ve miyeloid hücreler olmak üzere birçok immün popülasyonda da aktif olduğunu gösterdiler. Yüksek PDHA1’e sahip sarkomlar, tümörün derinliklerindeki faydalı öldürücü T hücrelerinin azalması, daha fazla sert, lifli stroma işaretleri ve immün hücrelerin saldırmasına izin verilmeyip kenarda tutulduğunu düşündüren desenler gibi “immün-dışlanmış” bir duruma ilişkin bulgular sergileme eğilimindeydi.
İmmün saldırıyı engelleyen moleküler zincir
Laboratuvar deneyleri PDHA1’in metabolizmayı immün kaçışa nasıl bağladığını ortaya koydu. Araştırmacılar sarkom hücre hatlarında PDHA1 düzeylerini azaltınca hücrelerin daha az bölündüğü, daha az hareket ettiği, daha az koloni oluşturduğu ve daha fazla programlı hücre ölümü geçirdiği görüldü. Aynı zamanda hücre bölünmesi ile ilişkili genlerin çekirdek düzenleyicisi olan E2F1 ile tümör hücresi yüzeyindeki bir immün “fren” olan PD-L1 seviyeleri de düştü. Halka açık DNA-bağlanma verilerini inceleyip hedefli deneyler yaparak ekip, E2F1’in PD-L1 geninin kontrol bölgesine doğrudan bağlandığını ve onu etkinleştirdiğini gösterdi. PDHA1 eksikliğinde E2F1’in geri getirilmesi PD-L1’i yeniden yükseltti ve hücre sağkalımını kısmen kurtardı; bu da PDHA1’i, tümörlerin T hücrelerinden saklanmasına yardımcı olan E2F1–PD-L1 zincirinin üstünde konumlandırdı.
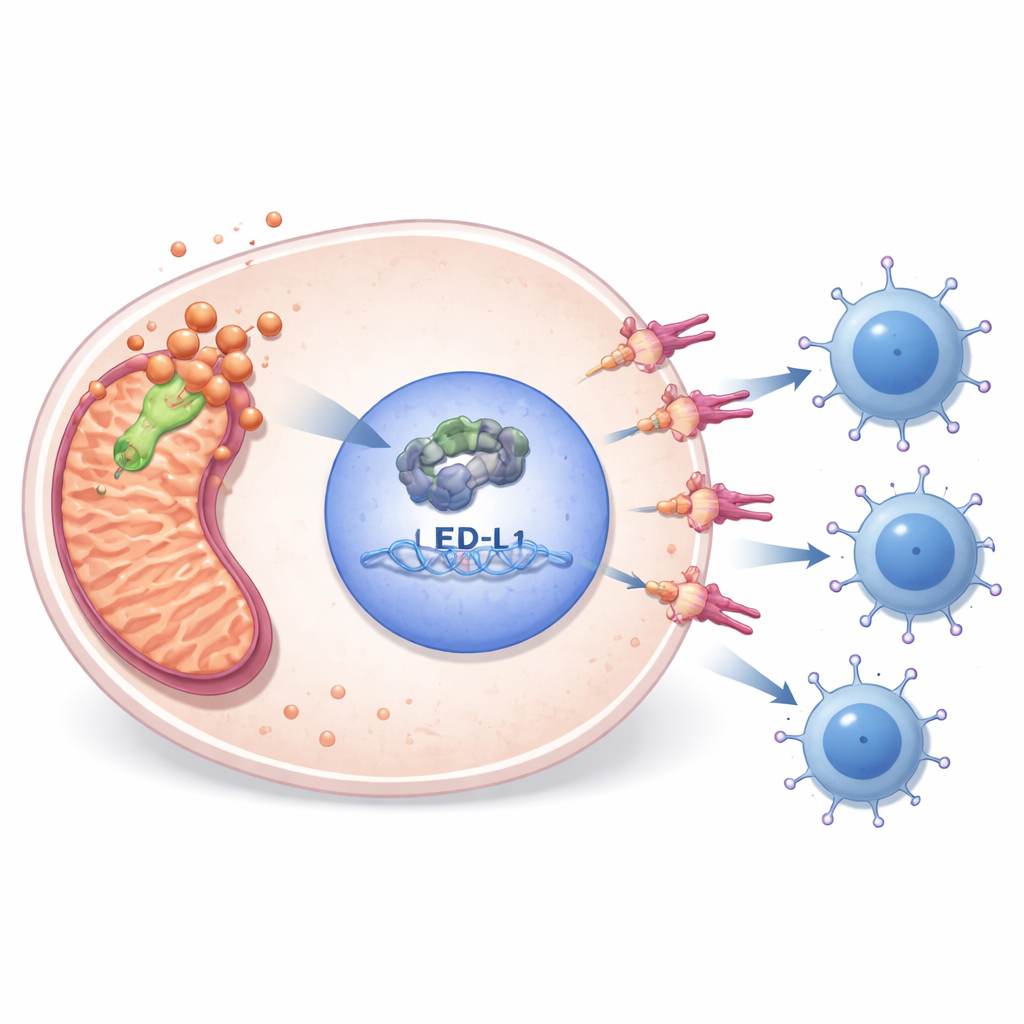
Bakır ilişkili hücre ölümü ve ilaç fırsatları
PDHA1 ayrıca bakır tarafından tetiklenen yakın zamanda tanımlanmış bir hücre ölümü türü olan cuproptosis ile bağlantılıdır. Çalışma, bakır kullanılabilirliğini bir ilaçla engellemenin bu yolakla ilişkili lipoyle olmuş bir mitokondriyal proteinin düzeyini azalttığını ve özellikle PDHA1 susturulmasıyla birleştirildiğinde PDHA1–E2F1–PD-L1 zincirini zayıflattığını gösterdi. Genomik ve epigenetik analizler, yüksek PDHA1’in genellikle DNA değişiklikleri, PDHA1 geninin düşük metilasyonu ve daha agresif tümörlerle ilişkilendirilen RNA modifikasyon desenleriyle örtüştüğünü öne sürdü. İlaç tarama veri tabanları ve hücre bazlı testler, metabolik ajan fenformin ve bir E2F1-yolak inhibitörü gibi, aktif PDHA1’e sahip sarkomların özellikle duyarlı olabileceği birkaç ilaca işaret etti; bu da immün kontrol noktası inhibitörleriyle mantıklı kombinasyonlara dair ipuçları verdi.
Kötü bir işareti tedavi rehberine çevirmek
Hayvan modellerinde ve hasta biyopsilerinde yüksek PDHA1’e sahip tümörler daha büyük, daha proliferatif, PD-L1 bakımından zengin ve CD8⁺ öldürücü T hücre infiltrasyonundan daha fakirdi. Yine de bu yüksek-PDHA1 tümörleri aynı zamanda daha yüksek mutasyon yükü ve daha güçlü kontrol noktası sinyalleri gibi, PD-1 veya PD-L1’i bloke eden ilaçlara daha iyi yanıtlarla ilişkili olan özellikler de gösteriyordu. Bu tür immünoterapi alan ileri evre sarkom hastalarının küçük bir klinik kohortunda yüksek PDHA1’e sahip olanlar fayda görme olasılığı daha yüksekti. Genel okuyucu için çıkarım şudur: PDHA1 hem sarkom büyümesi için bir gaz pedalı hem de immün saldırıya karşı bir kalkan görevi görüyor; ancak bu davranış, doğru frenler uygulandığında bu tümörleri daha savunmasız hale getirebilir. PDHA1’in ölçülmesi ve hedeflenmesi, yüksek riskli hastaların belirlenmesine, immünoterapi kullanımının yönlendirilmesine ve inatçı sarkomlar için yeni metabolik–immün ilaç kombinasyonlarının ilham kaynağı olmasına yardımcı olabilir.
Atıf: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Anahtar kelimeler: sarkom immünoterapi, kanser metabolizması, PDHA1, immün kontrol noktası engellemesi, tümör mikroçevresi