Clear Sky Science · fr
La PDHA1 associée à la cuproptose favorise la progression du sarcome et la réponse à l’immunothérapie via l’axe E2F1–PD-L1 : une étude de validation multi-omique et clinique
Pourquoi cette recherche est importante
Les sarcomes sont des cancers rares mais agressifs qui résistent souvent aux traitements immunitaires modernes. De nombreux patients atteints d’une maladie avancée ont épuisé les options standards comme la chirurgie, la chimiothérapie et la radiothérapie, et présentent néanmoins un pronostic sombre. Cette étude explore un interrupteur métabolique caché à l’intérieur des cellules de sarcome qui semble à la fois alimenter la croissance tumorale et façonner la réponse du système immunitaire. Comprendre cet interrupteur pourrait ouvrir de nouvelles voies pour prédire quels patients bénéficieront de l’immunothérapie et pour concevoir des traitements combinés plus intelligents.
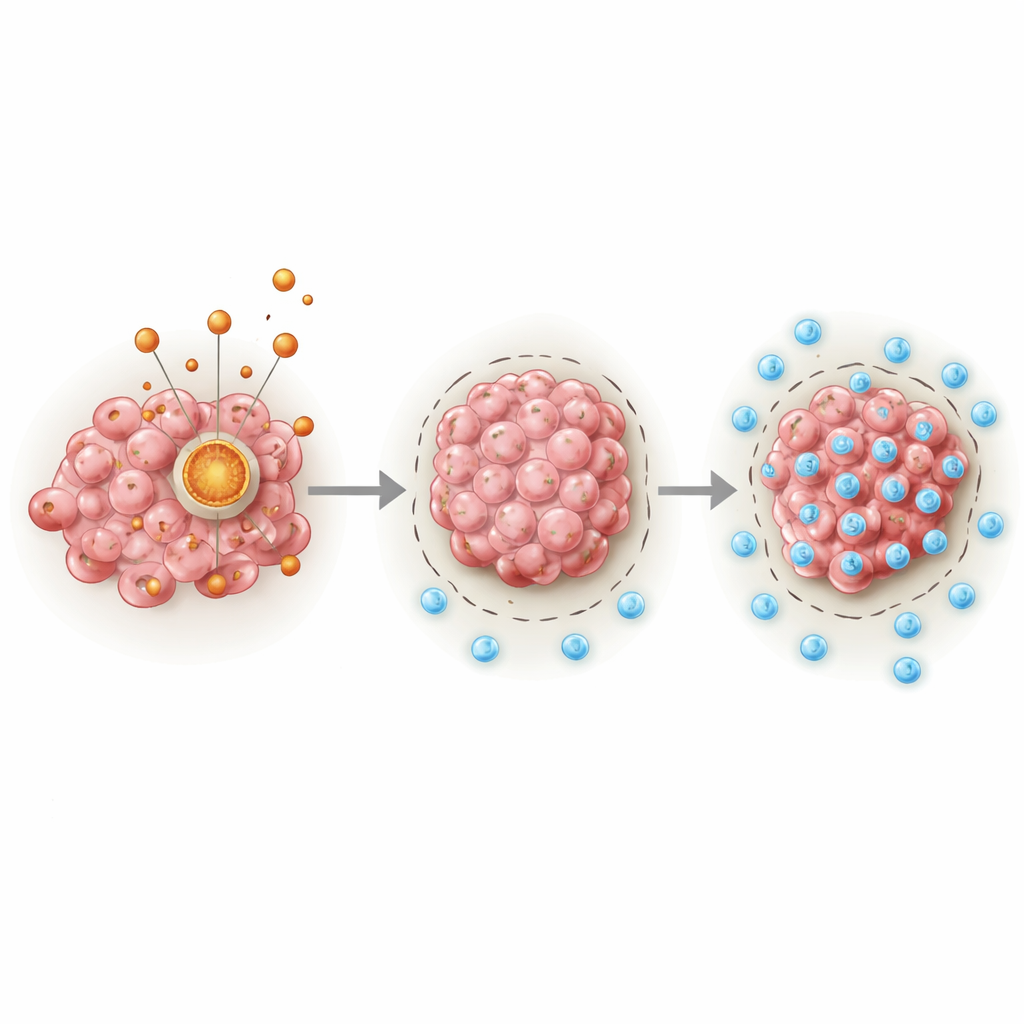
Un moteur caché à l’intérieur des cellules cancéreuses
Au centre de cette histoire se trouve PDHA1, une protéine qui joue le rôle de porte d’entrée clé entre la dégradation du glucose et le principal cycle énergétique de la cellule dans les mitochondries. Les auteurs ont analysé de larges bases de données sur le cancer et des échantillons cliniques et ont constaté que les sarcomes présentent systématiquement des niveaux de PDHA1 supérieurs aux tissus normaux. Les patients dont les tumeurs exprimaient davantage de PDHA1 avaient tendance à vivre moins longtemps, indépendamment de l’âge, du sexe ou d’autres facteurs cliniques. En combinant les niveaux de PDHA1 avec des informations cliniques standard, l’équipe a construit un outil de prédiction estimant la survie à un, trois et cinq ans avec une précision supérieure aux mesures traditionnelles seules.
Comment le métabolisme façonne le voisinage tumoral
Au-delà de son simple rôle dans la croissance, PDHA1 semblait remodeler le microenvironnement tumoral — le mélange de cellules immunitaires et de cellules de soutien entourant la tumeur. À l’aide de méthodes informatiques inférant les types cellulaires immunitaires à partir de l’ARN tumoral en masse, ainsi que du séquençage unicellulaire d’éléments immunitaires individuels, les auteurs ont montré que PDHA1 est actif non seulement dans les cellules tumorales mais aussi dans de nombreuses populations immunitaires, en particulier les lymphocytes T et les cellules myéloïdes. Les sarcomes à forte expression de PDHA1 montraient des signes d’un état « excluant l’immunité » : moins de lymphocytes T cytotoxiques utiles profondément au sein de la tumeur, davantage de signaux d’un stroma rigide et fibreux, et des schémas suggérant que les cellules immunitaires étaient maintenues en périphérie plutôt que laissées attaquer.
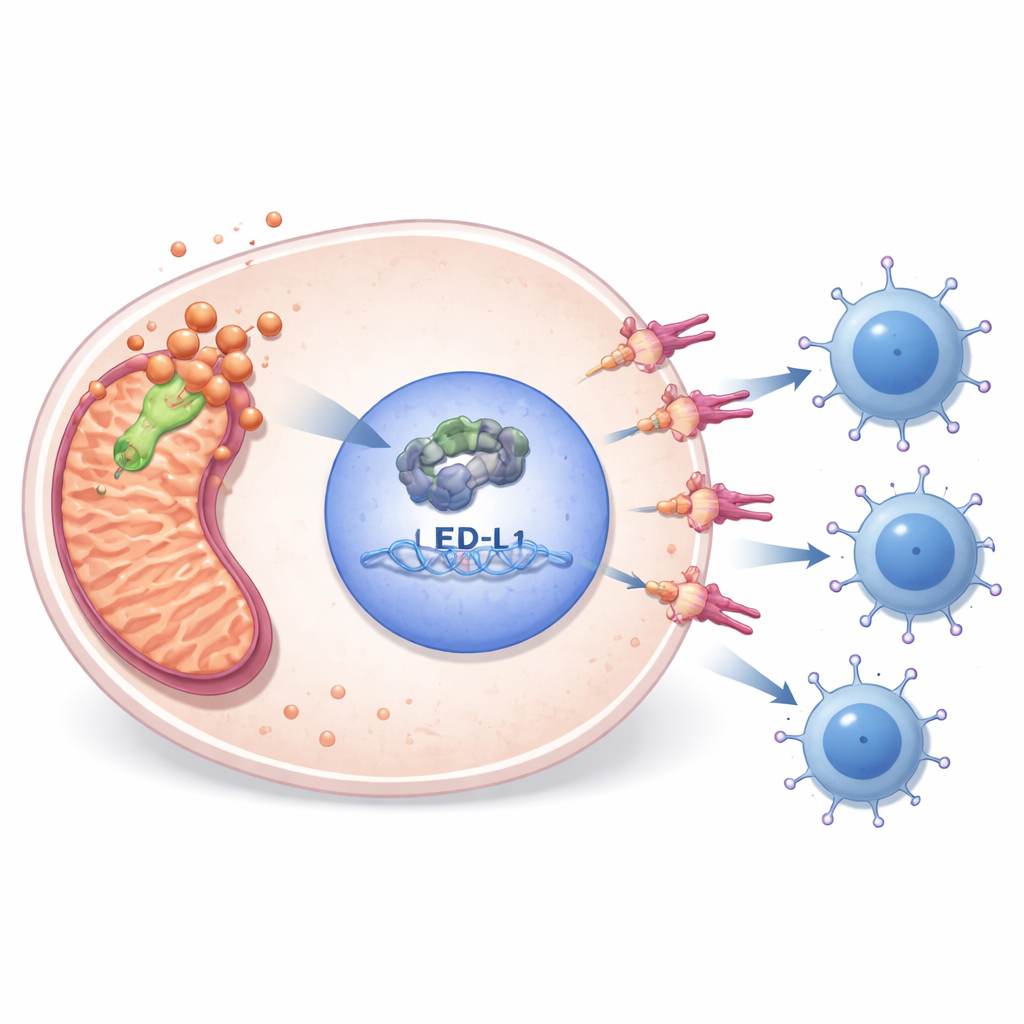
Une chaîne moléculaire qui bloque l’attaque immunitaire
Des expériences en laboratoire ont révélé comment PDHA1 relie le métabolisme à l’échappement immunitaire. Lorsque les chercheurs ont réduit l’expression de PDHA1 dans des lignées de sarcome, les cellules se divisaient moins, migraient moins, formaient moins de colonies et déclenchaient davantage de mort cellulaire programmée. Parallèlement, les niveaux d’E2F1 — un régulateur nucléaire des gènes impliqués dans la division cellulaire — et de PD-L1 — un « frein » immunitaire à la surface des cellules tumorales — ont tous deux diminué. En examinant des données publiques de liaison à l’ADN et en réalisant des expériences ciblées, l’équipe a montré qu’E2F1 se lie directement à la région de contrôle du gène PD-L1 et l’active. La restauration d’E2F1 dans des cellules déficientes en PDHA1 a rétabli PD-L1 et partiellement sauvé la survie cellulaire, plaçant PDHA1 en amont d’une chaîne E2F1–PD-L1 qui aide les tumeurs à se dissimuler des lymphocytes T.
Morte cellulaire liée au cuivre et opportunités médicamenteuses
PDHA1 est également lié à une forme de mort cellulaire récemment décrite et déclenchée par le cuivre, appelée cuproptose. L’étude a montré que bloquer la disponibilité du cuivre avec un médicament réduisait une protéine mitochondriale lipoylée associée à cette voie et affaiblissait la chaîne PDHA1–E2F1–PD-L1, en particulier lorsqu’il y avait en plus une inhibition de PDHA1. Des analyses génomiques et épigénétiques suggèrent qu’une forte expression de PDHA1 coïncide souvent avec des altérations de l’ADN, une hypométhylation du gène PDHA1 et des schémas de modifications de l’ARN associés à des tumeurs plus agressives. Des bases de données de criblage médicamenteux et des essais cellulaires ont mis en évidence plusieurs médicaments — tels que l’agent métabolique phenformine et un inhibiteur de la voie E2F1 — auxquels les sarcomes à PDHA1 active pourraient être particulièrement sensibles, suggérant des combinaisons rationnelles avec des inhibiteurs des points de contrôle immunitaires.
Transformer un mauvais signe en guide thérapeutique
Dans des modèles animaux et des biopsies de patients, les tumeurs à forte PDHA1 étaient plus volumineuses, plus prolifératives, plus riches en PD-L1 et moins infiltrées par les lymphocytes T CD8⁺ cytotoxiques. Pour autant, ces mêmes tumeurs à PDHA1 élevée montraient aussi des caractéristiques — comme une charge mutationnelle plus élevée et des signaux de points de contrôle renforcés — souvent associées à de meilleures réponses aux traitements bloquant PD-1 ou PD-L1. Dans une petite cohorte clinique de patients atteints de sarcome avancé traités par ce type d’immunothérapie, ceux dont les tumeurs exprimaient beaucoup de PDHA1 étaient plus susceptibles de bénéficier du traitement. Pour un lecteur non spécialiste, la conclusion est que PDHA1 agit à la fois comme un accélérateur de la croissance du sarcome et comme un bouclier contre l’attaque immunitaire, mais que ce comportement peut rendre ces tumeurs plus vulnérables une fois que les bons freins sont appliqués. Mesurer et cibler PDHA1 pourrait donc aider à identifier les patients à haut risque, guider l’utilisation de l’immunothérapie et inspirer de nouvelles combinaisons métaboliques–immunitaires pour les sarcomes récalcitrants.
Citation: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Mots-clés: immunothérapie des sarcomes, métabolisme du cancer, PDHA1, blocage des points de contrôle immunitaires, microenvironnement tumoral