Clear Sky Science · he
PDHA1 הקשורה לקופרופטוזיס מקדמת התקדמות סרקומה ותגובתיות לאימונותרפיה דרך ציר E2F1–PD-L1: מחקר ולידציה רב-אומיקס וקליני
מדוע מחקר זה חשוב
סרקומות הן סוגים נדירים אך אגרסיביים של סרטן שלעתים קרובות עמידים לטיפולים אימונולוגיים מודרניים. מטופלים רבים במחלה מתקדמת סיימו את האופציות הסטנדרטיות כגון ניתוח, כימותרפיה וקרינה, ועדיין סובלים מהישרדות לקויה. המחקר הזה בוחן מתג מטבולי סמוי בתוך תאי הסרקומה שנראה כי הוא גם מדליק את גדילת הגידול וגם מעצב את תגובת המערכת החיסונית. הבנת המתג הזה עשויה לפתוח דרכים חדשות לחיזוי אילו מטופלים יפיקו תועלת מאימונותרפיה ולעיצוב טיפולים משולבים חכמים יותר.
מנוע נסתר בתוך תאי הסרטן
במרכז הסיפור עומד PDHA1, חלבון הפועל כשער מרכזי בין פירוק הסוכר למחזור האנרגיה העיקרי של התא במיטוכונדריה. המחברים ניתחו מאגרי נתונים גדולים של סרטן ודגימות קליניות ומצאו שסרקומות נושאות ברמות PDHA1 גבוהות יותר באופן עקבי מרקמות תקינות. מטופלים שלגידוליהם היה PDHA1 גבוה נטו לשרוד זמן קצר יותר, ללא תלות בגיל, מין או מספר גורמים קליניים אחרים. על ידי שילוב רמות PDHA1 עם מידע קליני סטנדרטי, בניית הכלי החזויתי העריכה את הסיכוי לשרידות של שנה, שלוש וחמש שנים באופן מדויק יותר מאשר מדדים מסורתיים בלבד.
כיצד המטבוליזם מעצב את סביבת הגידול
מעבר לתפקודו בקידום הגדילה, נראה כי PDHA1 מעצב את השכונה של הגידול — תערובת תאי החיסון והתמיכה המקיפה את הסרטן. שימוש בשיטות חישוביות המסקנות סוגי תאי חיסון מרנ״א גולמי של גידול, וכן רצף תא-יחיד של תאים חיסוניים בודדים, הראו כי PDHA1 פעיל לא רק בתאי הגידול אלא גם ברוב אוכלוסיות החיסון, במיוחד בתאי T ותאי מיואיד. בסרקומות עם PDHA1 גבוה נצפו סימנים למצב "מנוצל על ידי חיסון" (immune-excluded): פחות תאי T קטלניים מועילים עמוק בתוך הגידול, יותר סימנים לרקמת מחיצה קשיחה וסיבית, ודפוסים המצביעים על כך שתאי חיסון נשמרו בשוליים במקום שיורשו לתקוף.
שרשרת מולקולרית שחוסמת את המתקפה החיסונית
ניסויים במעבדה חשפו כיצד PDHA1 מקשר בין מטבוליזם להימנעות חיסונית. כאשר החוקרים הקטינו את רמות PDHA1 בקו תאי סרקומה, התאים התחלקו פחות, זזו פחות, הקימו פחות מושבות ועברו יותר מוות מתוכנת. במקביל, רמות E2F1 — רגולטור גרעיני של גנים המעורבים בחלוקת התא — ו-PD-L1 — "בלם" חיסוני על פני תאי הגידול — ירדו שניהם. בבחינה של נתוני קשירת DNA ציבוריים ובניסויים ממוקדים, הצוות הראה כי E2F1 נקשר ישירות לאזור הבקרה של גן PD-L1 ומדליק אותו. שיחזור E2F1 בתאים חסרי PDHA1 החזיר את PD-L1 במידה מסוימת והציל חלקית את הישרדות התאים, וממקם את PDHA1 כמפעיל מקדים של שרשרת E2F1–PD-L1 המסייעת לגידולים להסתתר מתאי T.
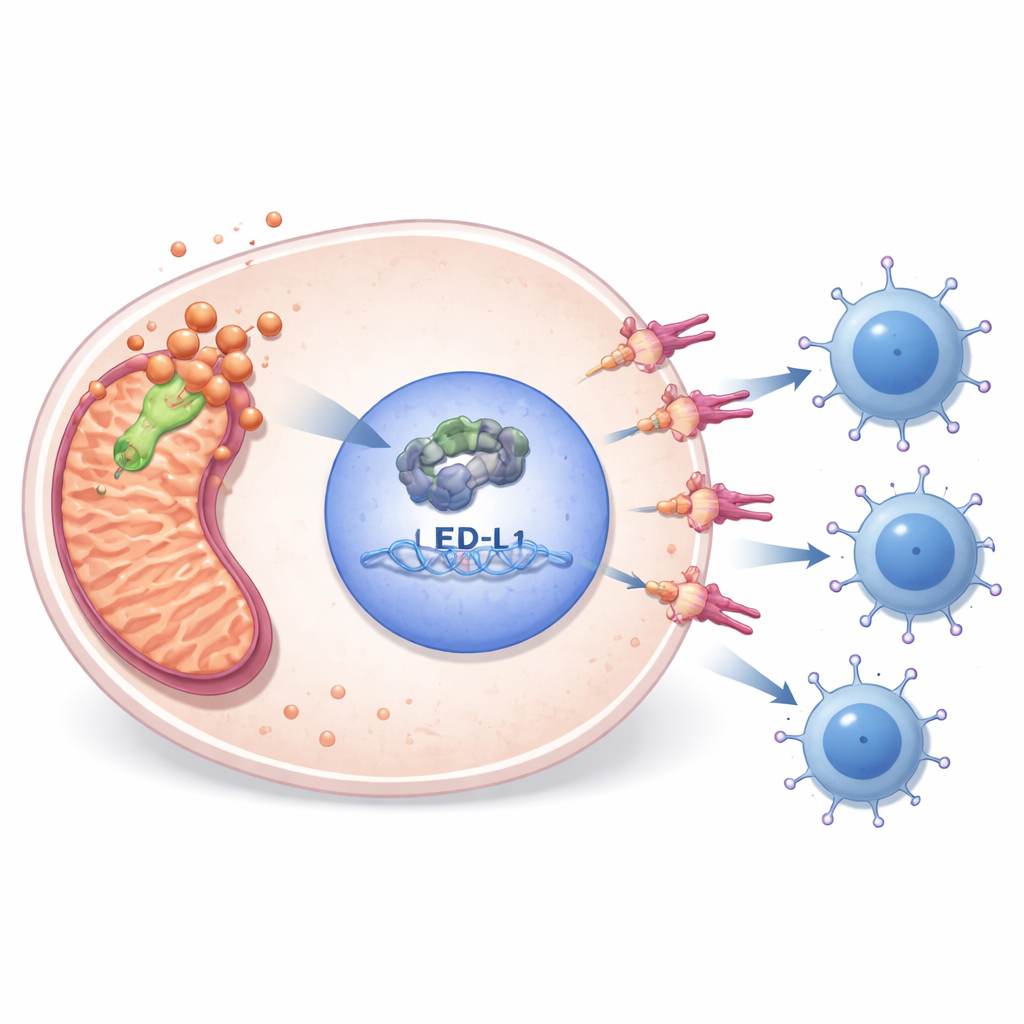
מוות תאי הקשור לנחושת והזדמנויות תרופתיות
PDHA1 קשור גם לצורת מוות תאי שתוארה לאחרונה ומופעלת על ידי נחושת, הנקראת קופרופטוזיס. המחקר הראה כי חסימת זמינות הנחושת באמצעות תרופה הפחיתה חלבון מיטוכונדריאלי ליפויילי המקושר למסלול זה והחלישה את שרשרת PDHA1–E2F1–PD-L1, במיוחד כאשר שולבה עם השתקת PDHA1. ניתוחים גנומיים ואפיגנטיים הצביעו על כך שרמות PDHA1 גבוהות לרוב מצויות יחד עם שינויים ב-DNA, חוסר מתילציה נמוכה של גן PDHA1, ודפוסי שינויי RNA הקשורים לגידולים אגרסיביים יותר. מאגרי סקר תרופות ובדיקות תאים הצביעו על כמה תרופות — כגון האגנט המטבולי פנפורמינים ומעכב נתיב E2F1 — שעל פיהן סרקומות עם PDHA1 פעיל עשויות להיות רגישות באופן מיוחד, ומרמזים על שיתופים הגיוניים עם מעכבי נקודות הביקורת החיסוניות.
הפיכת סימן רע למדריך טיפול
בדגמי חיות ובביופסיות של מטופלים, גידולים עם PDHA1 גבוה היו גדולים יותר, פרוליפרטיביים יותר, עשירים יותר ב-PD-L1 ודלים יותר בכיליון של תאי CD8⁺ קטלניים. עם זאת, אותם גידולים בעלי PDHA1 גבוה הראו גם תכונות — כגון עומס מוטציות גבוה יותר ואיתותי נקודות ביקורת חזקים יותר — שלעתים קרובות מקושרות לתגובות טובות יותר לתרופות החוסמות PD-1 או PD-L1. בקוהורט קליני קטן של מטופלים עם סרקומה מתקדמת שקיבלו אימונותרפיה כזו, אלה עם PDHA1 גבוה היו סבירות יותר להפיק תועלת. באופן פשוט, המסקנה היא כי PDHA1 פועל גם כדוושת תאוצה לצמיחת סרקומה וגם כמגן מפני מתקפה חיסונית, אך התנהגות זו עשויה להפוך לפגועה בשלב שבו מוחלים ה"בלמים" הנכונים. מדידה ומיקוד של PDHA1 יכולים לכן לסייע בזיהוי מטופלים בסיכון גבוה, לכוון שימוש באימונותרפיה ולעודד שילובים חדשים של תרופות מטבוליות–חיסוניות עבור סרקומות עקשניות.
ציטוט: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
מילות מפתח: אימונותרפיה לסרקומה, מטבוליזם של סרטן, PDHA1, חסימת נקודות ביקורת חיסוניות, מיקרוסביבת גידול