Clear Sky Science · ar
البروتين المرتبط بالموت الخلوي بالزئبق PDHA1 يعزّز تقدم الساركوما واستجابة العلاج المناعي عبر محور E2F1–PD-L1: دراسة متعددة الأومكس والتحقق السريري
لماذا يهم هذا البحث
الساركوما أورام نادرة لكنها عدوانية وغالباً ما تقاوم العلاجات المناعية الحديثة. الكثير من المرضى ذوي المرض المتقدّم تستنفد الخيارات القياسية مثل الجراحة والعلاج الكيميائي والإشعاعي، ومع ذلك يواجهون نتائج بقاء ضعيفة. تستكشف هذه الدراسة مفتاحاً استقلابياً مخفياً داخل خلايا الساركوما يبدو أنه يغذي نمو الورم ويشكّل في الوقت نفسه استجابة الجهاز المناعي. فهم هذا المفتاح قد يفتح طرقاً جديدة للتنبؤ بمن سيستفيد من العلاج المناعي وتصميم تراكيبات علاجية أكثر ذكاءً.
محرك خفي داخل خلايا السرطان
في صلب القصة يقف PDHA1، بروتين يعمل كبوابة رئيسية بين تحلل السكر ودورة الطاقة الأساسية في الميتوكوندريا. حلّل المؤلفون قواعد بيانات سرطانية واسعة وعينات سريرية ووجدوا أن الساركومات تحمل باستمرار مستويات أعلى من PDHA1 مقارنة بالأنسجة الطبيعية. المرضى الذين كانت أورامهم غنية بـPDHA1 كانوا يميلون إلى العيش لفترات أقصر، بغض النظر عن العمر أو الجنس أو عدة عوامل سريرية أخرى. بدمج مستويات PDHA1 مع معلومات سريرية اعتيادية، بنى الفريق أداة تنبؤية قدّرت البقاء لمدة سنة وثلاث وخمس سنوات بدقة أكبر من المقاييس التقليدية وحدها.
كيف يشكّل الاستقلاب محيط الورم
بعيداً عن تحفيز النمو فقط، بدا أن PDHA1 يعيد تشكيل محيط الورم — مزيج الخلايا المناعية والخلايا الداعمة المحيطة بالسرطان. باستخدام طرق حاسوبية تستنتج أنواع الخلايا المناعية من رنا إجمالي للورم، فضلاً عن تسلسل الخلايا المفردة للخلايا المناعية، أظهر المؤلفون أن PDHA1 نشط ليس فقط في خلايا الورم وإنما عبر مجموعات من الخلايا المناعية، خصوصاً الخلايا التائية والخلايا النخاعية. الساركومات ذات PDHA1 المرتفع كانت تميل لإظهار حالة «استبعاد مناعي»: خلايا قاتلة تائية مفيدة أقل داخل عمق الورم، ومؤشرات لنسيج داعم ليفي صلب، وأنماط توحي بأن الخلايا المناعية حُوصرت على الحواف بدل السماح لها بالهجوم.
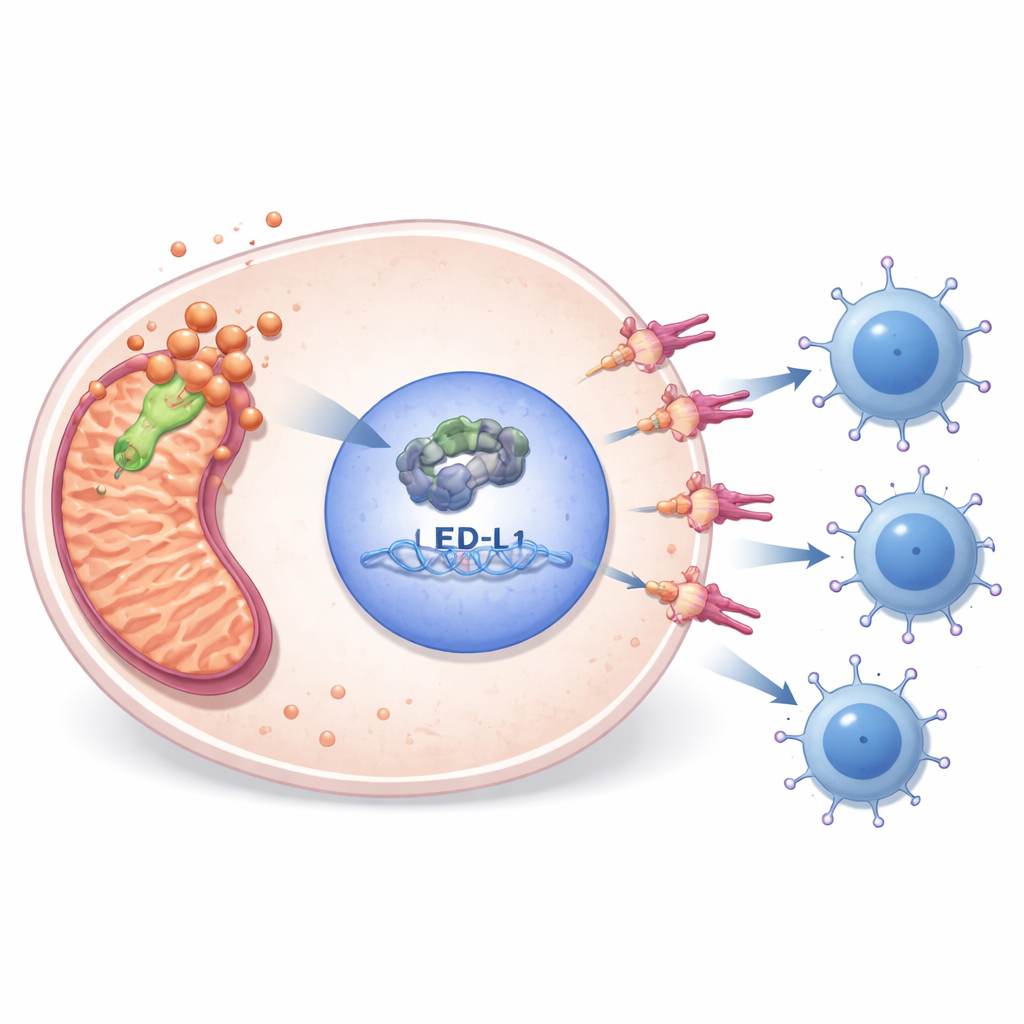
سلسلة جزيئية تمنع الهجوم المناعي
كشفت التجارب المخبرية كيف يربط PDHA1 بين الاستقلاب والهروب المناعي. عندما قلّل الباحثون من مستويات PDHA1 في خطوط خلايا الساركوما، انخفضت قدرة الخلايا على الانقسام، وقلت حركتها، وتكوّنت مستعمرات أقل، وازدادت الخلايا التي دخلت في موت مبرمج. في الوقت نفسه، انخفضت مستويات E2F1 — منظم نووي للجينات المشاركة في انقسام الخلايا — وPD-L1 — «مكبّح» مناعي على سطح خلايا الورم. من خلال فحص بيانات ربط الحمض النووي العامة وإجراء تجارب مستهدفة، أظهر الفريق أن E2F1 يرتبط مباشرة بمنطقة التحكم في جين PD-L1 ويشغّله. إعادة E2F1 إلى خلايا ناقصة PDHA1 أعادت رفع PD-L1 وأنقذت البقاء الجزئي للخلايا، ما يضع PDHA1 أعلى سلسلة E2F1–PD-L1 التي تساعد الأورام على الاختباء من الخلايا التائية.
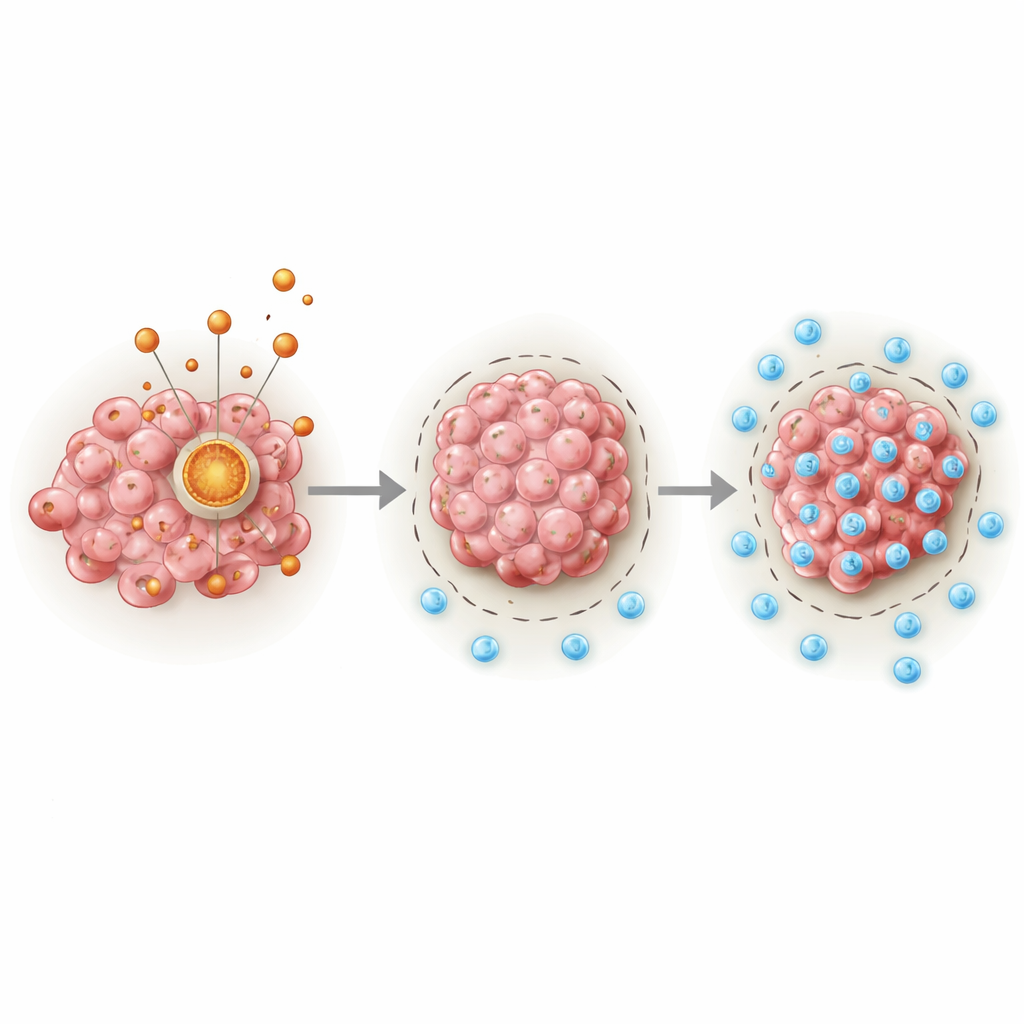
موت خلوي مرتبط بالنحاس وفرص دوائية
يرتبط PDHA1 أيضاً بنوع حديث الوصف من موت الخلايا يُستَثار بواسطة النحاس، يسمى الموت النحاسي (cuproptosis). أظهرت الدراسة أن حجب توافر النحاس بدواء خفّض بروتيناً ميتوكوندرياً ليوبيلياً مرتبطاً بهذا المسار وقلّل سلسلة PDHA1–E2F1–PD-L1، لا سيما عند الجمع مع خفض PDHA1. أشارت التحليلات الجينومية والابيجينية إلى أن ارتفاع PDHA1 غالباً ما يتزامن مع تغيّرات في الحمض النووي، وانخفاض مثيلة جين PDHA1، وأنماط تعديل رنا مرتبطة بأورام أكثر عدوانية. دلّت قواعد بيانات فحص الأدوية وتجارب الخلايا على عدة أدوية — مثل العامل الاستقلابي فينفورمين ومثبط مسار E2F1 — التي قد تكون الساركومات ذات PDHA1 النشط حساسة لها بشكل خاص، مما يوحي بتراكيب منطقية مع مثبطات نقاط التفتيش المناعية.
تحويل علامة سيئة إلى دليل علاجي
في نماذج حيوانية وخزعات مرضى، كانت الأورام ذات PDHA1 المرتفع أكبر وأكثر تكاثراً، وأكثر غنى بـPD-L1، وأقل تسلل للخلايا القاتلة CD8⁺. ومع ذلك، أظهرت هذه الأورام المرتفعة أيضاً خصائص — مثل عبء طفرات أعلى وإشارات نقاط تفتيش أقوى — التي غالباً ما ترتبط باستجابات أفضل للأدوية التي تحجب PD-1 أو PD-L1. في مجموعة سريرية صغيرة من مرضى الساركوما المتقدّم الذين خضعوا لمثل هذا العلاج المناعي، كان المرضى ذوو PDHA1 المرتفع أكثر احتمالاً للاستفادة. بالخلاصة للقارئ العام، يعمل PDHA1 كدعسة غاز لنمو الساركوما وكسِترَة تحميها من الهجوم المناعي، لكن هذا السلوك نفسه قد يجعل هذه الأورام أكثر عرضة بمجرد تطبيق المكابح الصحيحة. لذا قد تساعد قياس واستهداف PDHA1 في تحديد المرضى ذوي المخاطر العالية، توجيه استخدام العلاج المناعي، وإلهام تراكيب دوائية استقلابية-مناعية جديدة للساركومات المقاومة.
الاستشهاد: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
الكلمات المفتاحية: العلاج المناعي للساركوما, استقلاب السرطان, PDHA1, حجب نقاط التفتيش المناعية, البيئة الدقيقة للورم