Clear Sky Science · pl
PDHA1 związany z cuproptoza promuje progresję mięsaka i wrażliwość na immunoterapię poprzez oś E2F1–PD-L1: badanie wieloomiczne i walidacja kliniczna
Dlaczego to badanie ma znaczenie
Mięsaki są rzadkimi, lecz agresywnymi nowotworami, które często opierają się nowoczesnym terapiom opartym na układzie odpornościowym. Wielu chorych z zaawansowaną chorobą wykorzystuje standardowe opcje leczenia, takie jak chirurgia, chemioterapia i radioterapia, a mimo to ich przeżycie pozostaje krótkie. W tej pracy zbadano ukryty metaboliczny przełącznik w komórkach mięsaka, który wydaje się napędzać wzrost guza i jednocześnie kształtować odpowiedź immunologiczną. Zrozumienie tego mechanizmu może otworzyć nowe możliwości przewidywania, którzy pacjenci skorzystają z immunoterapii, oraz projektowania bardziej przemyślanych terapii skojarzonych.
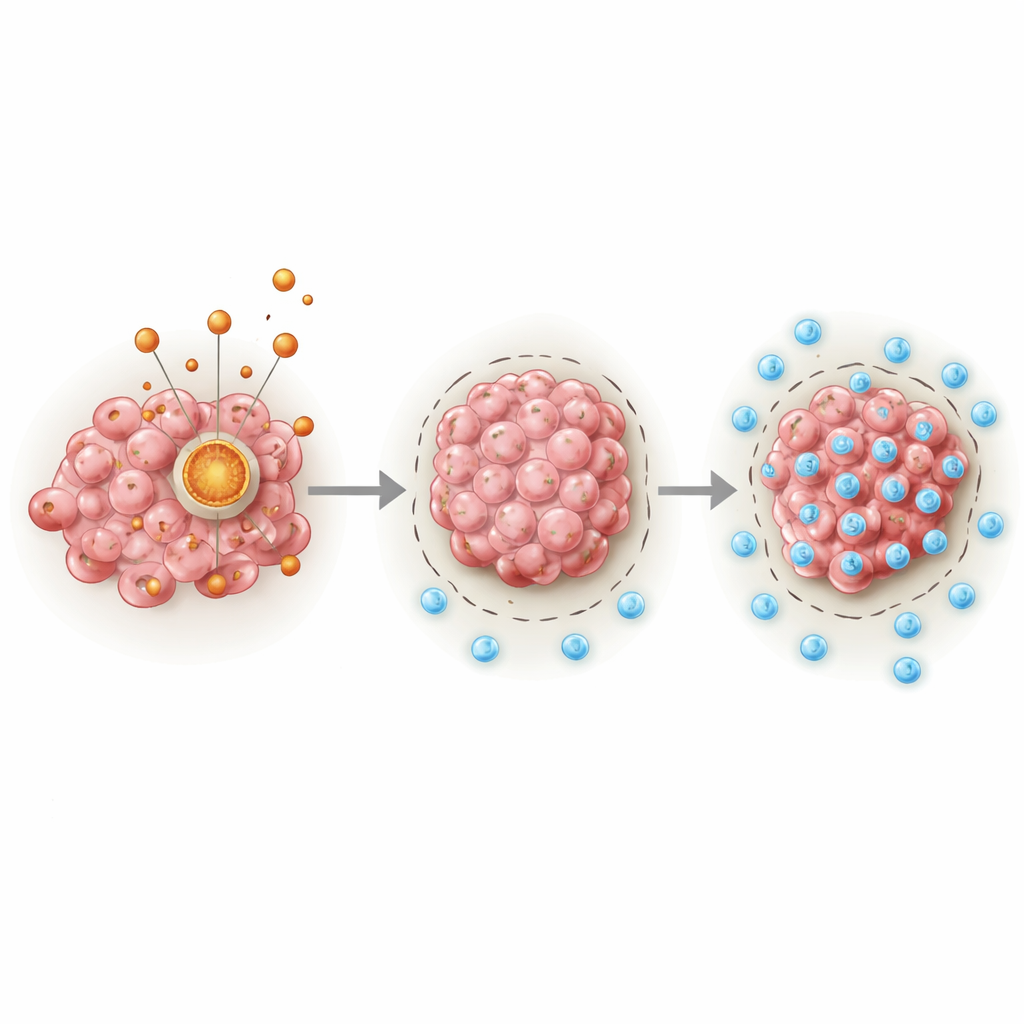
Ukryty silnik wewnątrz komórek nowotworowych
W centrum opisywanej historii znajduje się PDHA1, białko pełniące rolę kluczowego węzła pomiędzy rozkładem cukrów a głównym cyklem energetycznym w mitochondriach. Autorzy przeanalizowali obszerne bazy danych nowotworowych i próbki kliniczne, wykazując, że mięsaki stale wykazują wyższe poziomy PDHA1 niż tkanki prawidłowe. Pacjenci, których guzy miały podwyższone PDHA1, mieli skłonność do krótszego przeżycia, niezależnie od wieku, płci czy kilku innych czynników klinicznych. Łącząc poziomy PDHA1 ze standardowymi informacjami klinicznymi, zespół zbudował narzędzie prognostyczne, które dokładniej estymowało przeżycie jednoroczne, trzy- i pięcioletnie niż tradycyjne miary.
Jak metabolizm kształtuje mikrośrodowisko guza
Ponad mechanizmem wzrostu, PDHA1 wydawał się przebudowywać otoczenie guza — miks komórek odpornościowych i podporowych otaczających nowotwór. Korzystając z metod obliczeniowych wyprowadzających typy komórek odpornościowych z danych RNA z tkanki guzowej oraz z sekwencjonowania pojedynczych komórek, autorzy pokazali, że PDHA1 jest aktywny nie tylko w komórkach nowotworowych, lecz także w wielu populacjach immunologicznych, zwłaszcza w limfocytach T i komórkach mieloidalnych. Mięsaki o wysokim PDHA1 miały cechy stanu „wykluczenia immunologicznego”: mniej pomocnych cytotoksycznych limfocytów T głęboko wewnątrz guza, więcej sygnałów włóknistej, sztywnej zrębu oraz wzorce sugerujące, że komórki odpornościowe były utrzymywane na obrzeżach zamiast dopuszczane do ataku.
Cząsteczkowy łańcuch blokujący atak immunologiczny
Eksperymenty laboratoryjne ujawniły, jak PDHA1 łączy metabolizm z ucieczką przed układem odpornościowym. Gdy badacze obniżyli poziom PDHA1 w liniach komórkowych mięsaka, komórki dzieliły się rzadziej, poruszały się mniej, tworzyły mniej kolonii i częściej przechodziły zaprogramowaną śmierć komórkową. Jednocześnie spadły poziomy E2F1 — jądrowego regulatora genów związanych z podziałem komórkowym — oraz PD-L1 — „hamulca” immunologicznego na powierzchni komórek nowotworowych. Analiza publicznych danych dotyczących wiązania DNA oraz ukierunkowane eksperymenty wykazały, że E2F1 bezpośrednio wiąże się z regionem kontrolnym genu PD-L1 i go aktywuje. Przywrócenie E2F1 w komórkach pozbawionych PDHA1 odtworzyło ekspresję PD-L1 i częściowo uratowało przeżywalność komórek, umieszczając PDHA1 powyżej osi E2F1–PD-L1, która pomaga nowotworom ukrywać się przed limfocytami T.
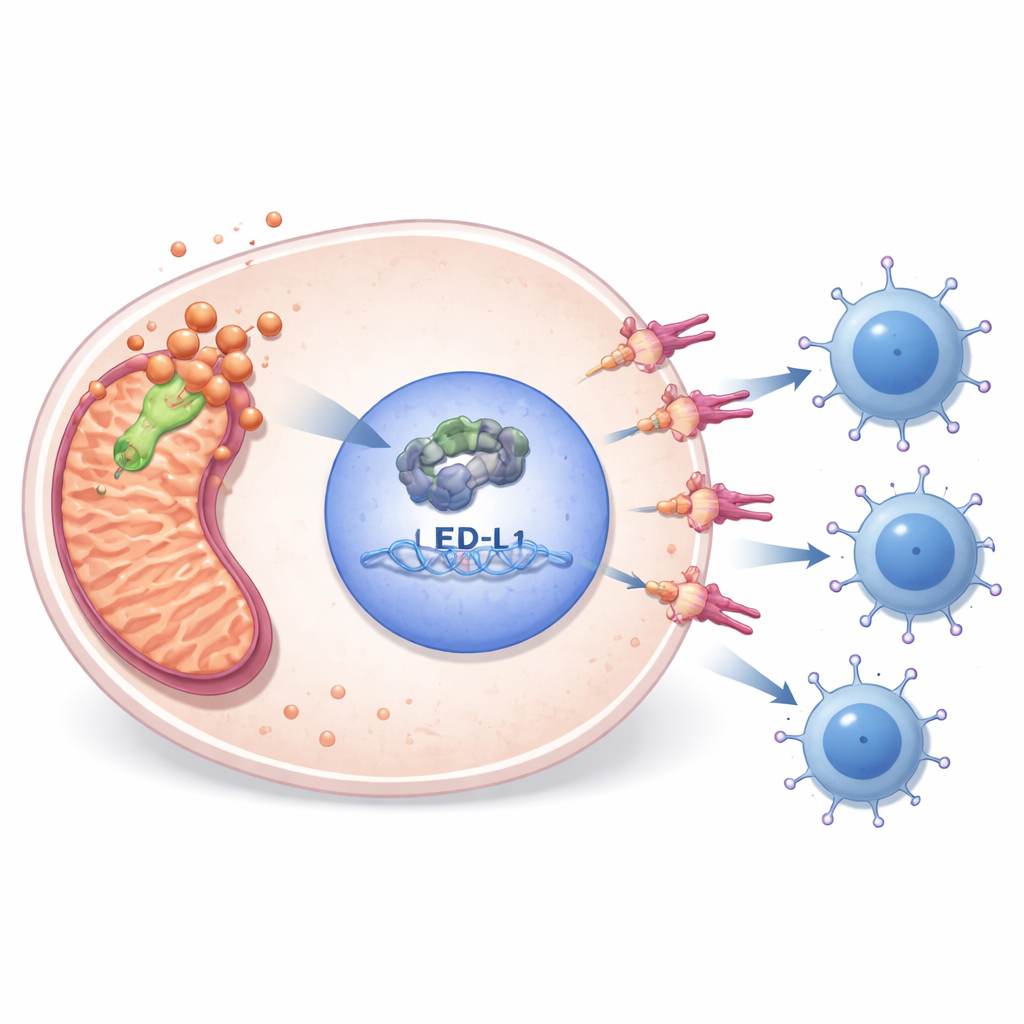
Śmierć komórkowa związana z miedzią i możliwości terapeutyczne
PDHA1 wiąże się również z niedawno opisanym typem śmierci komórkowej wywoływanym przez miedź, zwanym cuproptozą. Badanie wykazało, że blokowanie dostępności miedzi za pomocą leku obniżało poziom lipoilowanego białka mitochondrialnego powiązanego z tą ścieżką i osłabiało łańcuch PDHA1–E2F1–PD-L1, zwłaszcza w połączeniu z zahamowaniem PDHA1. Analizy genomowe i epigenetyczne sugerowały, że wysoki PDHA1 często współistnieje ze zmianami DNA, niskim metylowaniem genu PDHA1 i wzorcami modyfikacji RNA związanymi z bardziej agresywnymi guzami. Bazy danych z ekranami lekowymi i eksperymenty komórkowe wskazały kilka substancji — takich jak lek metaboliczny fenformina i inhibitor ścieżki E2F1 — na które mięsaki z aktywnym PDHA1 mogą być szczególnie wrażliwe, sugerując racjonalne kombinacje z inhibitorami punktów kontrolnych immunologicznych.
Przekształcanie złego prognostyka w wskazówkę terapeutyczną
W modelach zwierzęcych i biopsjach pacjentów guzy o wysokim PDHA1 były większe, bardziej proliferujące, bogatsze w PD-L1 i słabiej infiltrujące przez cytotoksyczne limfocyty CD8⁺. Jednocześnie te same guzy o wysokim PDHA1 wykazywały cechy — takie jak wyższe obciążenie mutacyjne i silniejsze sygnały punktów kontrolnych — które często wiążą się z lepszą odpowiedzią na leki blokujące PD-1 lub PD-L1. W małej kohorcie klinicznej pacjentów z zaawansowanym mięsakem leczonych taką immunoterapią osoby z wysokim PDHA1 częściej odnosiły korzyść. Dla czytelnika niebędącego specjalistą wniosek jest taki, że PDHA1 działa zarówno jako pedał gazu napędzający wzrost mięsaka, jak i tarcza przeciw atakowi immunologicznemu, lecz to właśnie to zachowanie może uczynić te guzy bardziej podatnymi, gdy zastosuje się odpowiednie „hamulce”. Pomiar i ukierunkowanie PDHA1 może więc pomóc zidentyfikować pacjentów wysokiego ryzyka, poprowadzić stosowanie immunoterapii i zainspirować nowe kombinacje leków metabolicznych i immunologicznych przeciw opornym mięsakom.
Cytowanie: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Słowa kluczowe: immunoterapia mięsaka, metabolizm nowotworu, PDHA1, blokada punktów kontrolnych układu odpornościowego, mikrośrodowisko guza