Clear Sky Science · ja
銅依存性細胞死関連のPDHA1はE2F1–PD-L1軸を介して肉腫の進展と免疫療法応答性を促進する:マルチオミクスおよび臨床検証研究
この研究が重要な理由
肉腫は稀ではあるものの侵襲性が高く、しばしば最新の免疫療法に抵抗します。進行例の多くは手術、化学療法、放射線といった標準的治療を使い尽くしても生存率が低いままです。本研究は、肉腫細胞内に潜む代謝のスイッチが腫瘍成長を促すだけでなく免疫応答の様相をも左右していることを明らかにしようとしています。このスイッチを理解することで、どの患者が免疫療法から利益を得るかを予測したり、より効果的な併用療法を設計したりする新たな道が開ける可能性があります。
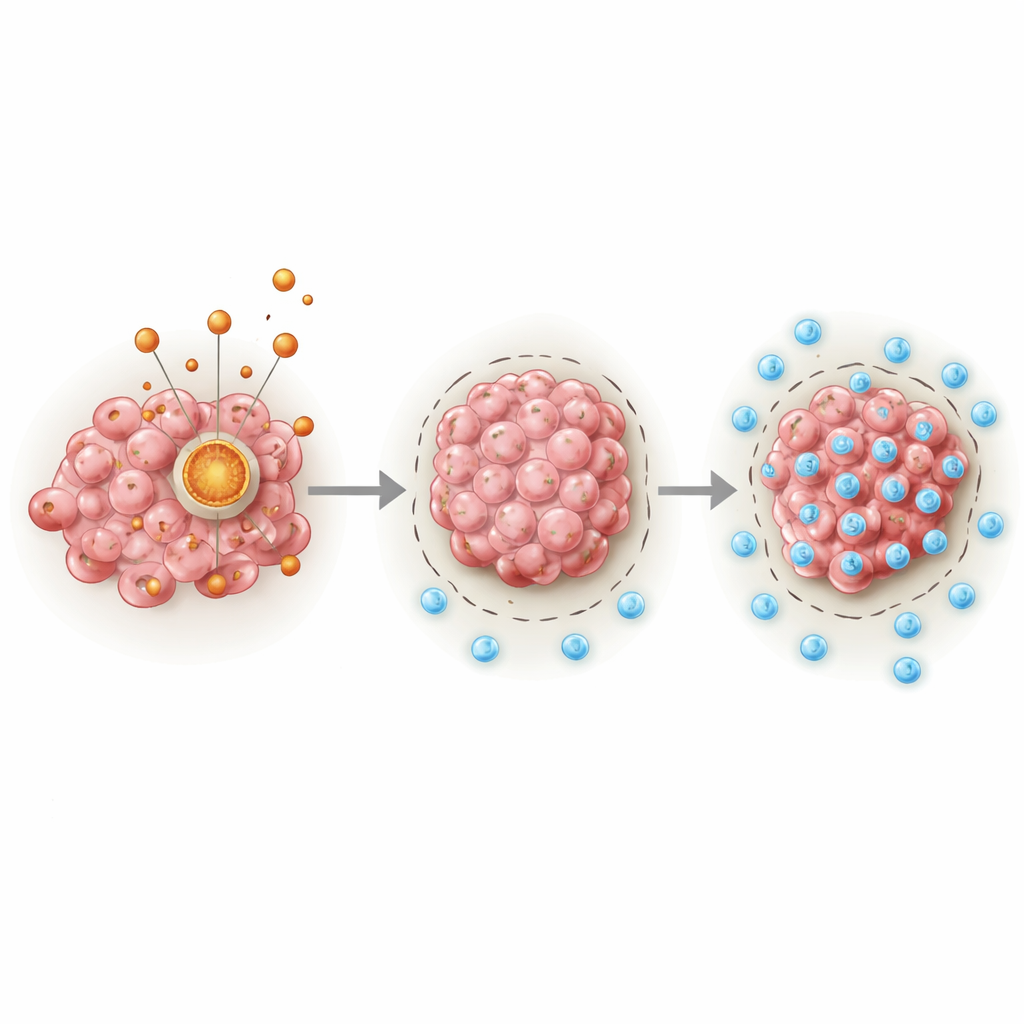
がん細胞内の隠れたエンジン
本研究の中心にあるのはPDHA1というタンパク質で、糖の分解とミトコンドリアにおける主要なエネルギーサイクルとをつなぐ重要なゲートウェイとして働きます。著者らは大規模ながんデータベースと臨床試料を解析し、肉腫は正常組織より一貫してPDHA1の発現が高いことを見出しました。腫瘍でPDHA1が高い患者は、年齢や性別、その他の臨床因子にかかわらず生存期間が短い傾向がありました。PDHA1のレベルと標準的な臨床情報を組み合わせることで、従来の指標よりも1年、3年、5年生存率をより正確に推定する予測ツールを構築しました。
代謝が腫瘍の“周辺”を形作る仕組み
単に増殖を駆動するだけでなく、PDHA1は腫瘍を取り巻く環境―免疫細胞や支持細胞の構成にも影響を与えるようでした。バルク腫瘍RNAから免疫細胞型を推定する計算手法や、個々の免疫細胞のシングルセルシーケンスを用いて解析すると、PDHA1は腫瘍細胞だけでなくT細胞や髄系細胞をはじめ多数の免疫集団でも活性を示しました。PDHA1が高い肉腫は“免疫排除”状態の特徴を示す傾向がありました。すなわち、腫瘍深部に浸潤する有効なキラーT細胞が少なく、硬く線維化した間質の兆候が強く、免疫細胞が腫瘍の周縁に留められて攻撃できないようなパターンが見られました。
免疫攻撃を遮る分子の連鎖
実験室での検証は、PDHA1が代謝と免疫逃避をつなぐ仕組みを明らかにしました。肉腫細胞株でPDHA1を減らすと、細胞の分裂や運動、コロニー形成が抑えられ、プログラム細胞死が増加しました。同時に、細胞分裂に関与する遺伝子の核内制御因子であるE2F1と、腫瘍細胞表面の免疫“ブレーキ”であるPD-L1の両方のレベルが低下しました。公開されているDNA結合データの解析と標的実験により、E2F1がPD-L1遺伝子の制御領域に直接結合してそれをオンにすることが示されました。PDHA1欠損細胞でE2F1を回復させるとPD-L1が再上昇し細胞生存が部分的に回復したため、PDHA1がE2F1–PD-L1という連鎖の上流に位置し、腫瘍がT細胞から身を隠すのに寄与していることが示されました。
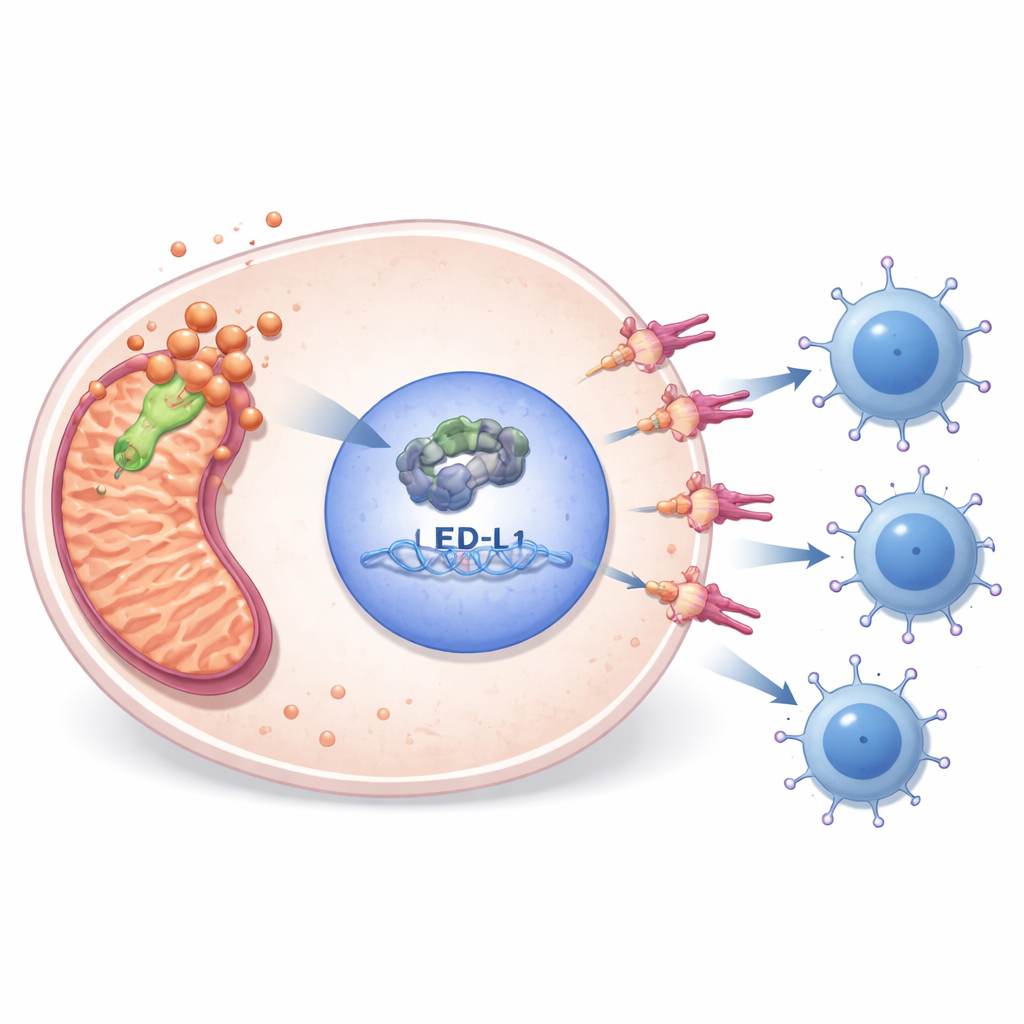
銅連結型の細胞死と薬剤の可能性
PDHA1は、銅によって誘導される最近記述された細胞死の一形態であるcuproptosis(クプロプトーシス)とも関連しています。本研究では、銅の利用可能性を阻害する薬剤がこの経路に関連するリポイル化ミトコンドリアタンパク質を低下させ、特にPDHA1ノックダウンと併用した場合にPDHA1–E2F1–PD-L1連鎖を弱めることを示しました。ゲノムおよびエピジェネティックな解析は、PDHA1高発現がしばしばDNA変化、PDHA1遺伝子の低メチル化、より攻撃的な腫瘍に関連するRNA修飾パターンと一致することを示唆しました。薬剤スクリーニングデータベースと細胞ベースのアッセイは、代謝薬のフェンフォルミンやE2F1経路阻害剤など、PDHA1が活性な肉腫で特に感受性が高い可能性のある薬剤をいくつか示し、免疫チェックポイント阻害剤との合理的な併用の手がかりを与えました。
悪い徴候を治療の指針に変える
動物モデルおよび患者生検において、PDHA1高発現の腫瘍は大きく、増殖性が高く、PD-L1が豊富で、CD8⁺キラーT細胞の浸潤が乏しい傾向がありました。一方で、これらの高PDHA1腫瘍は高い変異負荷や強いチェックポイントシグナルなど、PD-1/PD-L1阻害薬に対する良好な反応と関連する特徴も示していました。小規模な進行肉腫患者コホートで免疫療法を受けた症例では、PDHA1が高い患者が利益を得やすい傾向が見られました。一般向けに言えば、PDHA1は肉腫の成長のアクセルであると同時に免疫攻撃に対するシールドとして働きますが、その性質が適切な“ブレーキ”をかける治療と組み合わされると脆弱性にもなり得ます。PDHA1を測定・標的化することは、高リスク患者の同定、免疫療法の適用指針作成、および難治性肉腫に対する新しい代謝—免疫併用療法の創出に役立つ可能性があります。
引用: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
キーワード: 肉腫の免疫療法, がん代謝, PDHA1, 免疫チェックポイント阻害, 腫瘍微小環境